来源:中华胰腺病杂志
[ 编者按 ]
随着
2026年2月,欧洲胰腺俱乐部联合美国胰腺协会、国际胰腺病学会等国际权威学术组织,在《United European Gastroenterology Journal》上正式发布了《脂肪胰定义、诊断标准与管理的国际多学科共识报告》。李兆申院士/杜奕奇教授团队及时对该国际共识进行了深度解读,旨在为我国脂肪胰的规范化诊疗与高水平临床研究提供参考。
我们期待,这份共识解读能够引发国内同道对脂肪胰的更广泛关注与思考,在深化认知的基础上推动该领域的规范化诊疗,从而惠及广大患者。
摘 要
欧洲胰腺学会联合美国胰腺协会、国际胰腺病学会等多家国际专业组织,共同制定了《脂肪胰定义、诊断标准与管理的国际多学科共识报告》。该报告于2026年2月发表于欧洲胃肠病学联盟官方期刊《United European Gastroenterology Journal》,首次系统规范了脂肪胰的术语、诊断标准及临床管理策略。核心内容包括:明确推荐“脂肪胰”作为标准化统一术语;确立以
全文阅读
脂肪胰(fatty pancreas)是指胰腺组织内脂肪异常积聚的病理状态[1]。该概念自20世纪初提出,近年来因其与代谢性疾病、胰腺炎乃至胰腺癌的潜在关联而受到广泛关注。但目前脂肪胰的术语与定义尚未统一,给学术交流与临床实践带来显著障碍;其诊断主要依赖影像学检查,缺乏标准化方案;同时高质量前瞻性证据不足,临床意义与致病机制仍不明确。为此,欧洲胰腺学会联合美国胰腺协会、国际胰腺病学会等多家国际专业组织,共同制定了《脂肪胰定义、诊断标准和管理的国际多学科共识报告》[2]。作为脂肪胰领域的里程碑式文献,该共识报告首次系统规范了脂肪胰的术语、诊断标准及临床管理策略。本文对其核心内容进行解读,供国内同道参考。
一、术语定义
术语统一是规范诊疗、促进学术交流的基础。共识明确推荐使用“脂肪胰”作为描述胰腺内各种形式脂肪积聚的标准、通用术语。既往文献中曾出现的胰腺脂肪瘤病、胰腺脂肪变性、胰腺内脂肪浸润、非酒精性脂肪性胰腺病、胰腺内脂肪沉积、胰腺异位脂肪、胰腺脂肪替代及胰腺脂肪积聚等多种表述,均予以统一。
“非酒精性脂肪性胰腺病”虽然也较常用,命名方式也与代谢综合征相关的“
二、病因学
脂肪胰的发生与多种因素有关,包括衰老、肥胖、2型糖尿病、各种原因引起的炎症、纤维化、遗传性疾病及慢性胰管梗阻等。胰腺内、外多种细胞均可分化为胰腺内脂肪细胞,例如胰腺外分泌细胞转分化、组织驻留干细胞定向分化,或胰周脂肪等胰腺外脂肪前体细胞的浸润[4]。共识指出,脂肪胰的发生主要存在两种情形:一是与肥胖程度直接相关,二是由胰腺外分泌组织损伤丢失所致。具体病因分类见表1,该分类对临床实践具有重要指导意义,有助于避免对所有脂肪胰患者采取单一化干预方案。

三、与饮酒、吸烟的关系
现有可靠证据不支持饮酒、吸烟会增加脂肪胰患病率,也未证实二者与脂肪胰的发生、进展存在因果关联。部分观察性研究虽提示可能存在关联,但研究多为异质性较强的横断面设计,缺乏高质量前瞻性数据佐证。尽管生活方式干预是脂肪胰管理的基础环节,但目前尚无研究系统评估戒酒、戒烟能否预防脂肪胰的发生与进展。
四、流行病学
当前脂肪胰的流行病学特征仍不明确。受定义与诊断标准不统一的影响,不同研究报道的患病率差异较大。临床观察显示,脂肪胰的发生率随年龄、
五、组织病理学
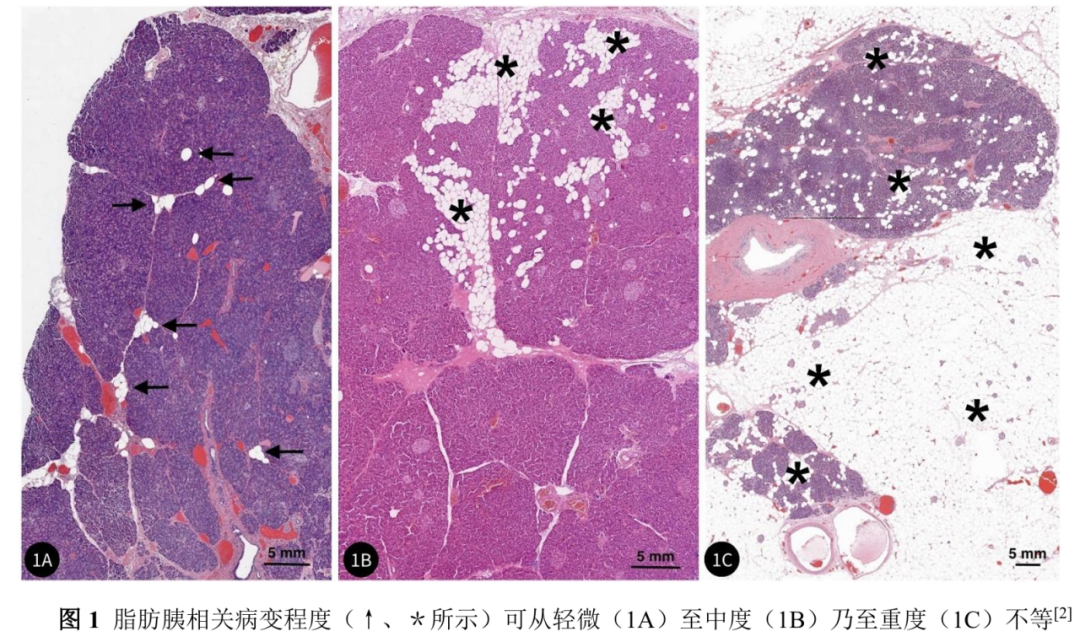
胰腺内出现非肿瘤性脂肪细胞是脂肪胰的核心病理特征。此类脂肪细胞形态成熟,内含单个大脂滴,可分布于胰腺小叶内、小叶间隙(小叶外);少数情况下,腺泡细胞与胰岛内分泌细胞内也可出现脂质沉积。脂肪细胞数量不等,少则几个散在分布,多则融合成片(图1)。广泛脂肪浸润常伴随腺泡实质丢失,最终形成大片脂肪组织中散在分布胰岛、导管或残留腺泡细胞簇的病理形态。
大体观上,病变进展期胰腺可呈大理石样外观,质地明显变软[5]。脂肪胰的病理改变多呈斑片状、不均匀分布,胰周组织交界区的浅表小叶更易受累[6]。现有证据未发现脂肪细胞浸润增多伴随炎症、纤维化加重,因此胰腺并不存在类似肝脏“脂肪变性→脂肪性肝炎”的进展过程。
目前脂肪胰的组织学分级方法多样,包括视觉半定量评估、脂肪细胞占胰腺组织面积比例、高倍视野脂肪细胞计数、图像自动形态计量分析等,但尚无公认且经过验证的客观分级标准,组织形态学特征与诊断标准仍未达成共识。
六、影像学诊断
临床与研究中可采用经腹超声、CT和MRI等影像学手段评估脂肪胰的存在及严重程度。
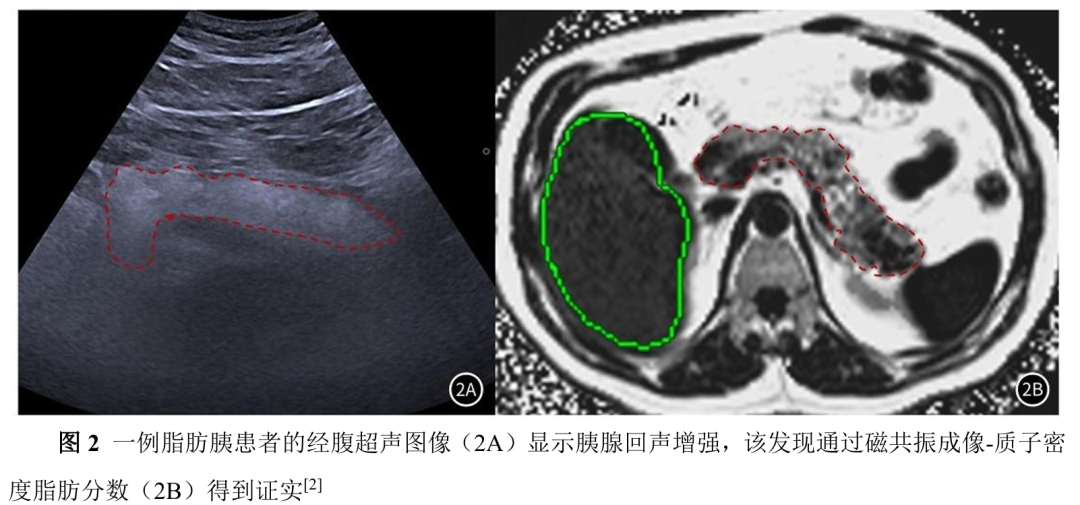
经腹超声检查可初步提示脂肪胰,表现为胰腺回声增强(图2A)。但回声强度易受纤维化、炎症、钙化等病理因素干扰;加之胰腺位于腹膜后,肥胖患者检查难度大,观察者间差异较大。临床常以胰腺回声与肝脏、脾脏、肾脏等邻近器官对比,采用无、轻、中、重四级半定量法评估严重程度[7]。若参照器官(如肝脏)合并脂肪变性,对比结果的可靠性下降,且该分级未与其他影像学方法对照验证。因此,经腹超声受操作者依赖性、技术易变性及标准不一致的限制,诊断可靠性与严重程度评估价值有限。
CT可辅助诊断脂肪胰,对中重度病例敏感性较高,但难以检出轻度脂肪胰。CT可实现全胰腺评估,脂肪胰表现为胰腺CT值衰减降低,测量目标区域亨斯菲尔德单位(HU)可定量评估脂肪浸润程度。但不同CT设备的扫描参数、对比剂剂量存在差异,影响结果的可重复性。此外,轻度脂肪沉积在CT上可表现为低密度(即所谓“隐形脂肪”),难以明确诊断。同时CT存在辐射暴露风险。与病理对照研究证实,平扫CT胰腺/脾脏密度比<0.7可作为脂肪胰的诊断标准[8]。
MRI,尤其是质子密度脂肪分数(proton density fat fraction,PDFF)序列,是胰腺脂肪定量的最可靠影像学手段(图2B)。其优势在于可快速完成全胰腺评估,测得的脂肪分数与组织学结果高度相关[9]。结合临床观察与专家意见,共识将脂肪胰分为三级:轻度(6%~15% PDFF)、中度(16%~30% PDFF)、重度(>30% PDFF)。
脂肪胰可呈不均匀分布,有时可模拟局灶性病变,如局灶性脂肪替代、脂肪瘤性假性肥大、远端胰腺发育不全等;部分胰腺肿瘤(如脂肪瘤、胰母细胞瘤)可含脂肪成分,
七、超声内镜诊断
超声内镜(endoscopic ultrasound,EUS)可通过回声定性评估诊断脂肪胰,典型表现为胰腺实质回声高于脾脏或邻近器官,这是脂肪浸润增加声波反射所致。但目前EUS高回声表现与组织学脂肪浸润的相关性尚未证实,且出于安全性考虑,不推荐常规行EUS引导下组织活检。
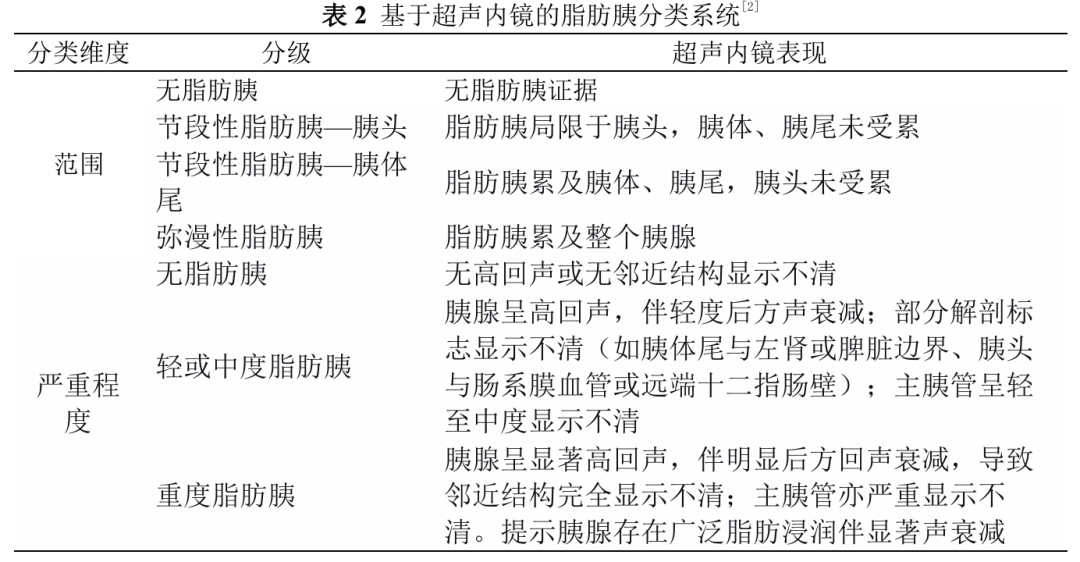
为促进研究的一致性与可比性,共识提出了基于EUS的脂肪胰初步分类系统,从累及范围与严重程度两个维度划分(表2)。为减少主观偏差、提高诊断可靠性,推荐采用标准化定量方法,将目标区域的胰腺回声与脾脏、肾脏等参照器官进行对比,计算平均回声比,以提升检查的可重复性与诊断准确性[10]。此外,人工智能分析EUS图像、剪切波弹性成像等先进技术在脂肪胰评估中展现出良好潜力,但其应用价值尚需大样本临床研究进一步验证。
八、与
脂肪胰可能是AP的危险因素。研究显示,AP患者合并脂肪胰的比例显著高于无AP者[11];脂肪胰与胰腺外分泌疾病、ERCP术后胰腺炎风险升高有关,且与急性胆源性胰腺炎的严重程度呈正相关。合并脂肪胰的AP患者,入院48h内的全身炎症反应评分更高。
九、与胰腺外分泌功能的关系
现有证据表明,并非所有脂肪胰患者都存在胰腺外分泌功能不全,胰腺脂肪含量与消化功能下降之间无明确关联。明确脂肪胰的病因,是理解其与胰腺功能关系的关键。目前二者关联的证据尚不统一,且易受基础胰腺疾病的干扰。
十、与慢性胰腺炎(chronic pancreatitis,CP)的关系
尽管现有证据有限,全基因组关联研究与队列研究提示,脂肪胰与CP风险升高相关。最近一项回顾性配对队列研究显示,平均随访4年,脂肪胰患者的CP发生率为6.1%,显著高于对照组的0.6%[12]。但CP所致胰腺萎缩也可引发脂肪胰,因此存在反向因果偏倚的可能。
脂肪胰与胰腺硬度增加有关,后者是胰腺纤维化的潜在表现,但仅靠胰腺硬度不足以诊断CP。近期一项基于脂肪胰全基因组遗传变异的研究显示,遗传预测的脂肪胰与AP、CP均显著相关[13]。该发现支持脂肪胰在胰腺炎发生中可能存在因果作用,但仍需前瞻性队列研究验证。
十一、与胰腺导管内乳头状黏液瘤(intraductal papillary mucinous neoplasms,IPMN)的关系
低质量证据显示,IPMN患者的脂肪胰患病率为47%~88%,可能高于非IPMN人群,在恶性IPMN、主胰管型IPMN中更为突出。但需注意,脂肪浸润可影响胰腺影像学背景衰减,可能导致囊性病变的检出率增高,从而高估患病率;且现有研究多为回顾性设计,无法明确二者之间的关联是因果关系还是仅为相关性。
在IPMN患者中,伴有恶性或高级别异型增生病变者的胰腺脂肪含量高于低风险IPMN;当IPMN向恶性进展时,胰腺脂肪含量呈上升趋势,而无进展者则保持稳定[14]。该发现与代谢综合征、肥胖升高IPMN进展风险的研究结论一致。尽管脂肪胰可能与IPMN进展风险升高存在关联,但目前尚缺乏充分证据以明确二者之间的因果关系,亦不支持依据脂肪胰情况调整IPMN的随访方案。
十二、与胰腺癌的关系
脂肪胰与胰腺癌存在关联。尽管直接因果关系与具体机制仍在研究中,但越来越多的证据提示,脂肪胰患者的胰腺癌风险升高。但多数研究仅证实二者存在相关性,而非直接因果。一项孟德尔随机化研究以遗传变异为工具变量,最大程度减少混杂因素干扰,进一步支持脂肪胰可能参与胰腺癌发生的假说[15]。其潜在病理生理机制包括脂毒性、慢性炎症、氧化应激、代谢信号改变、自噬失调、免疫紊乱,以及胰腺星状细胞激活继发纤维化等,共同形成促肿瘤发生、进展与转移的微环境。
十三、与手术并发症的关系
脂肪胰会增加手术并发症风险,机制包括:增加组织分离与操作难度、诱发局部炎症、间接升高糖尿病发病风险。胰腺周围或实质内的脂肪浸润会增加手术难度、影响创面愈合,显著升高术后胰瘘等严重并发症发生率[16]。脂肪胰常合并代谢综合征与
十四、儿童人群患病率和临床意义
肥胖、2型糖尿病、MASLD患儿,以及囊性纤维化、Shwachman-Diamond综合征或Pearson综合征等先天性疾病患儿,脂肪胰患病率显著升高。普通儿童人群脂肪胰患病率为4.0%~26.5%,肥胖儿童为18%~50%,肥胖合并MASLD患儿则可达50.0%~74.5%,提示儿童脂肪胰的识别日益重要,尤其在肥胖、MASLD或特定遗传综合征患儿中。
研究证实,脂肪胰与腹部脂肪含量升高相关,是儿童代谢综合征的独立预测因素,还可能升高儿童期2型糖尿病、胰岛素抵抗、β细胞功能障碍及
十五、与MASLD和代谢综合征的关系
脂肪胰可升高MASLD的发病风险,并与患者
十六、与内分泌功能和血糖稳态的关系
脂肪胰可损伤胰腺内分泌功能,导致胰岛素分泌受损,升高糖尿病发病风险。共识汇总分析证实,脂肪胰与β细胞功能受损、胰岛素分泌减少及糖尿病前期显著相关,尤其在亚洲人群、糖尿病家族史阳性者及男性中更为突出,且独立于肝脏脂肪含量与体重。胰腺脂肪含量每增加1/5,糖尿病发病风险升高22%以上[11];而减少胰腺脂肪可改善空腹血糖与胰岛素分泌功能。
十七、治疗与监测
目前尚无针对脂肪胰的特异性治疗方案,治疗核心为针对病因干预。合并代谢综合征的患者,生活方式干预、减重手术及降糖药物均可有效减少胰腺脂肪含量与胰腺总体积。
脂肪胰患者的随访监测需结合基础胰腺疾病与相关代谢危险因素个体化制定。低热量、低脂饮食联合规律运动,以及降糖药物治疗,可显著降低胰腺脂肪含量(降幅2%~42%),有效干预时长至少为6周。胰岛素会促进
此外,脂肪胰与胰腺炎症、胰腺癌及癌前病变也存在显著关联,但目前证据尚不足以将其纳入胰腺癌筛查指征。
综上所述,该共识首次确立“脂肪胰”为描述胰腺内脂肪积聚的统一标准术语,明确了MRI-PDFF、EUS的核心影像学诊断与分级标准,为临床规范化评估与后续研究搭建了关键框架。除术语与诊断外,共识系统梳理了脂肪胰的病因、流行病学、与饮酒吸烟的关系,及其在AP、CP、胰腺外分泌功能不全、手术并发症中的作用;同时阐明了脂肪胰与IPMN、胰腺癌、代谢性疾病(如MASLD、代谢综合征、β细胞功能受损)的内在联系,总结了儿童脂肪胰的患病特点与临床意义。尤为重要的是,共识明确了当前领域的关键证据缺口,尤其是高质量前瞻性临床研究的缺乏,凸显了深入开展研究的迫切性,以期明确脂肪胰的临床意义,建立循证的治疗与监测方案。期待本解读能为我国脂肪胰的临床诊疗与科研工作提供参考,推动该领域的规范化发展。