导 语
本期要点
AML是一种高度异质性疾病,分子遗传学异常与诊断、预后分层及治疗选择密切相关,是精准治疗的核心前提。
优化分子遗传学检测技术以尽早完成患者诊断工作并定制个体化治疗势在必行。
当下检测技术组合策略(如PCR快筛和NGS并行检测IDH突变)或适当延迟治疗启动时间是实现个体化治疗的路径。
尽早启动靶向治疗可显著改善AML患者的生存期,如:对于unfit mIDH1 ND AML患者,IVO+AZA方案中位总生存期(OS)可达29.3个月,IVO+VEN±AZA方案3年OS率达71%。
▲ 点击观看视频
分子检测:AML精准诊疗的核心基石
AML是一种伴随复杂分子遗传学异常的高度异质性恶性血液肿瘤,成人AML患者中存在多种高频突变基因,包括DNMT3A、FLT3-ITD、NPM1、IDH1/2、RUNX1等[1,2],这些分子异常共同构成了AML精准分型的核心依据。
分子遗传学异常与AML的诊断、预后和治疗选择息息相关。ELN 2022风险分层基于遗传学特征,将AML分为预后良好、中等及不良组[3],其中RUNX1::RUNX1T1融合、CBFB::MYH11融合、NPM1突变(无FLT3-ITD)等归为良好预后因素,而TP53突变、复杂核型、KMT2A重排等则为不良预后因素。2024年ELN明确将接受

图1. 2022年版(左)和2024年版(右)ELN指南的风险分层标准
随着靶向治疗的快速发展,与传统化疗相比,靶向药物联合治疗模式显著改善了AML患者的生存结局。回顾性分析国际PETHEMA流行病学数据库17,908例新诊断(ND)AML患者数据显示[5],治疗模式从1990~2006年的“一刀切”统一方案期,到2007~2016年的个体化分层治疗期,再到2017~2024年的靶向治疗期,患者中位OS实现显著提升,从9.3个月增至12.8个月(p<0.001)。多变量分析证实,对年龄、性别、AML类型、ECOG状态、移植和治疗策略进行校正后,诊断时期与OS独立相关(图2)。靶向治疗时代的生存改善则进一步凸显了分子检测指导下精准干预的重要意义,当前ND AML治疗已形成“患者特征评估 + 全面分子分型”的诊疗路径(图3)[6],患者可根据分子检测结果选择针对性治疗方案,实现从“经验治疗”向“精准治疗”的范式转变。
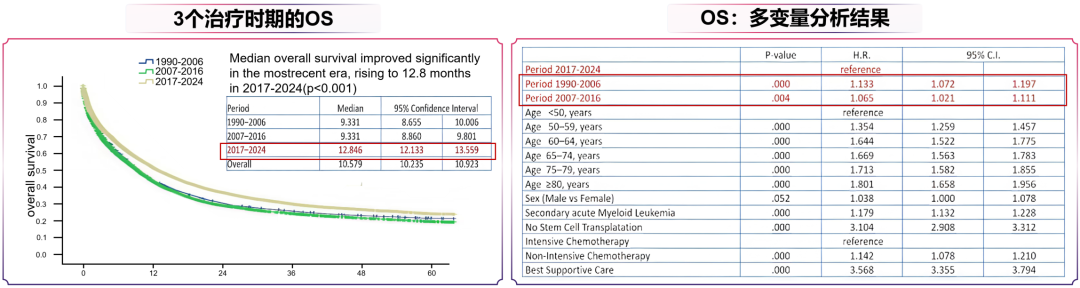
图2. 3个治疗时期的OS(左)和OS多变量分析结果(右)
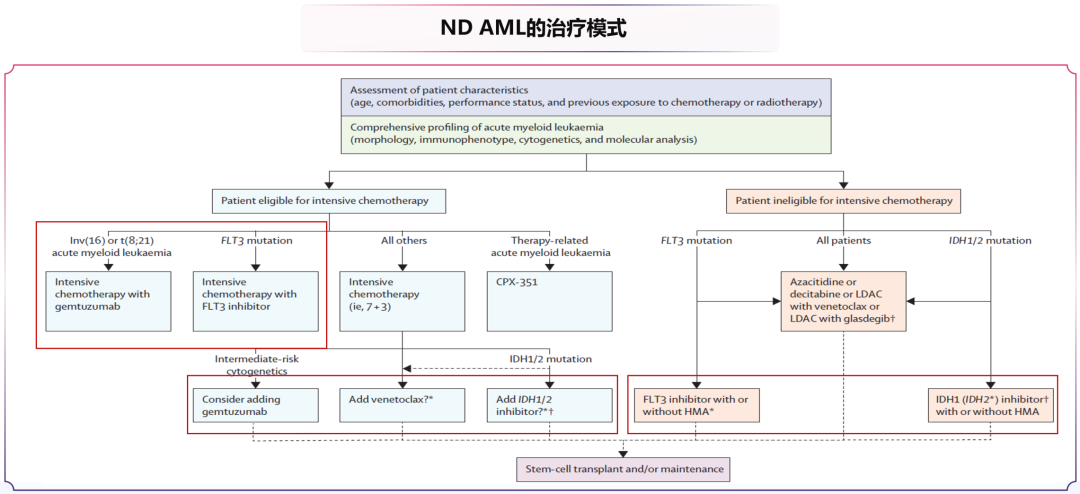
图3. 当前新诊断AML的治疗模式
分子检测现状与优化策略:
破解时效与精准难题
尽管分子检测的重要性已达成共识,但临床应用中仍面临诸多挑战,其中检测结果回报滞后与漏检问题尤为突出,可能影响靶向治疗的及时启动。ELN 2022 AML指南明确推荐,用于确诊和识别可干预治疗靶点的基因突变(如FLT3、IDH1/2、NPM1等)筛查结果,最好在3~5天内回报[3]。然而,实际临床中不同检测技术的周转时间(TAT)存在显著差异。PETHEMA PCR-LMA研究对比NGS与传统PCR检测发现[7],NGS获得结果的中位时间为28~30天,远长于PCR的5~12天,且检测的灵敏度和特异性可能因检测方法的不同而不同(图4),因此存在漏检风险,可能导致部分患者错失最佳治疗时机。
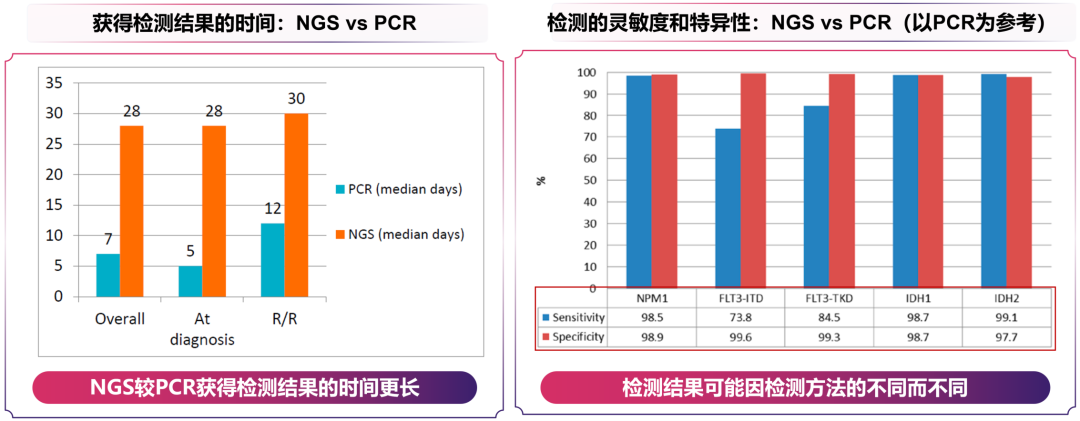
图4. NGS对比PCR获得检测结果的时间(左)以及检测的灵敏度和特异性(右)
为破解上述困境,多项优化策略已在临床实践中探索应用。首先是技术革新,例如美国国家癌症研究所发起的MyeloMATCH项目采用新型检测流程[8],实现95%的患者在样本送达后72小时内(<3天)获得完整的流式、分子学与细胞遗传学结果,98%的患者在120小时内(<5天)完整结果(图5),满足ELN指南对检测时效的要求,为快速启动靶向治疗奠定基础。其次是检测技术组合策略,以IDH1突变(mIDH1)检测为例,采用PCR快筛与NGS检测并行的模式,可缩短报告时间,降低漏检率:PCR操作简单、成本低、周转时间短,能快速识别高频突变;NGS则可覆盖所有突变类型,降低漏检风险[9-15]。
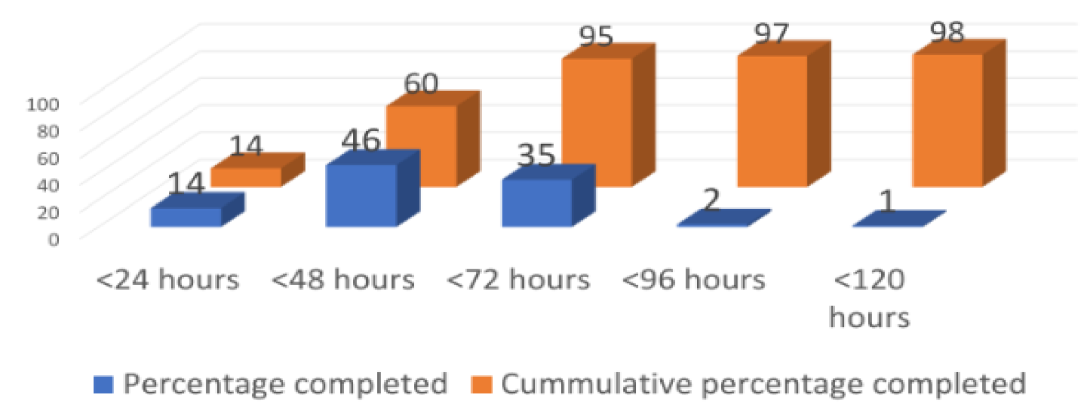
图5. 分子学和细胞遗传学检测结果的TAT
此外,临床实践中合理延迟治疗启动时间也为精准检测提供了缓冲空间。德国白血病研究联盟-急性髓系白血病(SAL-AML)注册中心的大型回顾性真实世界研究纳入2263例Fit ND AML患者[16],发现从诊断至治疗启动时间(TDT)延长至15天以上时,患者的2年OS率与TDT 0~5天组无显著差异(50% vs 51%,p=0.21),且不同年龄亚组结果一致(图6)。另一项针对unfit ND AML患者的回顾性真实世界研究同样证实[17],接受
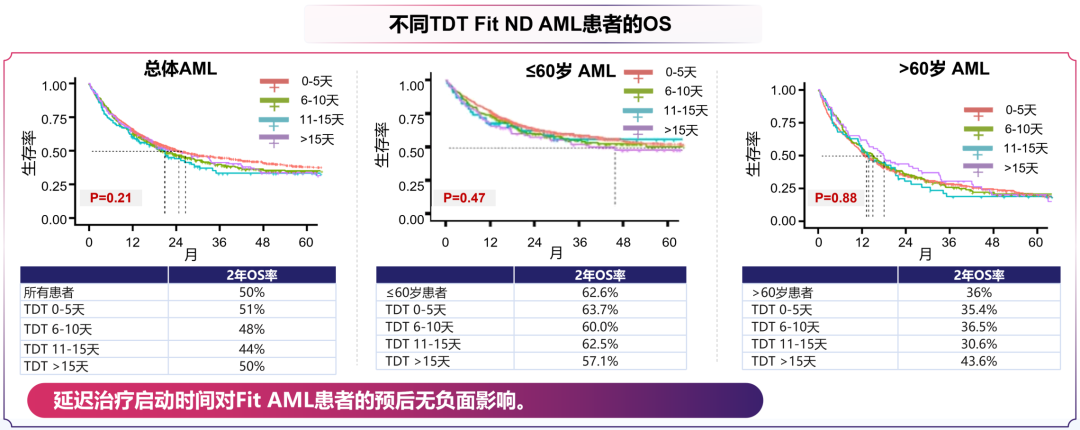
图6. 不同TDT Fit ND AML患者的OS
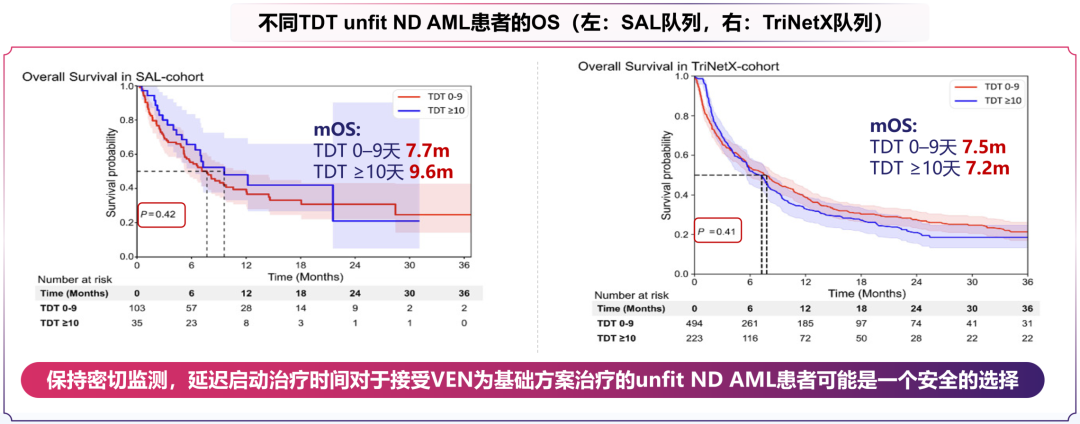
图7. 不同TDT unfit ND AML患者的OS(左:SAL队列,右:TriNetX队列)
分子检测指导下的AML精准治疗:
临床获益显著
在完善的分子检测体系支撑下,AML靶向治疗已取得突破性进展,多款针对特定分子靶点的药物获批上市,涵盖FLT3突变、IDH1突变、IDH2突变、KMT2A重排等多个可干预靶点[19,20],为不同分子亚型患者带来精准治疗选择。临床研究证实,基于分子检测结果选择靶向方案,可显著提升缓解率、延长生存期,且安全性更优,充分体现了精准治疗的核心价值。
VIALE-A研究是一项随机、双盲、安慰剂对照的多中心3期临床试验[21],共入组431例unfit ND AML患者,其中mIDH1亚组和IDH2突变(mIDH2)亚组分别为23例和40例。研究结果显示,中位随访43.2个月,mIDH1亚组和mIDH2亚组中接受维奈克拉联合阿扎胞苷(VEN+AZA)方案治疗的患者,中位OS分别为10.2个月和27.5个月(图8),表明mIDH1 AML患者的预后较mIDH2差,VEN+AZA方案治疗下的OS仍不够理想,亟需探索切实可及的精准靶向治疗方案。
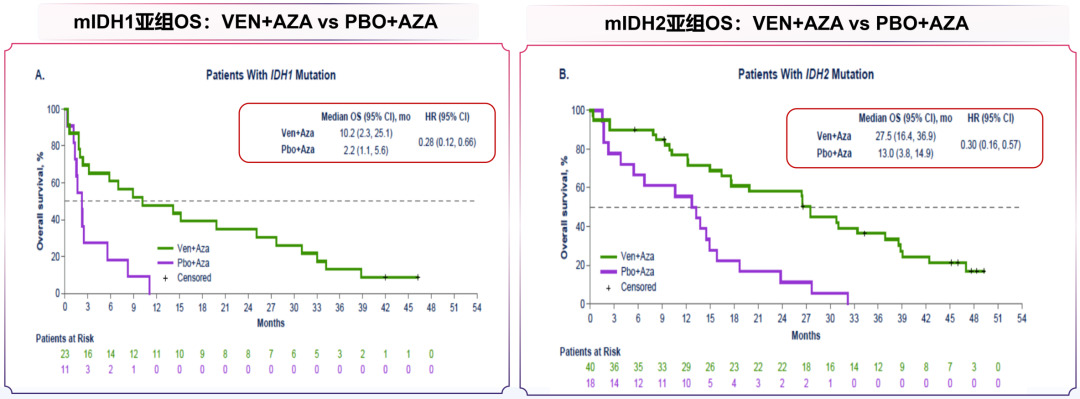
图8. mIDH1亚组(左)和mIDH2亚组(右)的OS
而全球首个且目前国内唯一获批的IDH1抑制剂艾伏尼布的出现,成功填补了mIDH1 AML靶向治疗的空白。AGILE Ⅲ期临床试验证实[22,23],IVO+AZA方案可使unfit mIDH1 ND AML患者的中位OS延长至29.3个月,显著优于安慰剂(PBO)+ AZA组的7.9个月(HR=0.42,p<0.0001);同时该方案安全性优势明显,≥3级
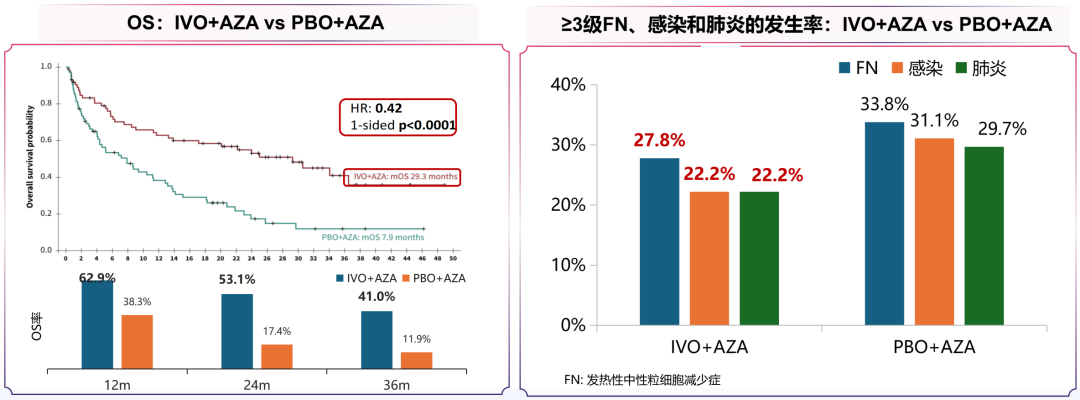
图9. IVO+AZA与对照组的OS和≥3级FN、感染及肺炎的发生率对比
真实世界研究进一步验证了艾伏尼布联合方案的有效性[24],与VEN+去甲基化药物(HMA)方案相比,IVO+HMA方案治疗unfit mIDH1 ND AML的完全缓解率(CR)和复合缓解率(CRc,即CR+CRi/p)更高(42.5% vs 26.3%, p=0.007;63.0% vs 48.5%,p=0.019),6个月无事件生存(EFS)率更优(55.8% vs 38.4%,p=0.015),且治疗前12周非计划就医发生率更低(38.6% vs 70.7%,p<0.001)。
此外,IVO+VEN±AZA三药联合方案在一项多中心Ⅰb/Ⅱ期研究中展现出深度的缓解效果[25],ND AML患者客观缓解率(ORR)达97%,流式MRD阴性率77%,3年OS率71%,为追求深度缓解提供了新方向;另一项Ⅰ/Ⅱ期、开放标签临床研究则证实[26],Olutasidenib(OLU)联合AZA方案治疗mIDH1 ND AML的ORR达76.9%,CR+CRh率53.8%,进一步丰富了治疗选择。
针对FLT3突变(mFLT3)unfit ND AML患者,一项临床Ⅰb期(NCT02203773)和临床3期(VIALE-A研究)事后汇集分析显示[27],与PBO+AZA方案治疗相比,VEN+AZA方案能带来临床获益(CRc率分别为36.4%和66.7%)。而另一项研究表明,奎扎替尼(QUIZ)+VEN +
这些临床数据充分证实,分子检测指导下的靶向治疗能够精准匹配患者分子特征与治疗方案,实现“量体裁衣”的个体化治疗,不仅显著提升了ND AML患者的治疗疗效,还优化了安全性与生活质量,进一步推动AML治疗进入精准获益的新时代。
赵晓甦 教授
参考文献
免责声明:本资料的内容仅作为科学信息参考,仅用于医疗卫生专业人士的学术交流,请勿用于任何其他用途。若您不是医疗卫生专业人士,请勿观看和/或传播此资料。
本资料可能会出现某些药品信息,但该药品/适应症可能尚未获得国家药品监督管理局的注册批准。医疗卫生专业人士做出的任何与治疗有关的决定应根据患者的具体情况并应参照国家药品监督管理局批准的药品说明书。对于本资料可能提到的相关诊断、治疗方法,请遵守国家卫生健康委员会以及相关部门批准使用的指南或规定。
审批编号:M-TIBSO-CN-202603-00024
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)