系统性轻链型(AL)淀粉样变性是一种罕见的
AL的致病核心是异常克隆的浆细胞,CD19和BCMA在这些异常浆细胞中均有表达,是开发相关治疗药物的理想靶点。CAR-T细胞治疗是一种新型精准细胞免疫治疗技术,可以通过改造T细胞表达相应靶点达到清除致病细胞的目的。对AL淀粉样变性这类疾病是理想的治疗方式。
2026年4月2日,东部战区总医院国家肾脏疾病临床医学研究中心
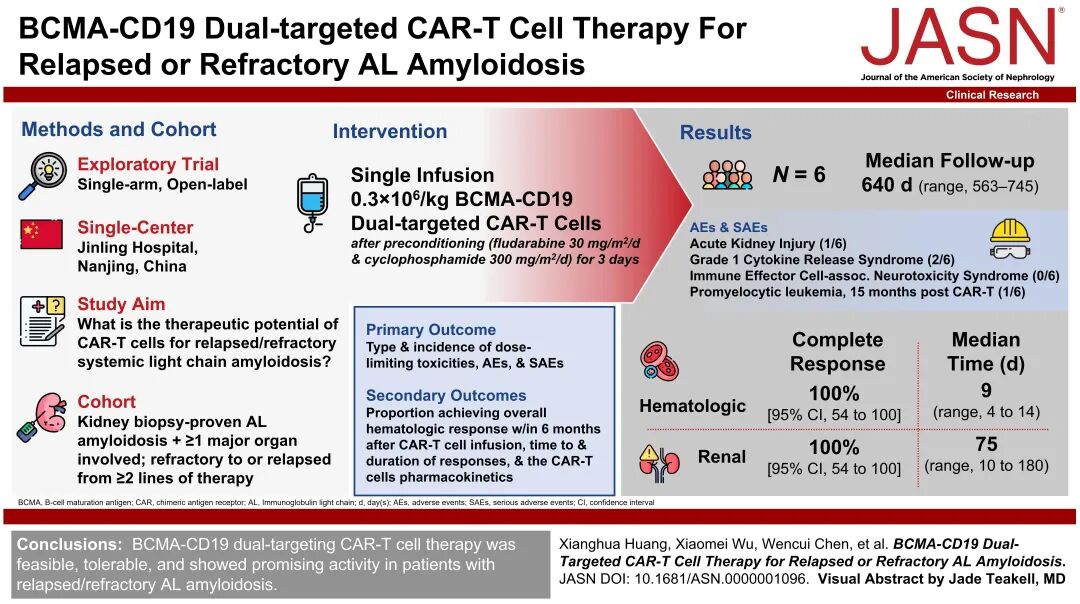
图1. Journal of the American Society of Nephrology文章摘要图
研究团队创新的设计了同时表达BCMA和CD19的CAR-T细胞,其目的在于同时清除表达BCMA或CD19的浆细胞和B细胞。这种创新设计的CAR-T细胞不但可清除产生异常轻链的浆细胞,对浆细胞的前体细胞也同时予以清除,可诱导更深的血液学缓解,并为后续免疫重置创造条件。研究纳入了6例复发/难治性AL淀粉样变性患者。主要入组标准为两线治疗失败,且均伴有主要器官受累的复发/难治性AL淀粉样变性患者。6例患者均有肾脏受累,其中1例患者合并心脏受累。患者在清淋预处理后接受剂量为0.3×10E6/公斤体重的BCMA-CD19双靶点CAR-T细胞治疗。
血液学反应评估显示6名患者均实现血液学完全缓解(100%)。首次出现血液学反应的中位时间为9天(范围4~14天)。最佳血液学反应出现中位时间为14天(10~60天),且所有患者均达到微小残留病变阴性。所有6例肾脏受累患者均达到肾脏反应。患者首次出现肾脏缓解的中位时间为75天(10~180天)。出现最佳肾脏反应的中位时间为180天(60~450天)。1例心脏受累的患者也在治疗后第28天实现了心脏部分缓解,并在CAR-T治疗后6个月评估时维持心脏缓解(图2,图3)。
患者中位随访时间为640天(563~745天),所有患者均存活。5例患者在随访期间维持血液学完全缓解。1例患者在治疗后6个月时出现血液学复发,在接受
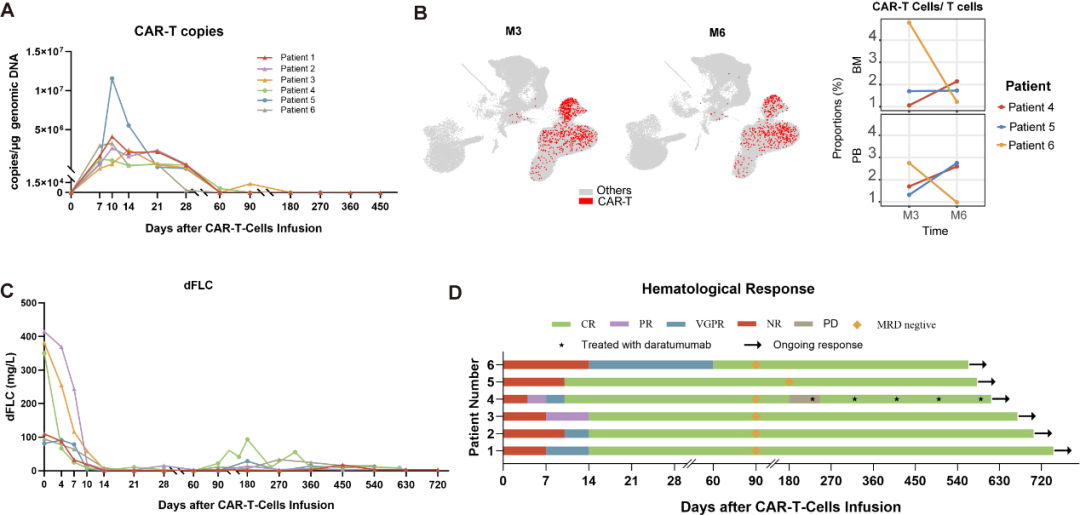
图2. BCMA-CD19双靶点CAR-T细胞治疗后CAR-T细胞动力学和血液学反应
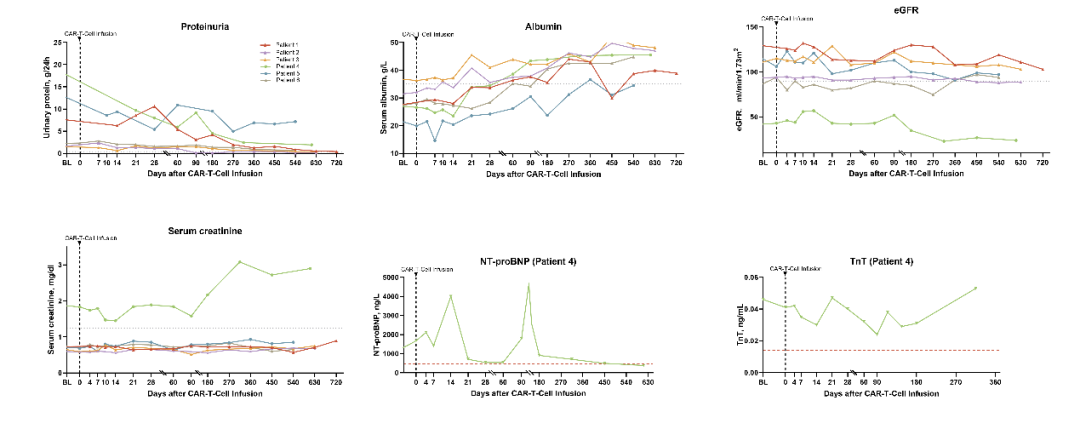
图3. BCMA-CD19双靶点CAR-T细胞治疗后的器官反应
随访期间,未观察到剂量限制性毒性。6例患者中2例(33.3%)出现1级细胞因子释放综合征,未出现免疫效应细胞相关神经毒性综合征。CAR-T治疗中最常见的不良事件为血液毒性和感染。研究共报告了5例SAEs。2例患者分别在CAR-T治疗后3周及5个月因
在临床验证BCMA-CD19双靶点CAR-T治疗的疗效及安全性之外,研究还通过单细胞测序技术解析CAR-T治疗在免疫重建方面的独特优势。该疗法不仅实现了对克隆性浆细胞的深度清除,还有效清除了异常的B细胞和CD19阳性的干细胞样浆细胞,这些细胞是疾病复发的重要隐患。研究团队发现患者的记忆B细胞已存在显著异常,表现为蛋白酶体介导的泛素依赖性蛋白分解代谢过程等通路上调。这些异常在CAR-T细胞输注后得到逆转,同时新产生的浆细胞内质网应激相关通路也明显下调。此外,CAR-T细胞输注后外周血中整体CD8+ T细胞及CD4+、CD8+效应T细胞均显著扩增,骨髓和外周血细胞毒性评分明显升高,提示CAR-T细胞治疗诱导机体产生抗克隆性浆细胞的免疫监视(图4)。
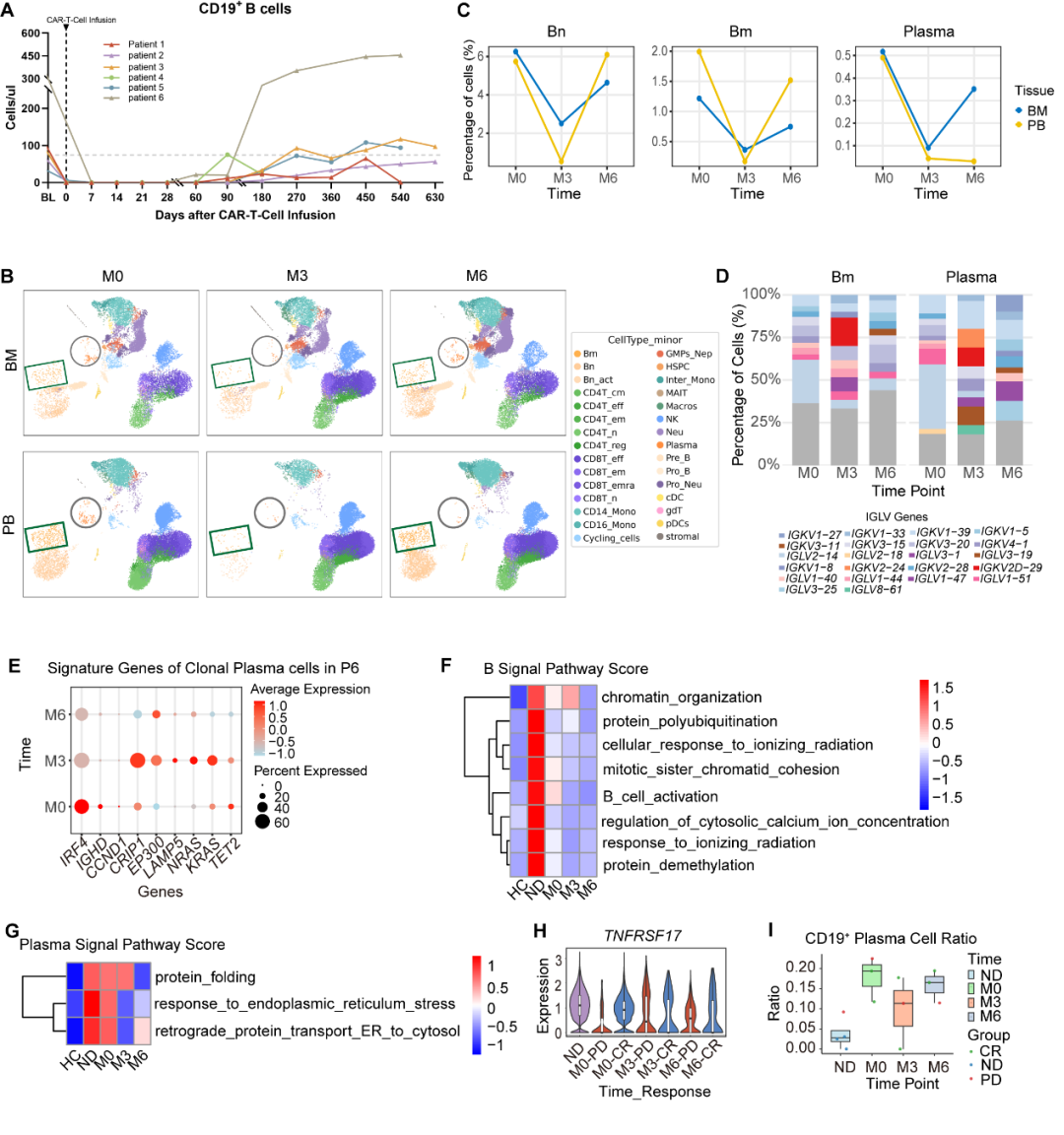
图4. CAR-T细胞治疗后外周血及骨髓单核细胞的免疫特征
重塑复发/难治性AL淀粉样变性患者的治疗格局。研究为BCMA-CD19双靶点CAR-T细胞疗法在复发/难治性AL淀粉样变性患者中的安全性和有效性提供了证据。研究发现,BCMA-CD19双靶点CAR-T细胞可产生快速且深度的血液学及器官反应,患者耐受性良好。该研究表明BCMA-CD19双靶点CAR-T细胞可能是复发/难治性AL淀粉样变性的潜在治疗选择,研究也为后续开展更大规模的临床研究提供了理论基础。
东部战区总医院国家肾脏疾病临床医学研究中心刘志红院士及
内容来源为东部战区总医院订阅号,本文经刘志红院士团队授权发布。
医脉通是专业的在线医生平台,“感知世界医学