突破微生态治疗精准化的临床瓶颈——南方医科大学深圳医院/珠江医院/天津医科大学联合团队提出“加减法”实现
Advance Microbiota Transplantation: A Novel Addition–Subtraction Paradigm for Optimising Faecal Microbiota Transplantation
Microbial Biotechnology
PMID: 41804658 [IF=5.2]
来源:IBD Daily
粪菌移植 (faecal microbiota transplantation,FMT) 近年来已从复发性
研究采用系统性综述与证据综合方法检索2016年1月至2025年7月在PubMed、Embase和Cochrane Library数据库中的FMT临床研究证据,应用PRIM对纳入文献的报告质量进行全面评估。同时,通过“证据映射”将现有FMT临床试验的干预措施系统归类至AMT框架的不同阶段,分析其作为“加法”或“减法”策略对优化FMT疗效的支持价值。
一、AMT概念的提出及其理论框架
AMT的核心在于将FMT重新定义为跨越移植前、移植中和移植后多阶段的系统性治疗过程,并以“加法”与“减法”作为基本干预逻辑 (图1)。“加法”即针对供体、制剂、受体及移植后环境补充利于疗效提升的因素,如饮食干预优化供体菌群、富集功能菌群、设计合理的移植频次与维持方案,以及移植后联合饮食、药物和生活方式管理增强菌群定植与功能表达;“减法”则强调去除影响疗效和安全性的因素,如降低潜在风险成分、减弱受体生态阻力、减少无效或冗余干预。作者特别指出,AMT是对FMT治疗逻辑的系统重构,目前仍是基于循证研究提出的阶段性假说框架,尚未完成临床验证。其核心价值在于推动 FMT 从经验性操作走向契合精准医学原则的微生态治疗。
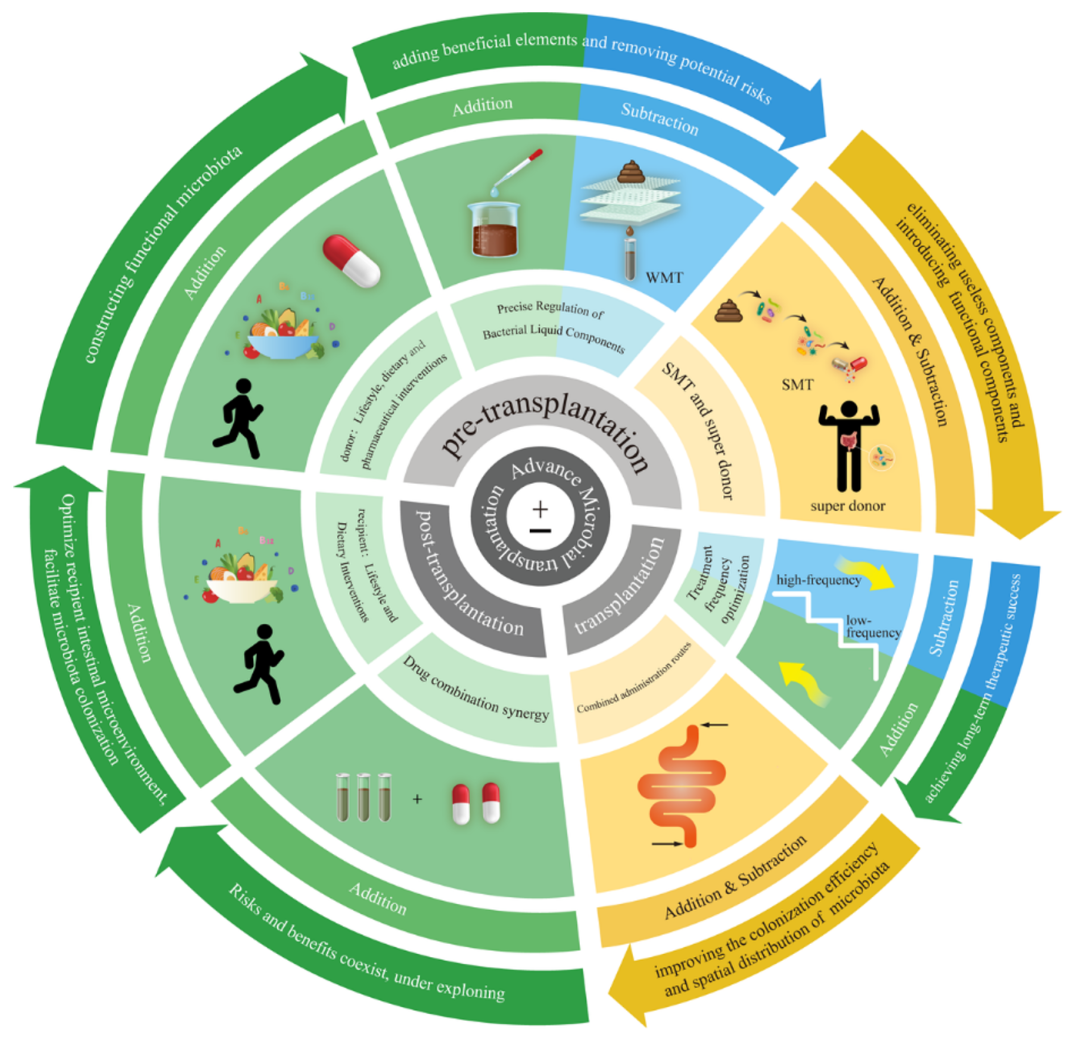
图1. AMT概念图
二、基于PRIM框架的FMT临床研究质量评估
除提出AMT概念外,该综述的另一重要内容是首次基于PRIM完成全球 FMT临床研究报告质量的系统评估。结果显示,FMT研究数量逐年增长,研究类型从病例报告向临床试验逐步转型,标志着领域从经验积累迈入循证研究阶段。质量评价方面,63.5%的研究达到高质量阈值,13.5%为低质量研究,且临床试验的PRIM评分显著高于病例报告。研究同时识别出6类研究报告的关键环节:供体筛选方法、生产制备方法、产品分类、辅料或附属材料、患者准备以及影响结局的伴随治疗 (图2) 。此类信息缺失直接影响FMT研究的可解释性、可比性及可重复性,也反映出当前FMT研究重疗效、轻方法学透明度与流程标准化的问题。
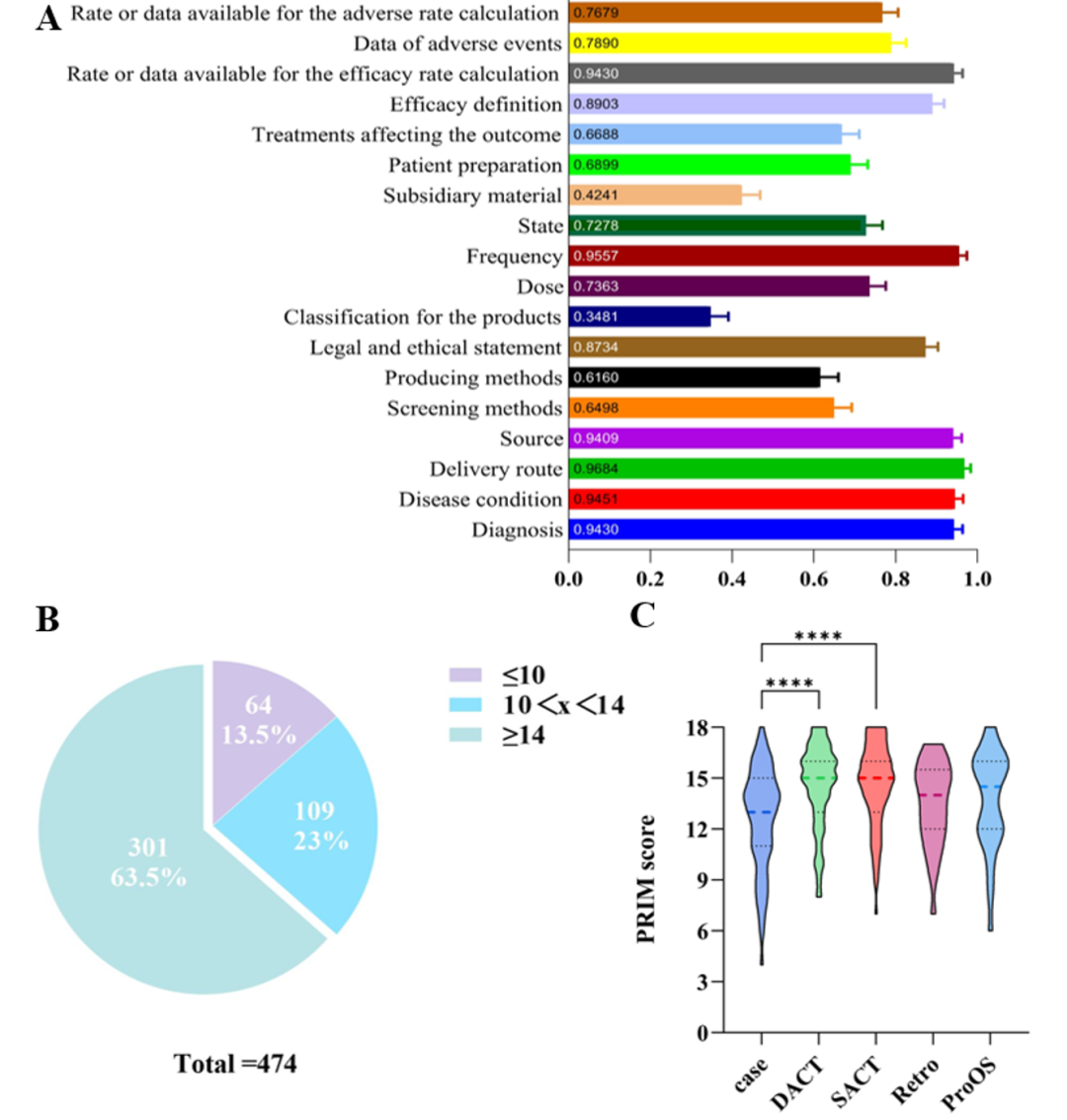
图2. 基于PRIM框架的FMT临床研究质量评估:A. PRIM中每个条目的平均分;B. PRIM总分的分布饼图;C. 不同研究类型的 PRIM 分数比较
三、移植前阶段的优化策略:供体、制剂与受体的系统重塑
1. 供体侧优化:从“健康供体”走向“功能供体”
综述指出供体菌群并非静态原始材料,其稳定性、功能性和定植潜力会受到饮食、生活方式及昼夜节律等多种因素影响。因此供体管理需遵循节律稳定、结构完整、功能相容原则,通过针对性“加减法”实现功能导向优化。一方面可通过饮食等方式增强供体有益功能菌群及其代谢潜力,另一方面应尽量减少不利饮食和促炎代谢通路带来的干扰。综述同时指出,供体优化真正关键的是供体菌群功能是否与目标疾病的治疗需求相匹配。基于此,FMT供体筛选应由传统“健康供体”向“功能供体”乃至“超级供体”升级。超级供体的优势源于整体菌群生态结构的协同效应。而混合供体策略并非绝对有效,供体群落间的竞争可能影响关键菌群的定植与协同效应,需谨慎应用。
2. 制剂层面的优化:从粗放移植走向精细化制备
在制剂层面,AMT将“加法”与“减法”进一步具体化:前者包括富集特定功能菌群、保护关键厌氧菌活性,后者则强调去除病原体、毒素及其他可能削弱疗效或增加风险的成分。综述重点讨论了WMT (洗涤菌群移植) 、厌氧制备、纯化孢子制剂等策略,并将合成菌群移植、定义化菌群组合和工程化活体生物治疗产品纳入AMT的发展谱系,提示FMT正由粗放移植走向可设计、可控制的微生态治疗疗法。
3. 受体预处理:降低生态阻力,提升定植基础
受体原有菌群和肠道微环境本身就可能构成强烈的生态阻力,因此移植前预处理是提升供体菌群定植和功能表达的重要环节。加法方面,某些药物预处理可能与FMT形成协同效应,但受疾病背景、药物类型、个体差异影响较大,无统一有效方案;减法方面,抗生素预处理和肠道清洁是降低生态竞争、为供体菌群创造生态位的重要策略,已获多项研究和共识文件支持。受体预处理的核心是识别能真正减少生态阻力、提升定植条件的干预,而非单纯增加操作。
表1. FMT中加减策略的证据图谱 (移植前)
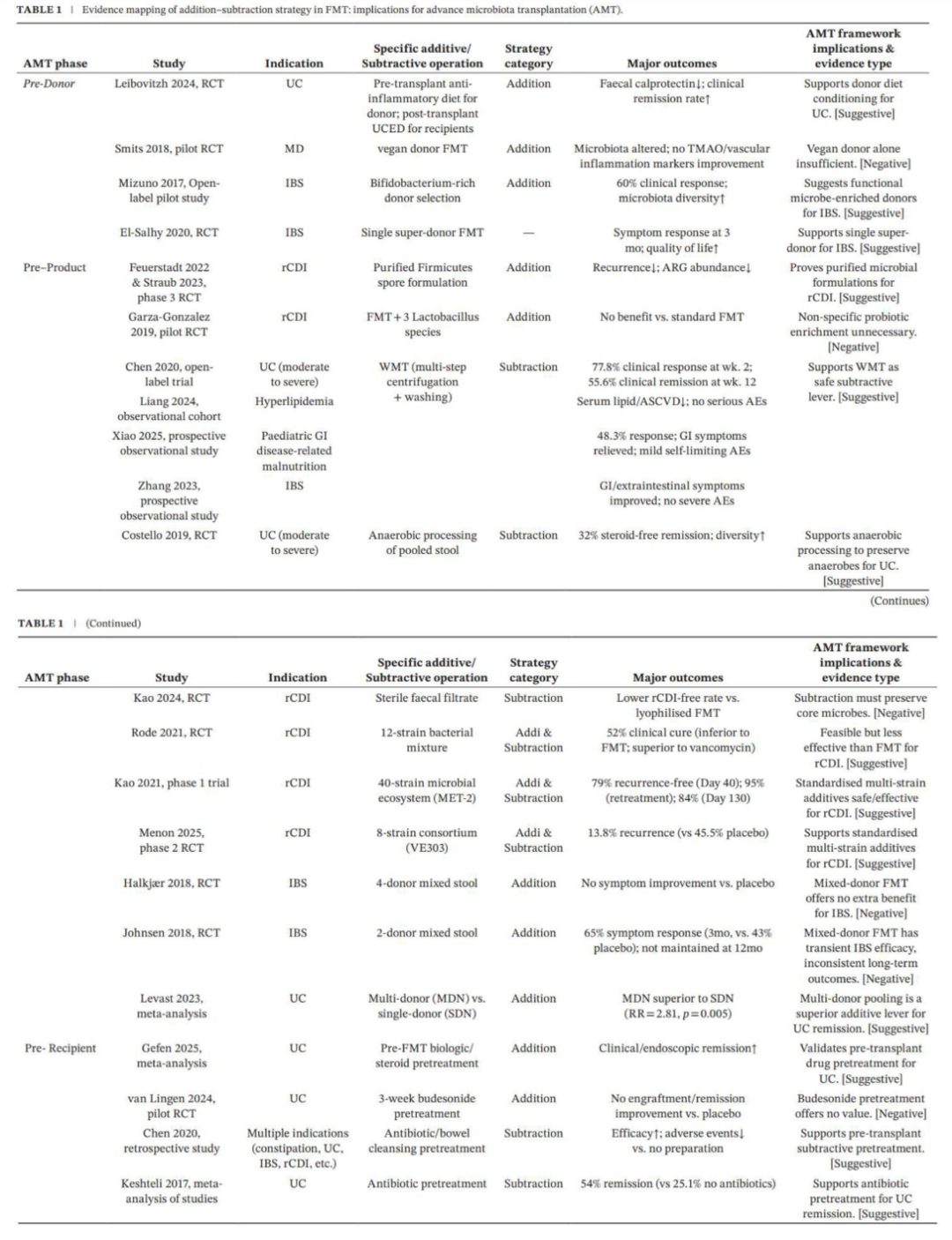
四、移植实施阶段的优化策略:频次、剂量与路径的个体化设计
1. 频次与维持策略:从单次治疗走向阶段化干预
综述表明移植频次的设计需结合疾病特征:rCDI等疾病经单次或少量FMT即可取得高疗效;但炎症性肠病、
2. 给药路径与解剖靶向:从技术参数到治疗设计
给药路径是影响FMT疗效的重要变量,单一路径易受胃酸降解、肠道清除速度、病灶空间分布等限制,而多路径联合给药可扩大肠道覆盖范围、延长菌群与肠黏膜接触时间、提升定植效率。尤其在炎症性肠病治疗中给药路径更需要结合病灶的解剖分布进行个体化设计。在AMT框架下,给药路径不再是单纯的操作技术细节,而是纳入疾病分层和个体化治疗设计的核心组成部分。
表2. FMT中加减策略的证据图谱 (移植中)
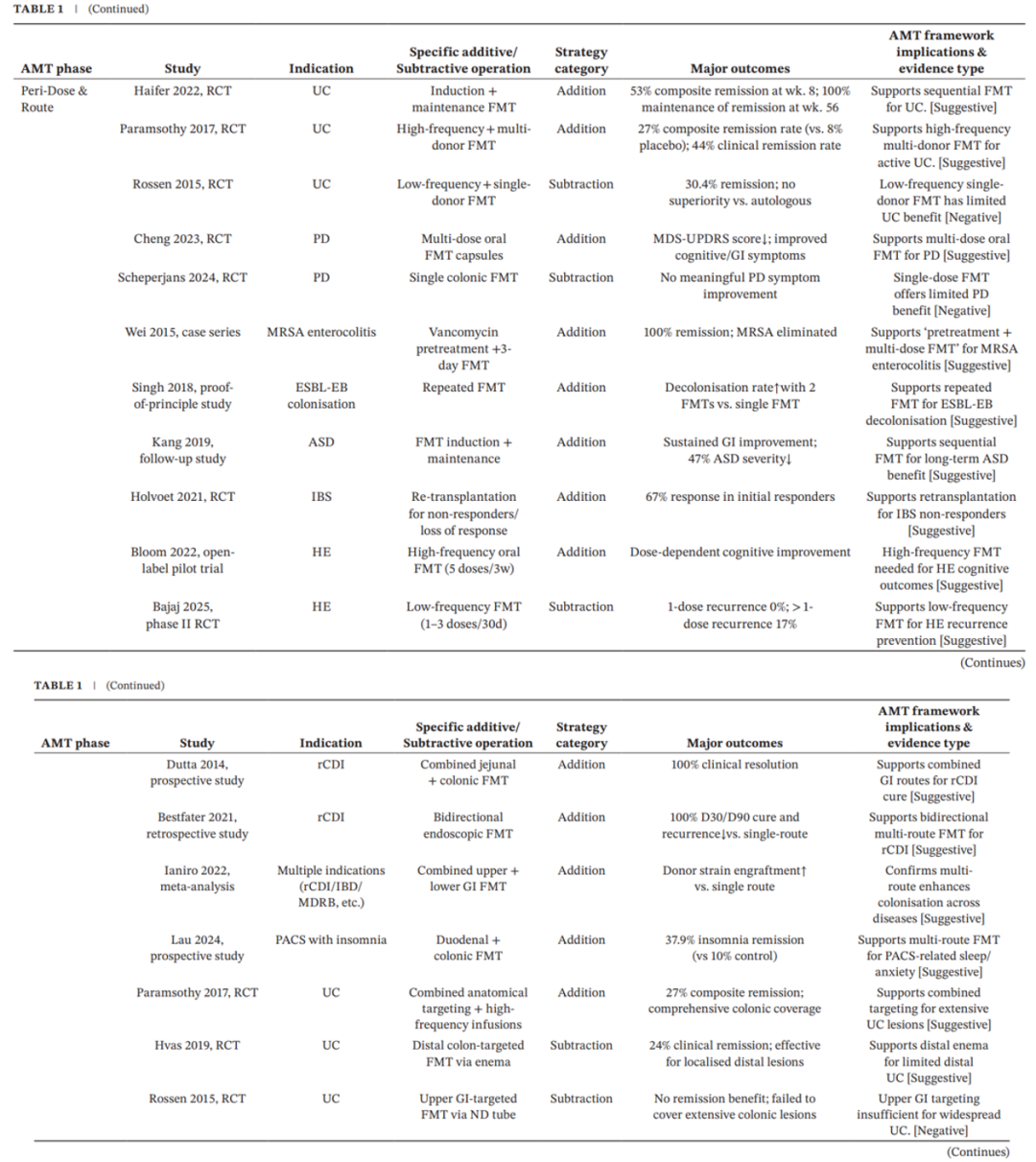
五、移植后阶段的优化策略:药物、饮食与生活方式的协同管理
1. 药物协同的适用边界
AMT特别强调移植后阶段的持续管理。综述指出,许多传统FMT研究关注“移植操作本身”,却相对忽视移植后微环境对菌群定植与长期疗效的决定性影响。药物协同方面,综述并未笼统主张“联合越多越好”,而是通过正反两方面证据提示其效果具有明显的情境依赖性。因此,AMT中的“加法”并非简单的治疗叠加,要求每一种联合干预都具备明确的协同机制、充分的循证依据和合理的风险—获益比。
2. 饮食与生活方式干预:构建有利于定植的宿主环境
在AMT移植后管理中,饮食和生活方式是维持菌群稳定定植的重要组成部分。综述提出,移植后饮食的本质在于“喂养”已移植的功能菌群,为其持续发挥作用提供合适的生态位。此外,作者还进一步讨论了不同类型饮食在不同疾病背景中的价值可能不同,提示移植后饮食管理需精细化、场景化、个体化,摒弃笼统的 “健康饮食建议”。
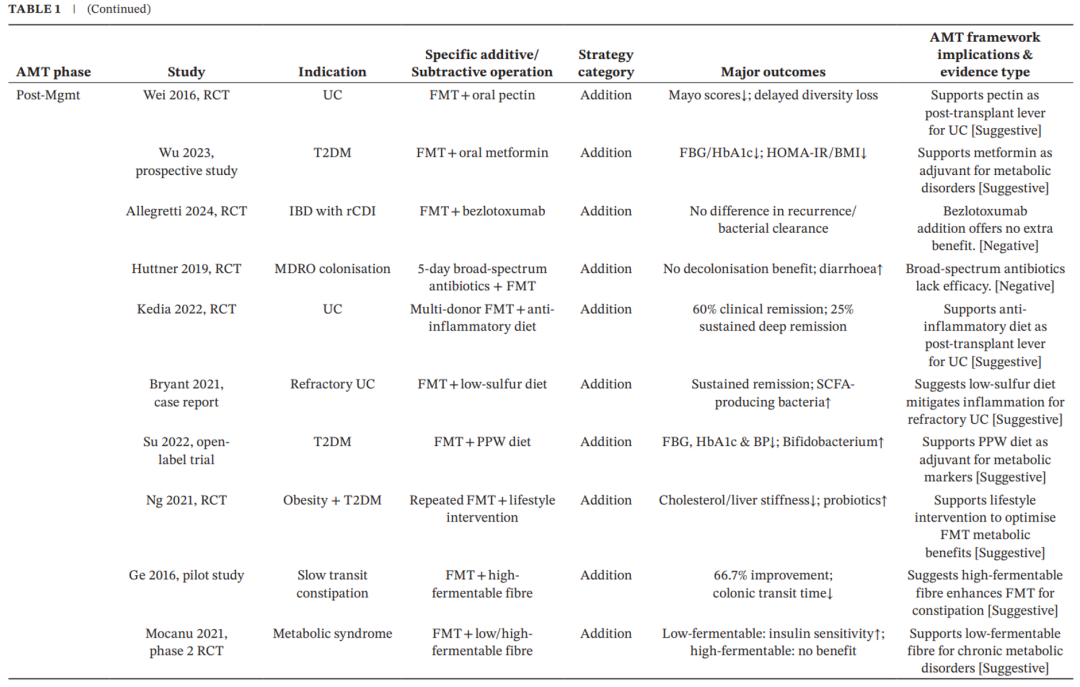
表3. FMT中加减策略的证据图谱 (移植后)
六、从机制合理性到转化研究设计:AMT的临床转化意义
在系统梳理前、中、后各阶段优化路径后,文章进一步讨论了AMT如何走向临床转化。综述指出:已有基础研究为AMT“分阶段加减法”提供机制合理性支持,并提出了一个面向
七、总结与展望
综述的核心要旨并非提出适用于所有疾病的统一的FMT方案,而是构建了一套重新组织FMT研究与临床实践的理论框架。该框架以“加减法”为核心逻辑,将供体优化、制剂精细化、受体预处理、移植频次与路径设计、以及移植后微环境管理整合为连续的治疗体系,推动FMT从传统经验性操作逐步走向基于生态学和机制学原则的精准干预。同时,基于PRIM的评估也明确了FMT领域当前的现实问题:报告内容不充分、标准不统一、证据异质性较高。未来AMT的发展既需要持续优化治疗策略,也需要推进标准化制备、规范化报告及更高质量临床研究。