来源:IBD Daliy
引言
炎症性肠病 (IBD) 与肠易激综合征 (IBS) 在临床上被视为两种特征不同的疾病。IBD的诊断需综合患者病史、查体、血粪检测,并结合内镜与组织学证实肠道炎症。相比之下,IBS作为一种肠脑互作障碍疾病,其肠道无肉眼可见的炎症,在排除报警征象与其他胃肠道疾病后,进行症状学诊断 (罗马IV标准)。
鉴于IBS的确诊需预先排除其他器质性疾病,已确诊IBD的患者通常不再叠加IBS诊断。然而,大量临床观察显示,即使在达到组织学缓解的IBD患者中,仍有约四分之一的人持续报告腹痛、排便异常等非炎症性症状。这些表现与IBS的临床特征相似,被称为IBD中的IBS样症状。
控制肠道炎症是每一位IBD专科医生的基本工作,但面对这些在炎症消退后的IBS样症状,现有的临床干预手段和治疗标准仍不成熟。在该综述中,作者详细梳理了IBD患者合并IBS样症状的流行病学特征与自然病史,并深入剖析了潜在的病理生理学基础,同时提出了一套针对此类患者的诊断与治疗路径。
非炎症性症状的流行病学与临床负担
活动性炎症是IBD患者出现胃肠道症状的首要原因。传统观念将缓解期患者的IBS样症状归咎于内镜下难以察觉的隐性炎症。然而,随着组织学评估的普及,近期的流行病学数据揭示了不同的临床现状:一项纳入3169名缓解期IBD患者的大型荟萃分析显示,IBS样症状的总体患病率达32.5%;更为关键的是,即使在经证实达到组织学缓解的患者中,该患病率仍高达25.8%;且
病理生理学基础
1. 是隐性炎症还是真正的功能异常?
关于IBD缓解期持续存在非炎症性症状的原因,隐性炎症与合并/既往存在IBS是长期以来最具争议的两种假说。然而,这两种传统观点均受到临床证据的挑战。一方面,尽管部分内镜下缓解患者的肠黏膜内存在轻度免疫激活,但在无炎症因子升高的深度缓解 (内镜和组织学均缓解) 患者中仍有27%存在排便异常,提示低度炎症与IBS症状的发病机制有关,同时可能存在炎症以外的机制。这种机制错位 (潜在的低级别炎症通路与典型IBD不同/其他可能机制) 解释了为何常规抗炎药及强效生物制剂对这些残余症状效果不佳,可能需要优先考虑特定的免疫调节疗法 (例如,肥大细胞稳定剂疗法)。此外,纵向队列研究表明IBS样症状与IBD复发、激素需求或治疗升级等风险均无显著关联,这共同提示“隐性”炎症未必需要干预,因其并不影响疾病的自然演变史。另一方面,普通人群5%~10%的IBS患病率远低于IBD人群中高达27.4%~37.9%的受累比例,驳斥了既往存在IBS的可能。
因此需要考虑其他因素,如在两者共享的病理生理学基础以及在脑肠互动的系统性紊乱中寻找答案。
2. 异病同源?
尽管临床界限相对明确,IBD与IBS在病理生理学层面有相似的特征,二者的发病均涉及遗传易感性、环境因素及肠道微生态失衡。在遗传层面,不仅IBD的遗传机制广受认可,特定基因 (如SCN5A) 在IBS中的致病作用也正被逐步揭示;一项西班牙家系研究发现,IBD患者的一级血亲罹患IBS的风险显著升高,而其配偶未见此种关联,这种独立于共同生活环境的家族聚集性,提示了两者间存在共享的易感基因。在环境层面,空气污染与特定饮食模式被认为是二者共同的诱发因素。尤为引人瞩目的是,基于英国生物样本库的大数据分析显示超加工食品对这两种疾病的共同驱动作用。
关于IBD合并IBS样症状患者肠道菌群的横断面研究目前尚无一致结论,且未能阐明微生物群导致胃肠道症状发展的机制。感染后IBS (postinfection IBS,PI-IBS) 的病理模型为揭示这些非炎症性症状的来源提供了机制参考。研究表明,PI-IBS患者局部微环境中蛋白水解活性升高,而该活性通过肠道微生物的β-
3. 肠-脑相互作用
在肠道局部微环境改变之外,系统性的肠-脑互动紊乱在非炎症性症状的演变中扮演着关键角色 (图1)。对于IBS,通过全基因组关联分析研究,已发现其与情绪和
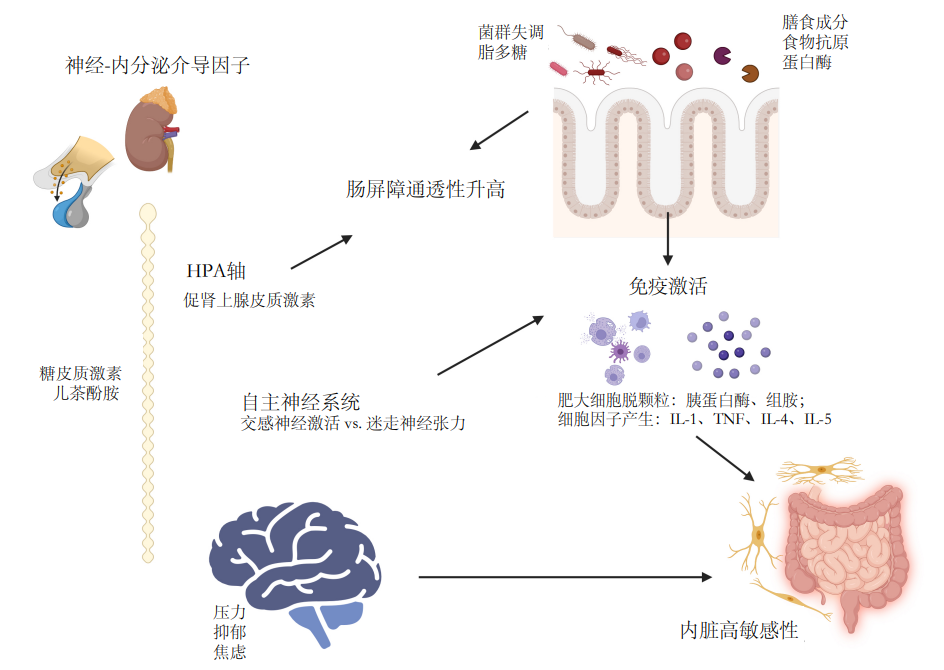
图1 具有IBS样症状的IBD患者脑-肠相互作用的双向性
临床诊断和治疗
即使在内镜与组织学证实炎症已经愈合的前提下,临床医生也不能贸然将患者的腹胀、腹痛或排便异常直接归结为功能性疾病。在确立IBS样症状的诊断前,必须精准排查具有特定治疗方案的隐匿性器质性病因,例如:有回盲部切除史的患者需高度警惕胆汁酸
鉴于目前缺乏针对IBD合并IBS样症状治疗的循证证据,临床多采用经典的IBS疗法,包括解痉药、止泻药、纤维补充剂和三环类抗抑郁药。
研究者建议一种以症状为导向的整合诊疗策略:在完善检查并确认为炎症缓解期后,临床医生应以主诉症状为导向,针对患者的感觉症状 (如疼痛、腹胀或直肠排空不全感) 或动力相关症状 (如腹泻或
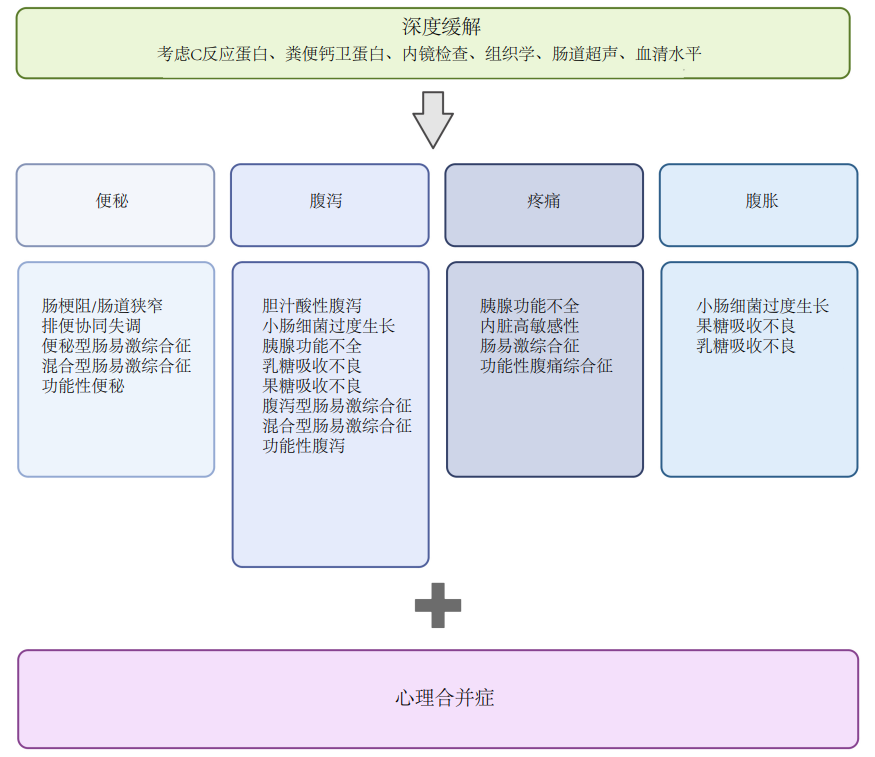
图2 针对缓解期患者持续症状的诊断和管理
饮食与生活方式调整是IBS的一线干预手段;相比之下,对于IBD,大多数补充与替代疗法(含运动、瑜伽及大麻等草药) 主要改善的是生活质量而非直接缓解疾病症状,目前仅有姜黄素对控制UC症状显示出初步但证据质量较低的益处。因此,针对炎症已受控但仍有类似IBS症状的IBD患者,建议也可以考虑采用针对IBS的心理与行为辅助疗法进行管理。
基于肠道微生物组的疗法由于现有证据等级较低,目前除
地中海饮食是IBD的普遍推荐方案 (伴肠狭窄者需注意纤维摄入);而低FODMAP饮食(FODMAPs是指难消化吸收的短链碳水化合物,可能会触发一些IBS患者的症状) 则是IBS最有效且循证最充分的饮食疗法。实施低FODMAP饮食必须严格经历4-6周的限制期、随后的重新引入期以及最终的个性化拓宽期,这既能明确诱发症状的具体糖类,又能避免长期严格限制导致的
经典的IBS药物 (如解痉药、止泻药和泻药) 也可尝试用于IBD的肠道运动障碍;但需注意,止泻药和泻药可能会加重难以管理的腹痛与腹胀。相比之下,薄荷油、H1受体阻滞剂 (如
神经调节剂 (如抗抑郁药) 通过靶向脑-肠轴和降低内脏高敏感性,是改善肠道动力异常和腹痛的有效辅助手段,即使患者没有心理合并症也同样适用。
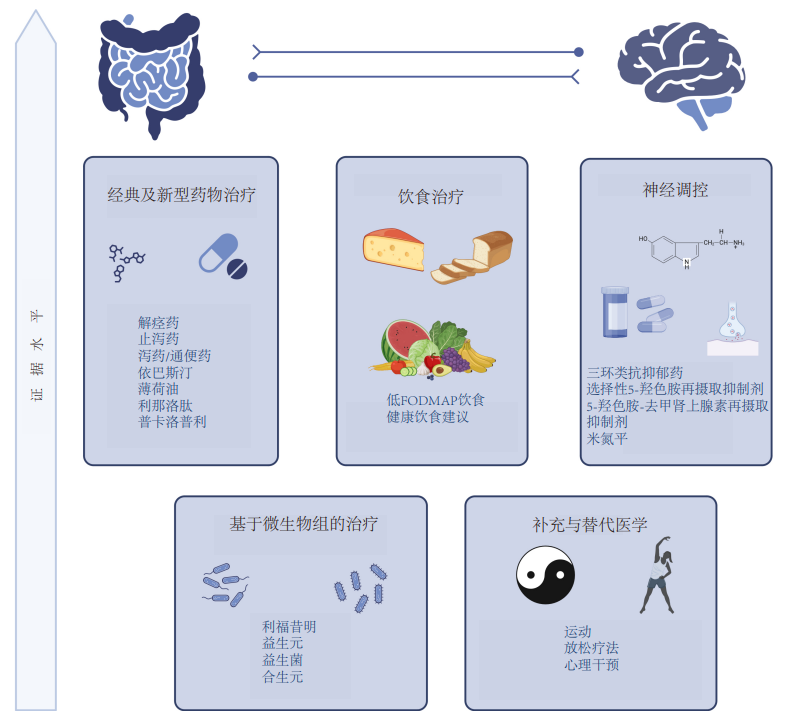
图3 当前用于治疗IBD中IBS样症状的治疗方案
治疗目标
尽管IBS和IBD均为终身性疾病,但其治疗理念已发生显著转变:STRIDE-II指南所强调的,恢复生活质量和无残疾状态已与内镜愈合并列为IBD的长期治疗目标,这意味着真正的愈合超越单一的抗炎治疗,涵盖情绪健康、疼痛管理与疲劳改善等更广泛的维度。鉴于IBS的治疗核心同样在于缓解症状、提升生活质量及降低不必要的医疗负担,临床上在管理伴有IBS样症状的IBD患者时,理应将两者的目标相融合。为了在控制生理炎症与提升整体身心状态之间取得平衡,须打破单一治疗的局限,通过与患者深入沟通,并在多学科团队的协作下,将饮食调整和肠道定向
总结
首先治疗炎症是改善IBD患者长期预后的核心基石,但至少四分之一的患者仍会受IBS样非炎症性症状的困扰,临床医生的目标应随之拓宽。在精准评估炎症负荷之外,IBD患者的非炎性症状同样需要重视和积极管理。最终,我们不仅要致力于消除病理炎症,更要秉持综合、整体的康复理念,采取以患者核心主诉为导向的积极策略,全面关怀患者的综合福祉与生活质量。