骨松“3+9”序贯方案:
前3个月,利用罗莫索珠单抗黄金窗口期“强力建骨”(每月1次);
后9个月,序贯
在现有的治疗武器库中,2025年12月于我国获批上市的骨松治疗新药罗莫索珠单抗注射液(Romosozumab,简称Romo;每月1次,持续12个月)凭借其独特的抑制骨硬化蛋白(Sclerostin)机制,展现出了明确的“促成骨+抑破骨”双重调节作用,相比传统药物能够更显著地提升骨密度(BMD)。

然而,由于种种原因,其在现实世界中的停药率较高——美国患者一年内停药率甚至超过50%。如何能既“借用”Romo强大的早期促成骨优势,又规避其长期使用的弊端?近期,哈佛大学医学院团队在《柳叶刀·
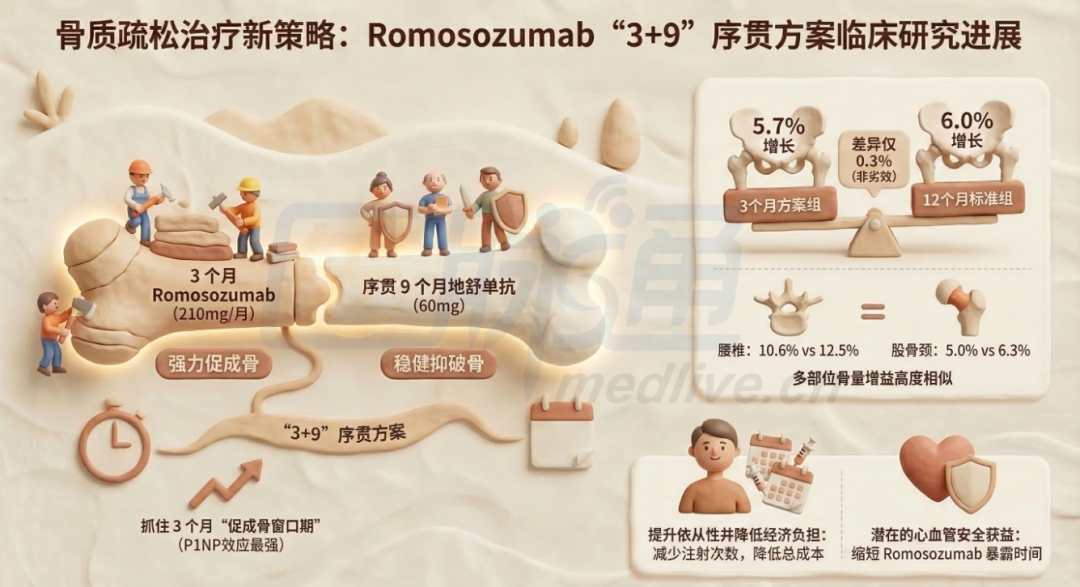
Romo的药理动力学具有极其鲜明的“时效特征”。研究证实,其促骨形成效应(如骨形成标志物P1NP)在给药后几天内即可迅速达峰,这一“早期快速骨建模(Modeling-based bone formation)”阶段是骨密度(BMD)快速拉升的黄金期。然而,这种促成骨作用是短暂的,在2-3个月后便会逐渐回落至基线水平,随后主要转为持续的抗骨吸收作用。
此外,受限于按月就诊注射的便利性要求、卫生经济学考量,以及需关注的潜在心血管安全性评估(说明书黑框警告),美国真实世界数据显示,该药的一年内停药率超过50%。
基于这一机制特征与临床管理痛点,美国麻省总医院(哈佛大学医学院附属)的Benjamin Z Leder教授团队提出假设:如果仅利用前3个月的Romo进行“早期强效促成骨”,随后立即序贯使用强效抗骨吸收药物地舒单抗(Denosumab)“巩固新骨”,是否能达到与打满12个月Romo同样优异的全髋部BMD获益?
LIDA研究是一项为期12个月的前瞻性、随机、开放标签的非劣效性临床试验,共纳入50名具有高
3个月序贯组(3-month ROMO组):前3个月皮下注射Romo(210mg/月),随后在之后的第3个月和第9个月分别皮下注射地舒单抗(60mg)。
12个月标准组(12-month ROMO组):持续12个月皮下注射Romo(210mg/月)。
1. 核心大考(全髋部BMD)
成功达到非劣效性界值:12个月时,3个月序贯组的全髋部BMD平均增长了 5.7%,而12个月标准组平均增长了 6.0%。两组间差异仅为0.4%(90% CI: -1.2至1.9,p=0.644),完全落在预设的严苛非劣效性阈值(2%)内,表明缩短Romo疗程并未造成核心负重部位骨量获益的显著损失。
2. 多部位骨量齐升
次要终点高度一致:除了全髋部,两组在全身多个骨骼位点的BMD增长均未表现出统计学显著差异:
腰椎 BMD:10.6% vs 12.5% (p=0.184)。
股骨颈 BMD:5.0% vs 6.3% (p=0.29)。
桡骨远端 BMD:-0.3% vs -1.5% (p=0.079)。
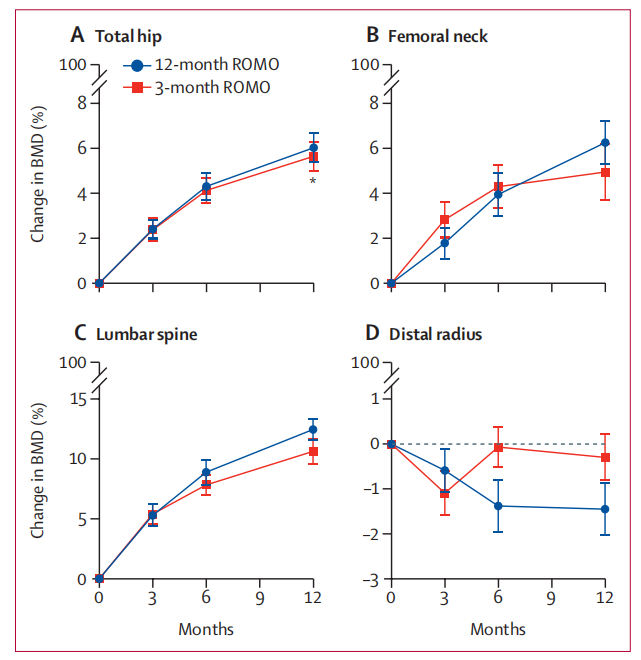
图 治疗12个月期间的骨密度(BMD)变化情况
3.骨转换标志物(BTMs):机制的印证
血清学数据精准反映了药物机制的切换:在治疗前3个月,两组患者的促成骨标志物(P1NP)均显著升高;而在第3个月后,序贯地舒单抗组的骨吸收(CTX)和骨形成(P1NP)标志物均受到更深度的抑制,体现了抗骨吸收药物的“守卫”作用。
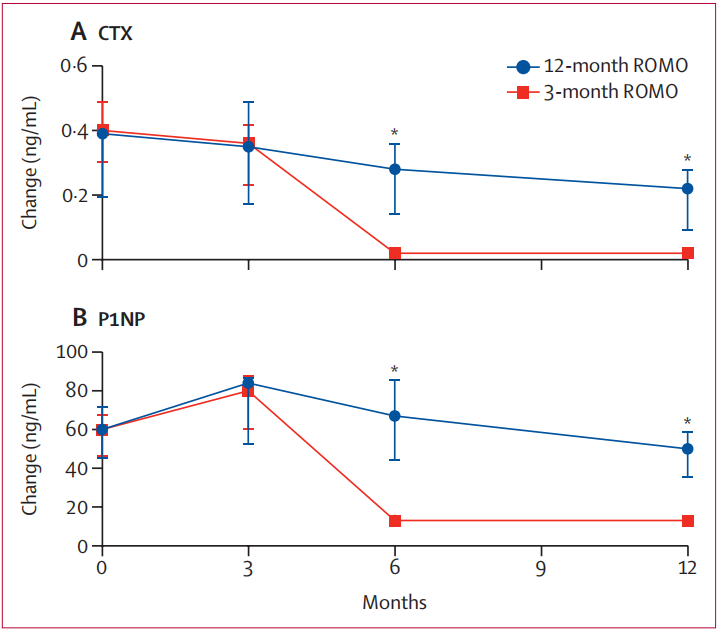
图 治疗12个月期间骨转换血清标志物的变化情况
如果疗效不相上下,新方案的临床价值体现在哪里?
LIDA研究为内分泌及骨松领域的医生带来了一个充满智慧的临床策略:精准利用Romosozumab黄金窗口期“强力冲刺”,序贯地舒单抗进行“长效维稳”。
作为首个验证该策略的RCT,本研究不仅在循证医学上证实了BMD获益的非劣效性,更为创新药物在真实世界中的可及性优化指明了方向。对于中国临床实践而言,这种“缩减版”方案有望让更多受限于经济成本或就医不便的高骨折风险患者,拥有接触并完成顶尖促成骨治疗的机会。未来,期待能有以骨折发生率为直接终点的大规模研究,进一步夯实该策略的长期循证基石。
参考文献