目前,
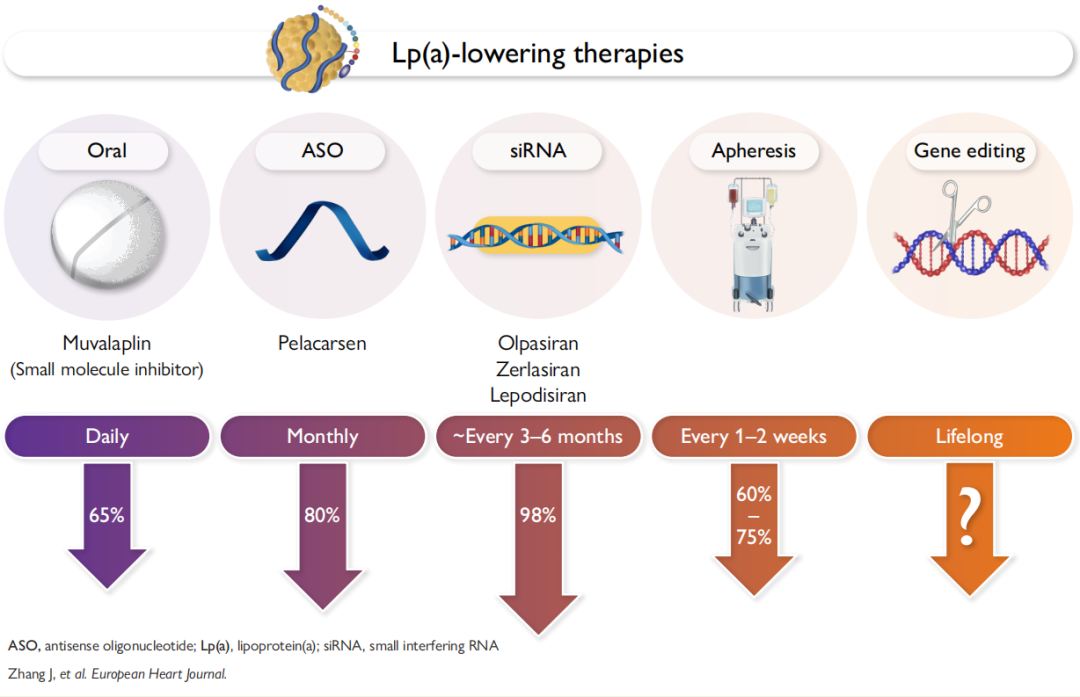
图1 中心图
现有降脂疗法对Lp(a)水平的影响
虽然传统降脂疗法降低LDL-C的疗效显著,但降低Lp(a)的作用有限;生活方式干预对Lp(a)降低的作用亦是微乎其微,亟需研发更高效、靶向性更强的治疗策略。
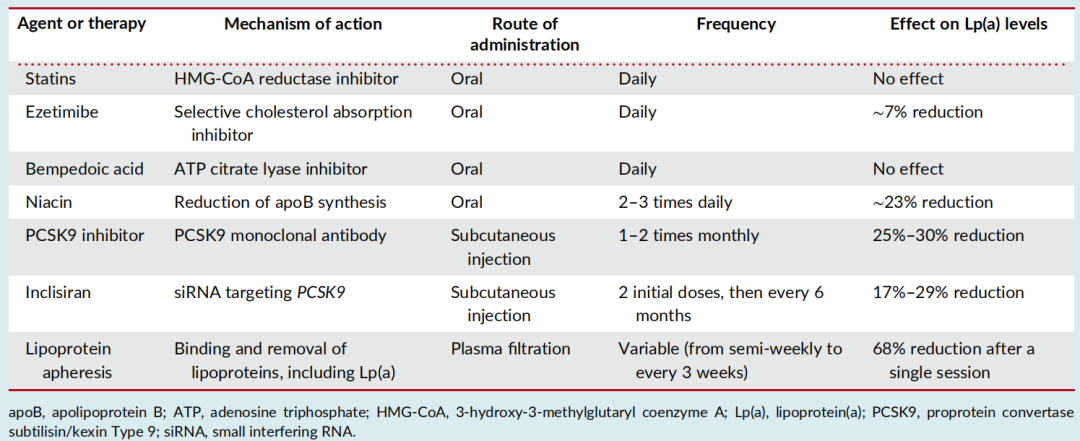
表1 现有降脂疗法作用机制、给药方式及Lp(a)降低疗效
0
1
他汀类药物是降脂治疗的基础,其降低LDL-C的作用和心血管获益已得到充分证实,但该类药物无法降低Lp(a)水平。早期研究结果甚至提示,他汀类药物或可升高Lp(a)水平(8.5%~19.6%),但荟萃分析并未证实这一结论,相关机制也尚未明确,且本文中涉及的其他降脂药物均为表现出类似升高Lp(a)的作用。
依折麦布的主要作用机制为抑制肠道胆固醇吸收,从而降低LDL-C水平,但其对Lp(a)水平的影响极小,且现有证据并不一致。荟萃分析显示,进行依折麦布单药治疗可使Lp(a)水平降低约7%,该降幅虽有统计学意义,但无临床意义。此外,另一项荟萃分析显示,依折麦布对Lp(a)水平无任何影响。
贝派地酸(Bempedoic acid)是一种口服的三磷酸
烟酸可抑制apoB合成,从而降低LDL-C、甘油三酯和Lp(a)水平。
荟萃分析(纳入14项随机研究)显示,烟酸可使Lp(a)水平降低23%。然而,目前尚未在仅纳入高Lp(a)血症人群的研究中验证烟酸的疗效,且事后分析提示,即使在高Lp(a)血症人群中,烟酸也无明显获益。
AIM-HIGH研究显示,在接受
总体而言,目前应用烟酸治疗高Lp(a)血症尚缺乏明确证据,且存在血糖控制不佳、出血及感染等潜在不良反应风险。
PCSK9单克隆抗体可通过抑制PCSK9活性,上调低密度脂蛋白受体表达。总而而言,无论PCSK9抑制剂降低Lp(a)的作用能否在其介导的apoB或非HDL-C降低基础上带来额外获益,FOURIER和ODYSSEY OUTCOMES两项试验均证实,Lp(a)水平升高人群的心血管风险更高,且PCSK9抑制剂介导的LDL-C降低,可降低高Lp(a)血症人群的ASCVD事件整体风险。
英克司兰是靶向PCSK9基因的小干扰RNA(siRNA)疗法,可降低LDL-C水平。对ORION-9、ORION-10和ORION-11试验的分析显示,英克司兰可使Lp(a)水平降低17.2%~28.5%。目前,Lp(a)用于ASCVD预防的心血管结局试验正在开展,但该试验并非专门针对高Lp(a)血症人群。
胆固醇酯转移蛋白(CETP)抑制剂可通过干扰脂蛋白间的胆固醇酯转移,从而降低Lp(a)水平。目前以obicetrapib为代表的新型CETP抑制剂已在Ⅲ期临床试验中取得积极成果,或有望在未来几年内投入临床使用。
CETP抑制剂Anacetrapib相关REVEAL试验显示,在强化他汀治疗基础上,进行Anacetrapib治疗,可降低心血管事件风险,同时降低非HDL-C水平18%、Lp(a)水平25%。然而,由于Anacetrapib可蓄积于脂肪组织,因此未被推进至商业化阶段。此外,研究还提示,Anacetrapib降低Lp(a)的作用并未在非HDL-C降低基础上带来额外获益。
强效、高选择性CETP抑制剂Obicetrapib的Ⅲ期BROADWAY试验显示,在既往有ASCVD病史或杂合子
在现有疗法中,脂蛋白分离术是降低Lp(a)最有效的方法。德国前瞻性多中心研究显示,单次脂蛋白分离术治疗可使Lp(a)水平降低68.1%。对接受脂蛋白分离术治疗的患者进行5年随访发现,进行规律Lp(a)分离术治疗后,患者的心血管事件发生率降低。
尽管该结果令人鼓舞,但目前尚无大型随机对照研究验证脂蛋白分离术在降低心血管事件方面的疗效;且即使在已批准使用该疗法的国家,其临床可及性也较低。此外,频繁的医院就诊、静脉通路需求以及高昂的费用,均限制了其广泛应用。
高Lp(a)血症患者的现有管理策略
对于Lp(a)水平升高的患者,应根据现行指南,采用现有疗法优化其心血管疾病危险因素,包括进行高强度他汀类药物治疗,必要时联用新型降脂药物,以降低心血管疾病绝对风险。
值得关注的是,传统风险评估量表/评分或无法反应高Lp(a)血脂所带来的个体化风险。降低传统风险因素虽可带来整体获益,但或不足以抵消高Lp(a)水平介导的残余风险。《2025ESC/EAS
现有部分研究提示,
目前,多种新型疗法正在研发中,其降低Lp(a)的疗效显著优于现有药物,或可通过靶向治疗解决Lp(a)相关的心血管疾病风险(表2)。
表2 降低Lp(a)的新兴疗法
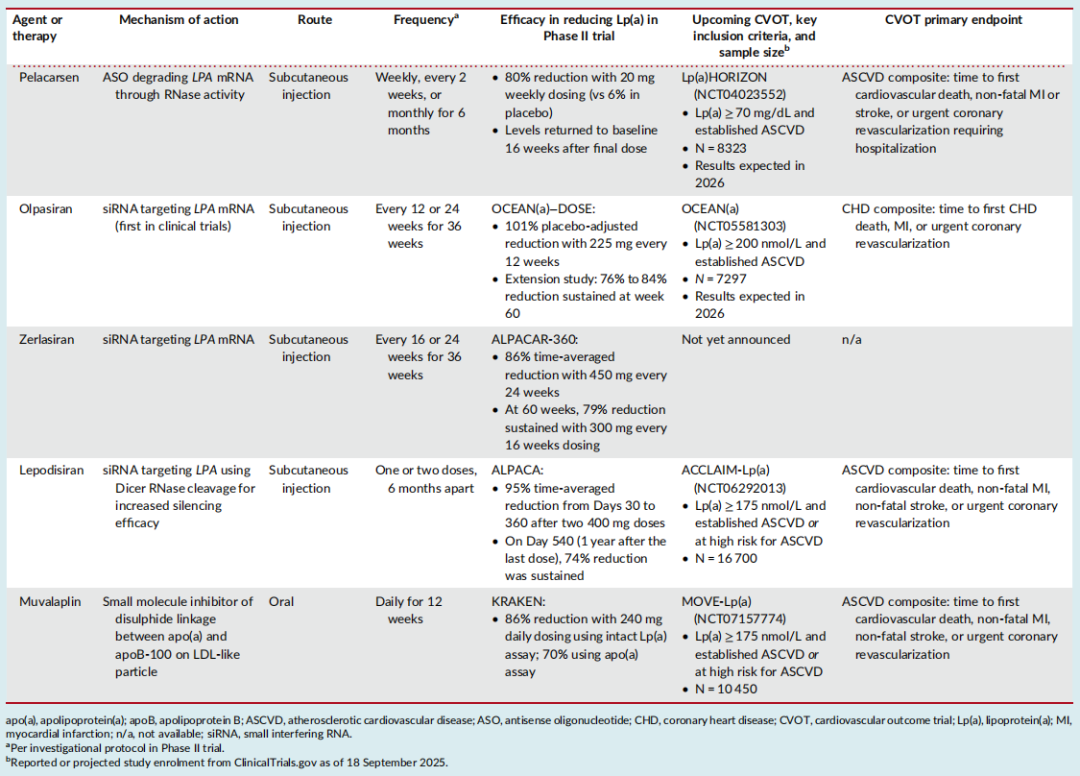
在研Lp(a)降低疗法
Apo(a)仅在肝细胞中合成,因此肝脏apo(a)合成过程成为治疗干预的主要靶点。近年来,靶向肝脏信使
Pelacarsen可通过与LPA mRNA结合,诱导其降解,从而减少apo(a)的合成,进而降低Lp(a)水平。Pelacarsen Ⅱ期随机对照试验(Lp(a)水平升高的ASCVD患者)的结果显示,Pelacarsen治疗6个月后,Lp(a)水平较基线降低80%,而安慰剂组仅降低6%;末次给药后16周,Lp (a)恢复至基线水平。除此之外,Pelacarsen还可降低apoB和LDL-C水平。
治疗组最常见的不良反应为肌痛、关节痛和全身乏力,且不良反应与剂量无明显关联,5%的患者因不良反应退出研究。目前,Pelacarsen的Ⅲ期心血管结局试验HORIZON正在进行中,预计将在2026年完成。
目前,Olpasiran、Zerlasiran和Lepodisiran三款siRNA类药物已进入临床研究阶段。
Olpasiran是首个进入临床试验的靶向LPA的siRNA药物。OCEAN (a)-DOSE Ⅱ期试验结果显示,在治疗36周时,Olpasiran组的Lp(a)水平较基线安慰剂校正的降幅为71%~101%,同时apoB(最高校正降幅19%)和LDL-C(最高校正降幅25%)水平也显著降低。Olpasiran的治疗相关不良反应较少,最常见的为注射部位反应和超敏反应。
对Ⅱ期研究对象的停药延伸研究显示,Olpasiran降低Lp(a)的效果虽有所减弱,但仍能持续:治疗60周时(12周给药组末次给药后24 周、24周给药组末次给药后36周),所有剂量组的Lp(a)水平仍降低76%~84%;治疗96周时(末次给药后60~72周),Lp(a)水平仍降低 28%~36%。目前,Olpasiran的心血管结局试验OCEAN(a)正在开展,预计2026年底完成,我们拭目以待。
Zerlasiran是另一种靶向肝脏LPA基因mRNA的siRNA。Ⅱ期剂量探索ALPACAR-360试验,将ASCVD患者随机分配至Zerlasiran 450 mg每24周1次组、300 mg每24周1次组、300 mg每16周1次组,或每16 周/24周1次的安慰剂组。
结果显示,在治疗36周末,450mg组的Lp(a)降幅最大(85.6%)。在研究开始60 周时(末次给药后28~36周),300 mg每16周1次组的Lp(a)水平较基线的降幅仍为最大(79.2%),提示更频繁给药可提升疗效的持久性。
除此之外,Zerlasiran还可降低LDL-C和apoB水平:治疗60周时,LDL-C降低24%~29%,apoB降低7%~13%。Zerlasiran的耐受性也较好,最常见的治疗相关不良反应为一过性注射部位反应,无严重治疗相关不良反应,也无患者因不良反应退出研究。目前,Zerlasiran Ⅲ期试验尚未公布。
Lepodisiran可通过结合LPA mRNA并促进其降解,减少Lp(a)颗粒的生成。ALPACA Ⅱ期试验显示,接受单次400 mg剂量治疗的患者,在治疗后第60~180天期间,Lp(a)的安慰剂校正时间平均降幅达93.9%(主要终点);且治疗效果具有持久性。
此外,Lepodisiran治疗还可使LDL-C和apoB水平实现了持续性降低;且总体耐受性良好,未观察到严重不良事件,部分患者出现轻度注射部位反应或肝功能异常,但均自行缓解。
目前,ACCLAIM-Lp (a)心血管结局试验计划纳入二级预防和一级预防高风险的混合人群,旨在探究Lepodisiran能否带来心血管获益。
Muvalaplin是一种口服的Lp(a)合成小分子抑制剂,可抑制apo(a)与apoB-100的相互作用,从而抑制Lp(a)的生成。
Lp(a)的检测方法是Muvalaplin研发过程中的一个挑战:现有Lp(a)检测试剂盒均以apo(a)为检测靶点,而在Muvalaplin作用下,试剂盒会同时检测游离的apo (a)和Lp(a)颗粒中结合的apo(a),或高估完整Lp(a)的水平。
KRAKEN Ⅱ期试验采用两种不同的apo(a)检测方法评估了Muvalaplin降低Lp(a)的疗效和安全性。研究显示,治疗12周后,10 mg、60 mg和240 mg剂量组的完整Lp(a)降幅分别为47.4%、81.6%和85.7%,而安慰剂组则无明显降低;采用传统仅检测apo(a)的方法时,降幅更小(分别为42.3%、70.9%和69.9%),证实了游离apo(a)的存在会导致完整Lp(a)水平的检测结果被低估。此外,240 mg剂量组治疗12周时,apoB和LDL-C的安慰剂校正降幅分别为16%和21%。严重不良反应发生率较低。目前,Muvalaplin的Ⅲ期心血管结局试验 MOVE-Lp(a)已正式启动。
近十年来,基于CRISPR-Cas9系统的基因编辑技术成为靶向多种遗传性疾病的研究热点。靶向LPA基因的基因编辑疗法,可通过减少apo(a)合成,抑制Lp(a)颗粒组装,其潜在优势在于作用的永久性,在理论上讲仅需单次治疗即可实现Lp(a)永久性降低。
目前,动物试验已初步证实了基因编辑疗法的可行性。有研究显示,在转基因小鼠中,CRISPR–Cas9基因编辑后1周内,apo(a)蛋白从血浆中几乎完全消除,并在4周内保持稳定。在食蟹猴中进行的早期数据显示,肝脏的LPA基因编辑呈剂量依赖性,治疗第15天,最高剂量组(3 mg/kg)的血浆Lp(a)水平较基线降低90%,且该效果可持续至研究结束(第 84 天)。一项单剂量研究(2mg/kg,食蟹猴)显示,治疗第14天的Lp(a)水平较基线降低94%,且该降幅在第224天复查时仍维持。
然而,目前尚未进行相关人体试验,Ⅰ期临床试验正在招募研究受试者。
Lp(a)降低疗法的其他潜在疗效靶点
除降低ASCVD风险外,Lp(a)水平升高还与钙化性
然而,目前临床尚无靶向CAVS进展的有效疗法,正在开展的FRONTIERS-CAVS试验提示,Pelacarsen可延缓轻中度CAVS合并高Lp(a)血症患者的疾病进展,若试验结果阳性,将为CAVS管理提供全新策略,大幅拓展Lp(a)靶向疗法的临床应用范围。
结 语
高Lp(a)血症人群的ASCVD事件风险显著升高,目前多种靶向Lp(a)的药物疗法正在研发中,这些疗法能显著降低Lp(a)水平,或可降低极高Lp(a)血症人群新发和复发性ASCVD事件风险。正在开展的心血管结局试验结果,将最终验证这些疗法在一级和二级预防中降低心血管事件的安全性和有效性。
未来,随着新兴靶向疗法的临床转化,Lp(a)相关心血管残余风险有望被降低/消除,为ASCVD及CAVS的防治提供全新策略,推动心血管疾病管理格局的重大变革。
医脉通编译自:Jingwen Zhang, Ann Marie Navar,Lale Tokgozoglu. Lipoprotein(a)-lowering therapies: a promising future. European Heart Journal (2026) 00, 1–11. https://doi.org/10.1093/eurheartj/ehag092
编辑&排版:GXM
医脉通是专业的在线医生平台,“感知世界医学
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)