医脉通乳腺肿瘤特别策划:“药”怎么用?
取材自国内正式获批的抗
德达博妥单抗(Dato-DXd)是一种靶向TROP-2的新型抗体药物偶联物(ADC),由人源化抗TROP-2抗体通过可裂解连接子与拓扑异构酶I抑制剂有效载荷偶联而成,兼具精准靶向与强效杀伤的双重优势,为乳腺癌患者提供了新的治疗选择。
本文将详细介绍德达博妥单抗的作用机制、使用方法及注意事项等,旨在帮助患者和临床医生更全面地理解这一药物,为抗击乳腺癌提供重要支持。

德达博妥单抗(达卓优)药理作用
Pharmacology
a
成份

>活性成份:德达博妥单抗
b
性状

>白色至黄白色冻干粉
>规格:冻干剂型:100mg/瓶。
c
药理

> 德达博妥是一种靶向滋养层细胞表面抗原2(TROP2)的抗体偶联药物(ADC),由人源化抗TROP2免疫球蛋白G1(IgG1)单克隆抗体通过四肽一可裂解连接子与拓扑异构酶抑制剂I(DXd,一种依喜替康衍生物)共价连接。德达博妥与肿瘤细胞上的TROP2结合后可内化进入肿瘤细胞,其连接子被裂解后释放DXd,抑制拓扑异构酶Ⅰ活性,从而诱导DNA损伤和细胞凋亡。
乳腺癌适应证
Breast Cancer Indications
> 本品用于治疗既往接受过内分泌治疗且在晚期疾病阶段接受过至少一线化疗的不可切除或转移性的激素受体(HR)阳性、人类表皮生长因子受体2(HER2)阴性(IHCO、IHC 1+或IHC 2+ISH-)乳腺癌成人患者。
剂量与给药方式
Dosage & Mode of Administration
a
用法用量

> 本品用于静脉给药。必须由医疗卫生专业人员复溶和稀释,通过静脉输注给药。本品不得以静脉推注或快速静脉注射方式给药。
b
给药方案

>本品推荐剂量为6mgkg(体重≥90kg的患者的最大剂量为540mg),采用静脉翰注给药,每3周一次(每周期21天),直至疾病进展或出现无法耐受的毒性。
>首次输注:输注应持续至少90分钟。输注过程中应观察患者,且首次给药后应至少留观1小时,以观察是否出现输液相关反应。
>第二次输注:如果首次输注时患者耐受性良好,第二次输注时间可缩短为至少30分钟。输注过程中应观察患者,且输注后应至少留观1小时。
>后续输注:如果既往输注时患者耐受性良好,本品的后续输注可缩短为至少30分钟。输注过程中观察患者,且输注后应至少留观30分钟。
c
剂量调整

>针对输液相关反应的剂量调整
如果患者发生输液相关反应,应减慢输注速率或中断输注。如发生危及生命的输液反应,则应永久停药。
>针对不良反应的剂量调整
根据表1和表2中的指导对不良反应进行管理,可能需要延迟给药、降低剂量或终止治疗。
降低剂量后,请勿再重新上调本品剂量。对于无法耐受3mg/kg每3周一次静脉给药的患者,永久停药。
表1 因不良反应而降低剂量

表2 针对不良反应的剂量调整
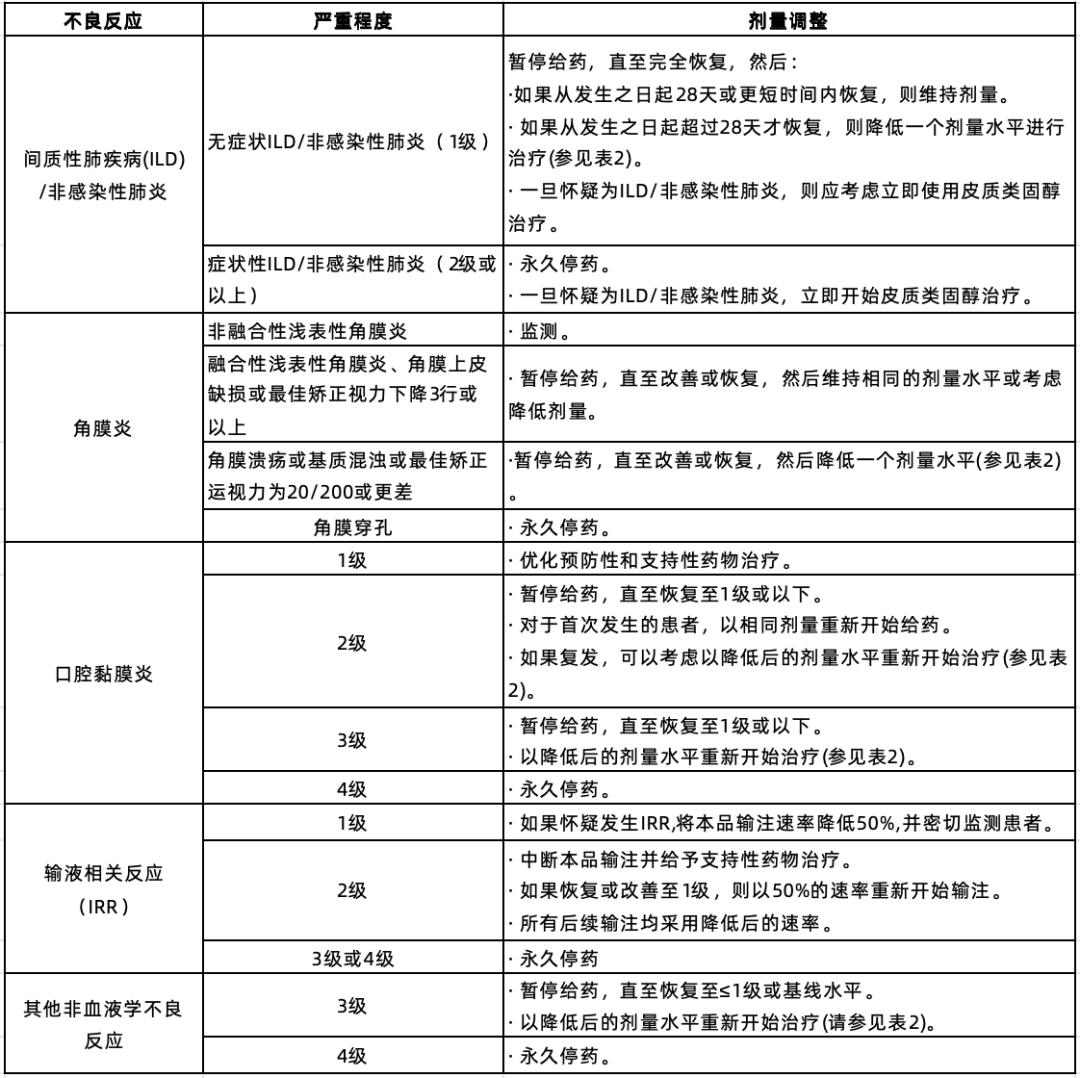
d
给药延迟或漏用

>如果计划给药出现延迟或漏用,应尽快给药,无需等到下一个计划周期。同时应调整后续给药时间表,确保两次给药间隔为3周。
e
特殊人群

>老年用药
65岁或以上患者无需调整本品剂量。TROPION-Breast 01研究中有365例患者随机至本品6mg/kg试验组,其中65岁及以上患者占24.9%。65岁及以上的患者和较年轻患者之间未观察到疗效和安全性的总体差异。本品在85岁及以上患者中的数据有限。
群体药代动力学分析表明,年龄对本品的药代动力学并无具有临床意义的影响。
>儿童用药
尚未确定本品在18岁以下儿童和青少年患者中的安全性和有效性。
>孕妇及哺乳期妇女用药
妊娠:尚未获得本品用于妊娠期妇女的数据。然而,根据动物研究结果及作用机制,在对妊娠女性给药时,本品的拓扑异构酶抑制剂组分可导致胚胎-胎儿损害。不建议孕妇使用本品,应在患者妊娠前告知本品对胎儿的潜在风险。女性患者一旦妊娠,必须立即联系医生。
哺乳期:尚不清楚本品是否会分泌至母乳中。由于很多药物可分泌至母乳中,且可能会对接受哺乳的婴儿造成严重不良反应,因此建议哺乳期女性在开始本品治疗前停止母乳喂养。哺乳期女性可在治疗结束后1个月后开始母乳喂养。
避孕:开始本品给药前,应确认有生育能力的女性的妊娠状态。有生育能力的女性应在本品治疗期间以及末次给药后至少7个月内采取有效的避孕措施。有具有生育能力女性伴侣的男性患者应在本品治疗期间以及末次给药后至少4个月内采取有效的避孕措施。
生育力:尚未对本品进行专门的生育力研究。基于动物毒性研究的结果,本品可能会损害生殖功能和生育力。在开始治疗前,应告知男性和女性患者寻求有关生育力保留的建议。尚不清楚本品或其代谢物是否存在于精液中。整个治疗期间,以及本品末次给药后至少4个月,男性患者不得冷冻或捐断精子。整个治疗期间,以及本品末次给药后至少7个月,女性患者不得捐献卵子或取卵自用。
>肾功能损害患者
轻度至中度肾功能损害(肌酐清除率[CLcr]:30至<90mL/min)患者无需调整剂量。尚未确定本品在重度肾功能损害患者中的推荐剂量。应密切监测重度肾功能损害患者。在接受本品6mg/kg治疗的基线时为中度肾功能损害的患者中,与肾功能正常的患者相比,观察到严重不良反应的发生率更高。
>肝功能损害患者
轻度肝功能损害(总胆红素≤正常值上限[ULN]且天门冬氨酸转移酶[AST]>ULN,或总胆红素>1至1.5倍ULN且无论AST值如何)患者无需调整剂量。对于中度(总胆红素>1.5至3倍ULN且无论AST值如何)肝功能损害的患者,用于确定剂量调整建议的数据有限。本品在重度(总胆红素>3倍ULN且AST值不限)肝功能损害患者中的数据不足。因此,应密切监测中重度肝功能损害患者。
动力学特征
Kinetics
a
分布

> 本品的稳态分布容积为3.52L。
体外研究显示,在10ng/mL至100ng/mL的浓度范围内,DXd的平均人血浆蛋白结合率为96.8至98.0%,DXd在血液/血浆中的浓度比为0.59至0.62。
b
生物转化

>本品在溶酶体酶的作用下发生细胞内裂解,释放DXd。
预期人源化TROP2IgG1单克隆抗体将通过与内源性lgG相同的方式经分解代谢途径降解为小分子肽和氨基酸。
人肝脏微粒体体外代谢研究表明,DXd主要通过CYP3A4的氧化途径代谢,不会显著通过UGT或其他CYP酶进行代谢。
c
消除

>本品的清除率估计值为0.57L/天。中位消除半衰期(t1/2)为4.82天,DXd的中位t1/2约为5.50天。在第1周期至第3周期期间,在6mg/kg剂量下未观察到本品蓄积情况。
大鼠和猴经静脉给予DXd后,主要排泄途径为粪便(经胆汁排泄)。DXd是尿液、粪便和胆汁中含量最高的药物成分。
d
线性/非线形

>经静脉给药,在4mg/kg至10mg/kg的剂量范围内(约为推荐剂量的0.7至1.7倍),本品和释放的DXd的暴露量与剂量成比例增加。
注意事项
Precautions
a
间质性肺疾病/非感染性肺炎

>本品可引起严重、危及生命或致死性间质性肺疾病(ILD)或非感染性肺炎。
>在本品治疗期间,应监测患者是否出现提示ILD/非感染性肺炎的新发或恶化的呼吸道症状(如呼吸困难、咳嗽、发热)。对于无症状(1级)的ILD/非感染性肺炎,考虑使用皮质类固醇进行治疗(例如,≥0.5mg/kg/天泼尼松龙或等效药物)。对于症状性ILD/非感染性肺炎(2级或以上),应立即开始系统性皮质类固醇治疗(例如,≥1mgkg/天泼尼松龙或等效药物),并持续治疗至少14天,随后逐渐减量(至少4周)。
>疑似发生ILD/非感染性肺炎的患者应暂停本品治疗,确诊≥2级ILD/非感染性肺炎时应永久停药。
b
眼部不良反应

>本品可引起眼部不良反应,包括干眼、角膜炎、睑缘炎、睑板腺功能障碍、流泪增加、结膜炎和视物模糊。
>建议患者每日数次滴用不含防腐剂的润眼液进行预防治疗。建议患者避免使用隐形眼镜,除非在眼科医生或护理专业人员的指导下进行。
>在本品治疗开始时、治疗期间(每年一次)、治疗结束时、以及出现临床指征时,应将患者转诊至眼科医生或护理专业人员处进行眼科检查,包括视力检查、裂隙灯检查(含荧光素染色)、眼内压、以及眼底镜检查。
>如果患者出现任何新发或恶化的眼部不良反应,应及时将其转诊至眼科医生或护理专业人员处。在本品治疗期间,应监测患者是否发生眼部不良反应,如果确诊发生相关反应,应根据严重程度延迟给药、降低剂量或永久停药。
c
口腔黏膜炎

>本品可引起口腔黏膜炎,包括口腔溃疡和口腔黏膜炎。
>建议患者使用含类固醇的漱口水预防和治疗口腔黏膜炎。在无法获得含类固醇的漱口水的情况下,可推荐使用温和的漱口水(例如,使用不含酒精和/或含碳酸氢盐的漱口水)。建议患者在本品的输注期间全程将冰块或冰水含在口中。
>应监测患者是否出现口腔黏膜炎体征和症状。如果发生口腔黏膜炎,增加漱口水使用频率,并根据临床指征进行其他局部治疗。根据不良反应的严重程度,暂停给药、降低剂量或永久停药。
d
胚胎-胎儿毒性

>根据本品的作用机制,妊娠女性使用本品时可能会对胚胎-胎儿造成伤害,因为本品的拓扑异构酶抑制剂组分DXd具有遗传毒性,可影响活跃分裂细胞。
>应告知患者本品对胎儿的潜在风险。建议有生育能力的女性患者在本品治疗期间和末次给药后7个月内采取有效的避孕措施。建议有具有生育能力女性伴侣的男性患者在本品治疗期间及末次给药后4个月内采取有效的避孕措施.
禁忌证
Contraindications
>禁用于已知对本品活性物质或任何辅料有超敏反应的患者。
【药物小结】
德达博妥单抗在HR阳性/HER2阴性晚期乳腺癌治疗领域已展现出显著价值,为接受过内分泌治疗且在晚期疾病阶段接受过至少一线化疗的患者提供了新的治疗选择。随着临床研究的不断深入,未来有望通过生物标志物筛选、联合治疗策略优化及更多前瞻性研究数据的积累,进一步拓展其适用人群,提升个体化治疗水平,为更多乳腺癌患者带来生存获益。
参考文献:
注射用德达博妥单抗说明书https://www.daiichisankyo.com.cn/Portals/0/340_0_AZCN_0705_123648_K3.pdf
编辑:Ocean
审校:Ocean
排版:Ocean
执行:Ocean
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)