
美丽
在医学地理学的版图上,存在一个长期悬而未解的疑问:居住在中国青藏高原、秘鲁安第斯山脉等高海拔地区的居民,其
这一"高原保护效应"在秘鲁、尼泊尔、中国西藏等地区反复得到验证,却始终缺乏机制层面的阐释。
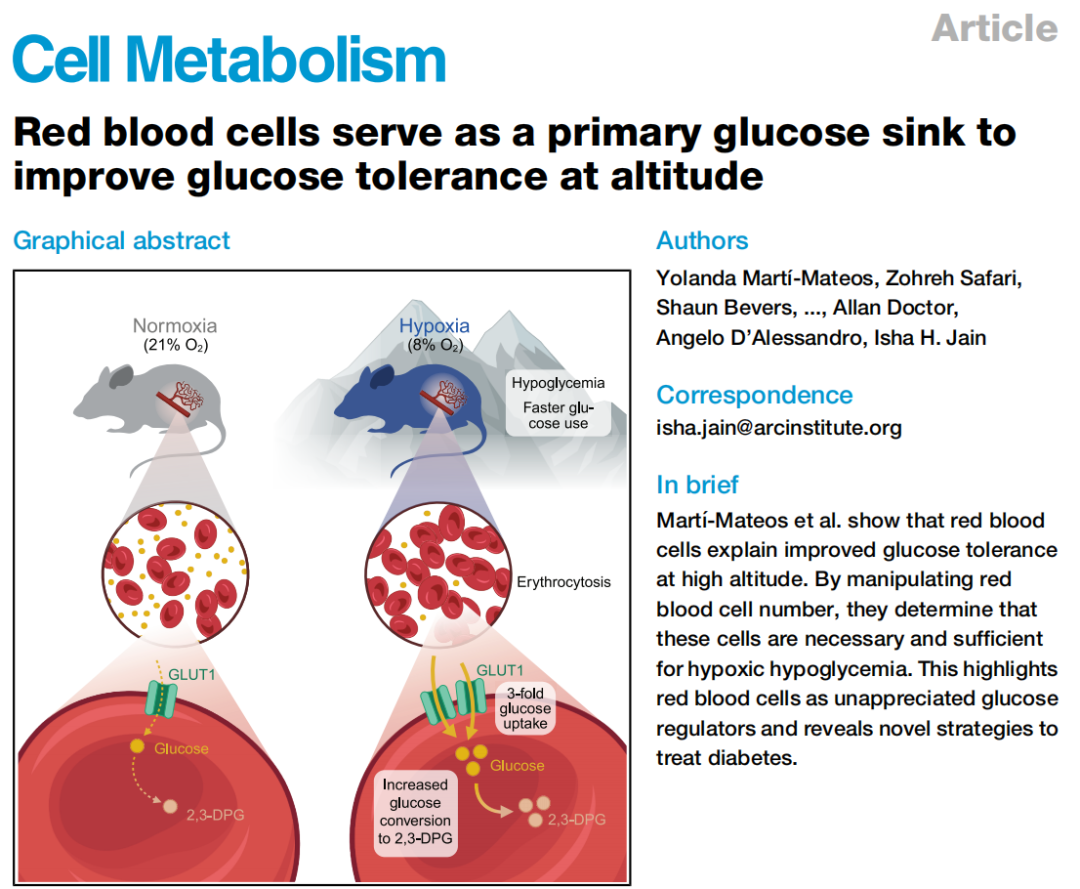
长期以来,科学界将这一现象归因于生活方式差异、紫外线暴露或饮食习惯。然而,2026年2月19日发表于Cell Metabolism的一项研究,揭开了这一谜团的面纱——红细胞,这群传统认知中“沉默的氧气搬运工",在缺氧环境下竟化身为高效的"血糖海绵"!


围绕“高海拔地区居民糖尿病风险更低”的科学探索,是一场跨越百年的生理学解密之旅。这一现象最早在20世纪20至40年代由哈佛疲劳实验室系统观察到,研究者发现被送往安第斯高地的健康志愿者糖耐量显著改善。尽管此后在藏猪、鹿鼠及多种高海拔鸟类中也发现了类似的进化适应特征,但其背后的确切生理机制在学界长期以来一直是一个未解之谜。
中国西藏地区(Xu et al. 研究):
在海拔 3,500–3,999 米的人群中,糖尿病风险的胜算比(OR)为 0.35,意味着风险比低海拔(<3,500米)对照组降低了约 65%。
在海拔 >4,000 米的人群中,风险进一步大幅下降,OR 仅为 0.11,意味着风险比对照组降低了约 89%。
美国地区(Woolcott et al. 研究):
在海拔 1,500–3,500 米的人群中,糖尿病风险的 OR 为 0.88,即风险比海拔 <499 米的地区降低了 12%。
厄瓜多尔地区(Lopez-Pascual et al. 研究):
在海拔 2,758–2,787 米的人群中,
传统的解释曾聚焦于外周组织在缺氧诱导因子(HIF)作用下增强了
1.1 意外的观察:低血糖与"失踪"的代谢底物
研究团队最初的关注点并非糖尿病,而是缺氧(hypoxia)状态下的代谢重编程。在先前的研究中,他们注意到暴露于低氧环境(8% O₂,持续3周)的小鼠表现出惊人的血糖清除能力——餐后血糖迅速下降,葡萄糖耐量显著改善。
然而,当研究人员采用PET/CT扫描追踪葡萄糖去向时,一个令人困惑的缺口出现了:即便将肌肉、肝脏、脑、脂肪等主要脏器的葡萄糖摄取量全部计算在内,仍有约70%的葡萄糖"去向不明"。这些糖分仿佛凭空消失,既未被主要代谢器官摄取,也未在血液中累积。
"当我们给缺氧状态的小鼠注射葡萄糖时,它几乎瞬间从血液中消失了,"该研究第一作者Yolanda Martí-Mateos博士回忆道,"我们检查了肌肉、大脑、肝脏——所有常规嫌疑对象——但无一能够解释这一现象。"
1.2 假设的转向:血液本身的"隐形消耗"
面对这一代谢黑洞,研究团队提出了一个大胆假设:葡萄糖的"消失"可能发生在血液系统内部。红细胞(RBCs)作为人体最丰富的细胞类型(约占细胞总数的85%),传统上被视为代谢惰性的简单载体,缺乏细胞核与线粒体,似乎不具备主动调节血糖的能力。
然而,红细胞具备几个关键特征使其成为理想的"嫌疑对象":其一,在慢性缺氧状态下,机体通过促
2.1 实验验证:从必要性到充分性
为验证红细胞的核心作用,研究团队设计了一系列精巧的"老派"实验。首先,他们通过反复放血(phlebotomy)阻止缺氧小鼠的红细胞增生,维持其红细胞数量于正常水平——每3天抽取相当于总血容量15%的血液,持续4周。结果令人震惊:单纯阻止红细胞增多,即可完全逆转缺氧诱导的低血糖效应,产生约170 mg/dL的稳定血糖平台。
随后,研究人员进行了反向验证:向正常氧环境下的健康小鼠输注额外的红细胞——连续两天每天两次眶后注射75%压积红细胞。仅仅增加红细胞数量,便足以降低血糖水平,且效果与缺氧暴露2周相当。这一系列实验确立了红细胞在血糖调控中的必要性与充分性——它们不仅是缺氧适应的被动参与者,更是主动清除循环葡萄糖的关键效应器。
2.2 分子机制:GLUT1上调与"缺氧记忆"
深入探究发现,缺氧环境下新生的红细胞具有独特的"代谢印记"。通过生物素标记实验(连续3天注射生物素标记已有红细胞),研究团队区分了缺氧前已存在的"老"红细胞与缺氧期间新生的"新"红细胞。流式细胞术分析显示,仅在缺氧骨髓中成熟的新生红细胞表现出GLUT1葡萄糖转运蛋白的显著上调,而老红细胞无此变化。
这一发现揭示了一个精妙的发育编程机制:缺氧并非直接改变成熟红细胞的功能,而是通过重塑骨髓造血微环境,"预设"新生红细胞具备更强的葡萄糖摄取能力。这些细胞一旦进入循环,便维持其高GLUT1表达水平长达数月,形成持久的"代谢记忆"。
2.3 代谢流向:2,3-DPG的枢纽作用
葡萄糖进入红细胞后去向何方?同位素示踪实验给出了答案:缺氧红细胞将葡萄糖迅速转化为2,3-二磷酸甘油酸(2,3-DPG)。这一分子与
值得注意的是,这一过程涉及一个快速可逆的分子开关。在正常氧状态下,糖酵解关键酶GAPDH(甘油醛-3-磷酸脱氢酶)被锚定在细胞膜蛋白Band 3上,糖酵解速率受限。当氧分压下降,脱氧血红蛋白构象改变,竞争性结合Band 3(特别是β-珠蛋白HBB第83位残基与Band 3第212位残基结合),释放GAPDH,从而在数分钟内加速糖酵解通量,提升2,3-DPG产量。这一"代谢开关"不依赖基因转录或新蛋白合成,实现了对缺氧的秒级响应。
3.1 持久效应:缺氧暴露的后遗获益
研究的一个重要发现是,缺氧诱导的代谢益处具有长期持续性。小鼠在返回正常氧环境后,其改善的葡萄糖耐量可持续数周至数月。这一"后遗效应"提示,短期高原暴露或模拟缺氧干预可能产生持久的代谢重塑,为糖尿病预防提供了非药物干预的新思路。
3.2 HypoxyStat:药物模拟的破晓
更具临床转化价值的是,研究团队评估了一种名为HypoxyStat的小分子药物。该药物通过增强血红蛋白对氧气的亲和力,在不降低环境氧分压的情况下诱导"功能性组织缺氧"。在链脲佐菌素诱导的糖尿病小鼠模型中,HypoxyStat治疗完全逆转了高血糖状态。
3.3 治疗前景与挑战
尽管前景广阔,临床应用仍面临诸多挑战。红细胞输注显然不适合作为长期疗法,但研究提示了若干可行方向:工程化改造红细胞以增强其葡萄糖亲和力,或通过调控红细胞周转促进"高代谢活性"的年轻红细胞群体扩增。
此外,该机制对创伤后病理缺氧、运动生理学的潜在影响亦值得深入探索。正如合作研究者Angelo D'Alessandro博士所言:"红细胞通常被视为被动的氧气载体,然而我们发现,在缺氧状态下,它们可占据全身葡萄糖消耗的相当大比例。"
4.1 范式转移:重新认识红细胞
这项研究的最大启示在于重新定义了红细胞的生理角色。长期以来,血液学将红细胞简化为"血红蛋白囊袋",忽略了其作为动态代谢参与者的潜能。事实上,红细胞每天处理约20克葡萄糖,在缺氧条件下这一数字可能翻倍。
从进化视角看,这一机制具有深刻的适应性意义:在高海拔低氧环境中,机体需要同时解决两大挑战——向组织供氧与维持能量稳态。红细胞通过将葡萄糖代谢与氧运输功能耦联,实现了"一石二鸟"的优化策略。
4.2 未解之谜与未来方向
研究同时抛出了新的科学问题。首先,用于合成2,3-DPG的葡萄糖最终命运如何?其代谢产物是否参与全身信号调控?其次,若红细胞具备如此大规模的葡萄糖消耗能力,我们对整体能量代谢的理解是否存在系统性盲区?
此外,该机制在已有糖尿病患者中的适用性尚需验证。既往研究表明,缺氧环境下糖尿病患者的血糖控制可能面临特殊挑战,包括
这项研究的完成仅用时不到一年,其高效得益于研究者对"非主流"假设的勇气与对经典技术的回归——放血、
正如资深作者Isha Jain博士所言:"红细胞代表了一个此前未被重视的葡萄糖代谢隐形区室。这一发现为血糖控制开辟了全新的思路。"从高原居民的低糖尿病发病率,到红细胞的糖海绵效应,科学再次证明:有时,真理就隐藏在显而易见之处,等待一双愿意质疑常规的眼睛。
对于临床医师与医学生而言,这项研究不仅提供了一种潜在的糖尿病干预靶点,更启示我们:生理学的经典教条可能随时被新的证据改写,保持对"异常"现象的敏感与对"简单"解释的警惕,是医学探索者最宝贵的品质。
参考文献
本视频/资讯/文章的内容不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。医脉通是专业的在线医生平台,“感知世界医学

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)