引言
一例41岁复发转移性HER2+乳腺癌女性患者出现软脑膜受累。其初始诊断为导管癌,免疫组化显示HER2+,
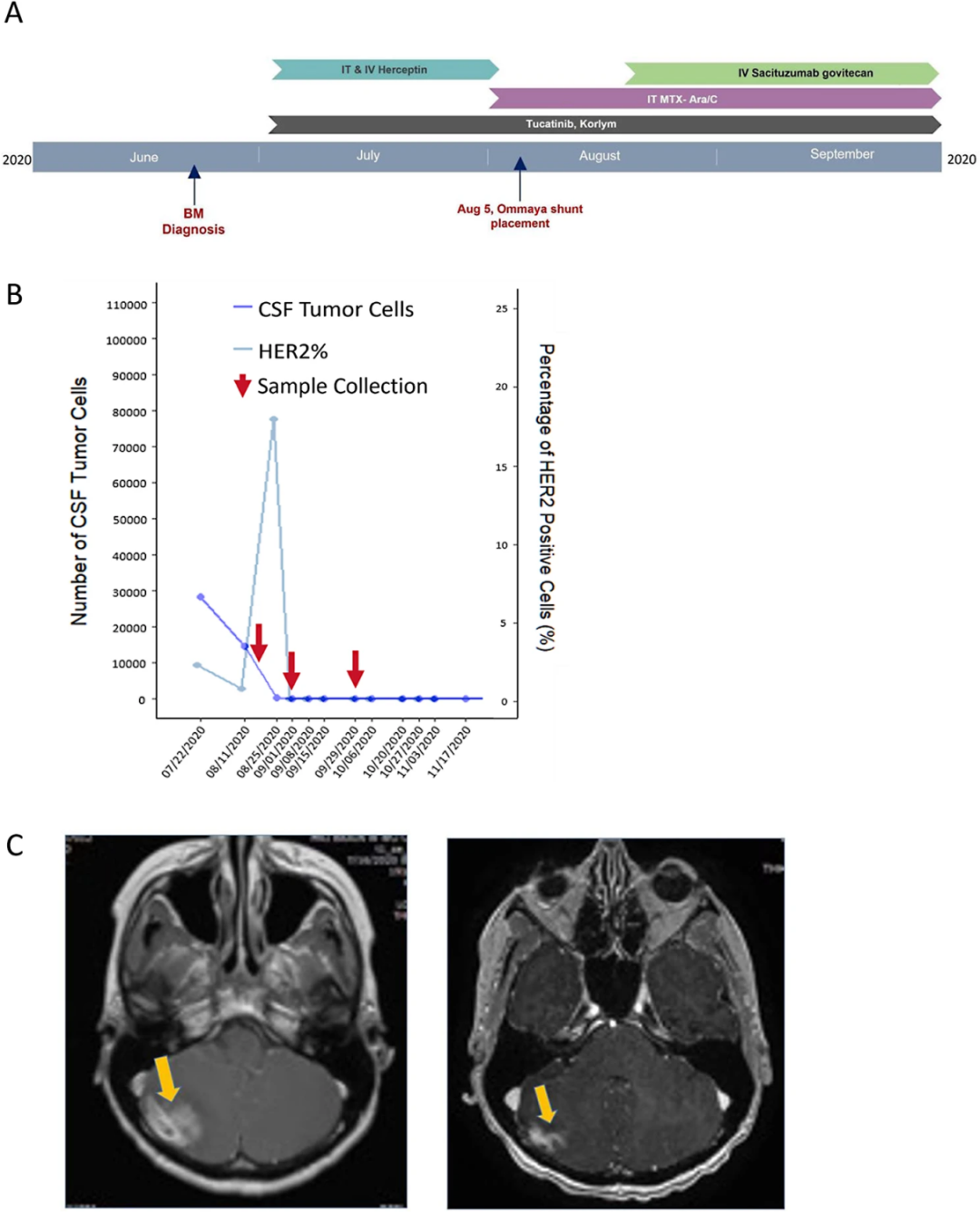
图1. 治疗史、脑脊液肿瘤细胞及MRI扫描显示的肿瘤反应[6]。(A)治疗史概述。(B)CSF肿瘤细胞数量及HER2阳性细胞百分比随时间变化曲线。(C)MRI扫描显示SG治疗前后肿瘤最大直径对比。
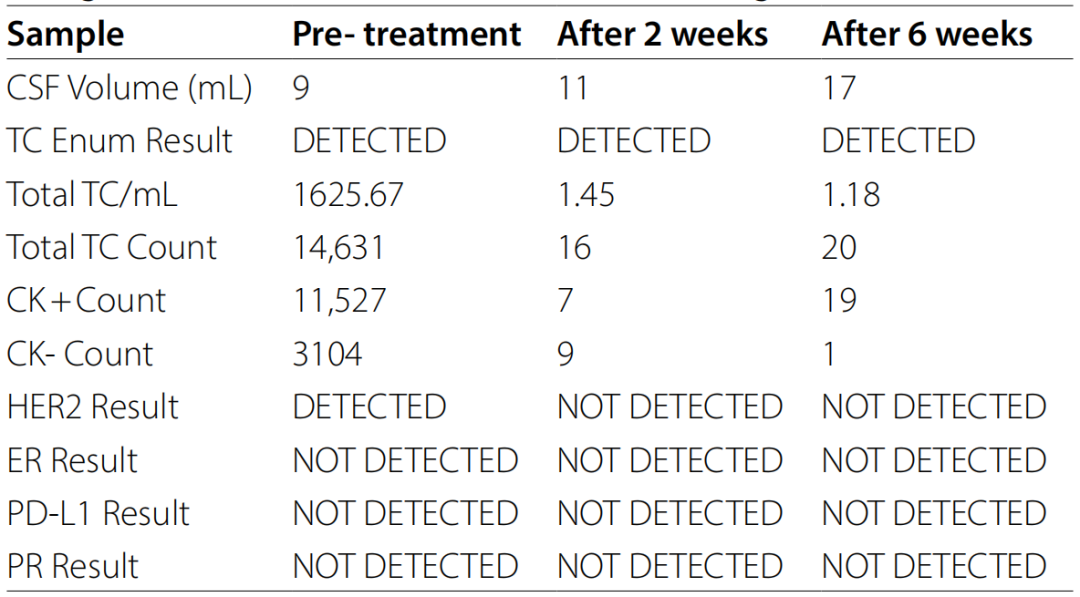
在开始SG联合鞘内治疗后约2周和6周采集脑脊液样本。细胞病理学分析及基因组表征结果显示,与基线水平相比,两个时间点的CTC数量均显著减少,且均未检测到表达HER2的细胞(表1;图1B)。在开始SG治疗后约4周进行的磁共振扫描显示肿瘤体积显著缩小(图1C),从影像学上证实了肿瘤负荷降低。
表1. 脑脊液细胞病理学分析及基因组表征结果[6]
通过单细胞RNA测序(scRNA-seq)技术,本研究对脑脊液微环境中的细胞图谱进行了全面解析。采用无监督聚类算法及UMAP降维可视化,表征了不同的细胞群体,揭示了脑脊液中肿瘤和免疫细胞类型的异质性。分析结果显示,脑脊液中存在CD8+ T细胞、CD4+ T细胞、B细胞、髓系细胞以及CTCs,并呈现出反映乳腺癌特征的基因表达谱。乳腺癌相关CTCs表现出显著的基因表达特征,包括PTPRF、KRT8、KRT19和KRT18等一系列基因的高表达,提示其具有恶性潜能并可能参与疾病进展(图2A,B,C)。此外,整合聚类分析鉴定了脑脊液样本中不同的细胞群体,整合UMAP图显示了代表各类细胞群的簇,表明脑脊液细胞群体具有异质性,如图2D所示。
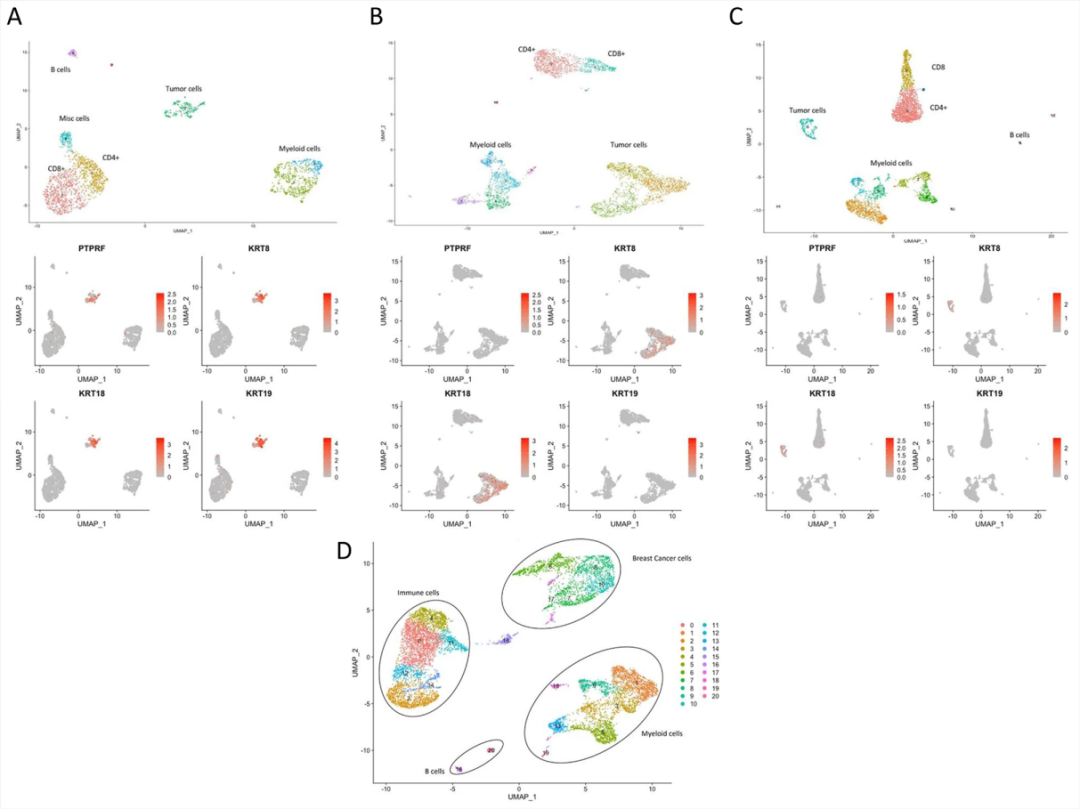
图2. 脑脊液单细胞转录组时序动态与整合UMAP可视化分析[6]。(A)治疗前;(B)治疗中;(C)治疗后;(D)整合UMAP图
随后,研究分析了与乳腺癌相关基因(PTPRF、KRT18、KRT19、KRT8)及TNBC特征基因(CRABP2、TM4SF1、KRT7)的表达水平在治疗过程中的变化。这些标志物的表达水平在不同样本间存在差异。图3A的小提琴图揭示了基因表达水平的变异性。图3B展示了细胞死亡相关基因(PCP4、MORN2、FHIT)在治疗期间的表达水平分布,图3C展示了细胞周期相关基因(TOP2A、MKI67、CCND1、CDT1)的表达分布,图3D则展示了三个时间点样本中基因表达水平的分布情况。
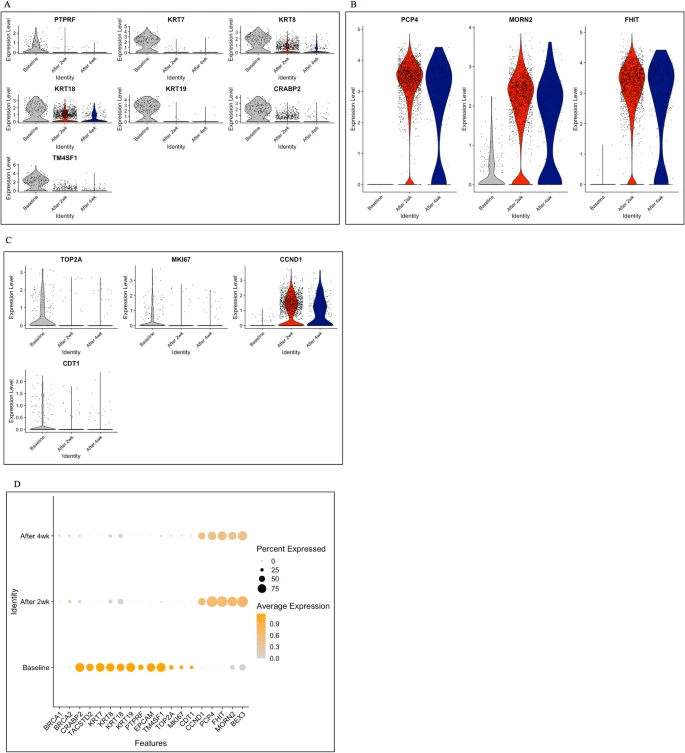
图3. 治疗诱导的基因表达变化[6]
在生成各样本差异表达基因热图后,对表达水平变化超过2倍的前20个基因进行了分析,以确定其相关生物学功能和通路。山脊图展示了这前20个差异表达基因在不同样本中的表达模式(图4A)。同时,分析了这些差异表达基因所涉及的功能背景,强调了受差异表达影响的前20个基因可能富集的生物学通路和过程(图4B,C)。值得注意的是,在对数据未进行任何过滤的分析中发现,存在一个数量较少但增殖活性极高的细胞群体,其乳腺癌标志物及HER2表达水平均很高,并且在治疗后持续存在,这可能提示存在治疗抵抗的肿瘤细胞。然而,由于本研究样本量有限,未来需要在更大规模的数据集中进行验证。
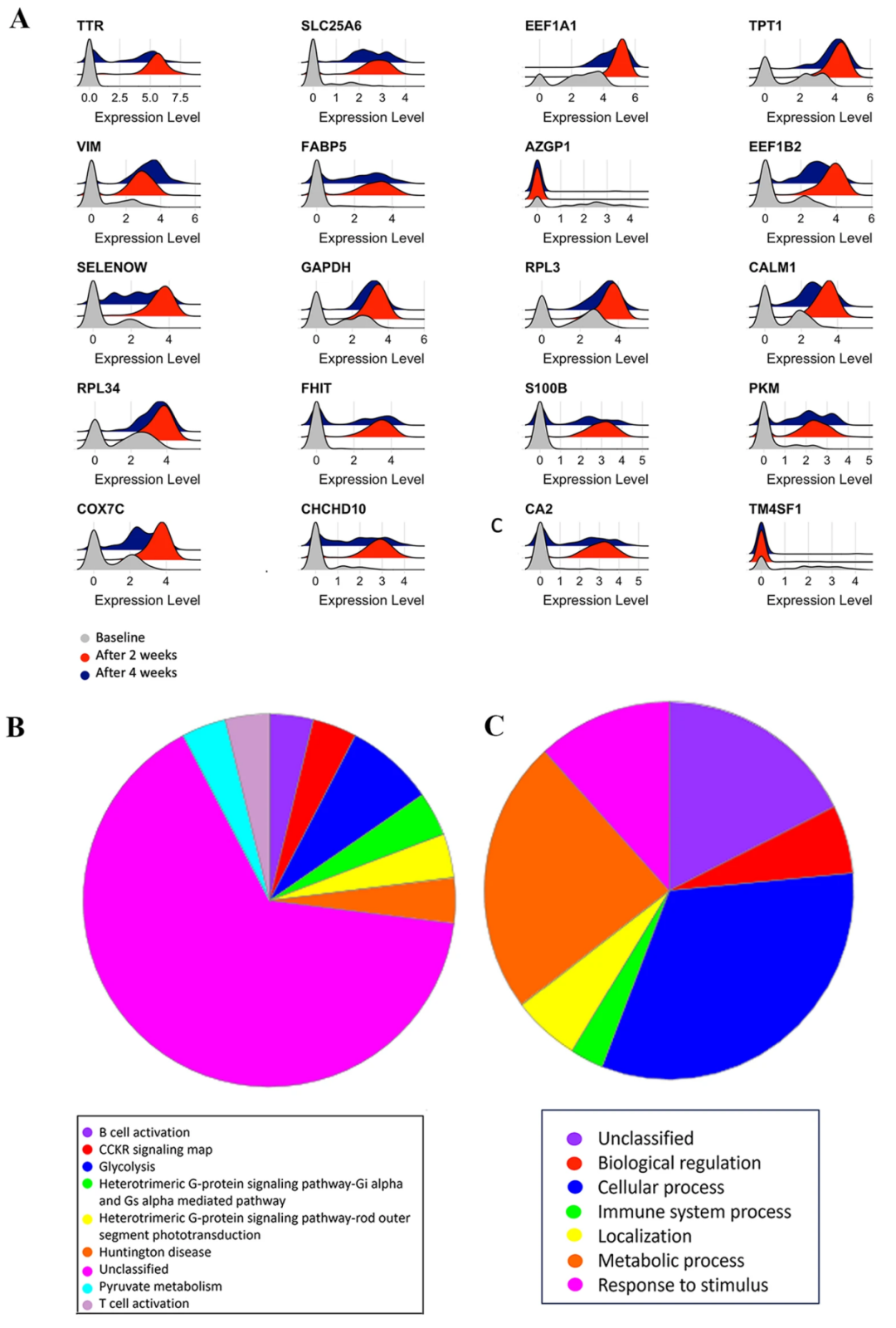
图4. 前20个差异表达基因的通路分布与生物学富集过程分析[6]
细胞因子谱分析显示,治疗后2周,患者脑脊液中IL-1β、IL-2、IL-4、IL-5、IL-6、IL-8、RANTES和表皮生长因子的水平升高(图5)。图3B展示了部分促炎细胞因子相关基因(PCP4、MORN2、FHIT)的表达分布,而图3C则显示了细胞周期相关基因(TOP2A、MKI67、CCND1、CDT1)的表达水平分布。图3D的点图呈现了三个时间点样本间的基因表达水平分布情况。单核细胞趋化蛋白-1和巨噬细胞迁移抑制因子在所有样本中均持续表达。
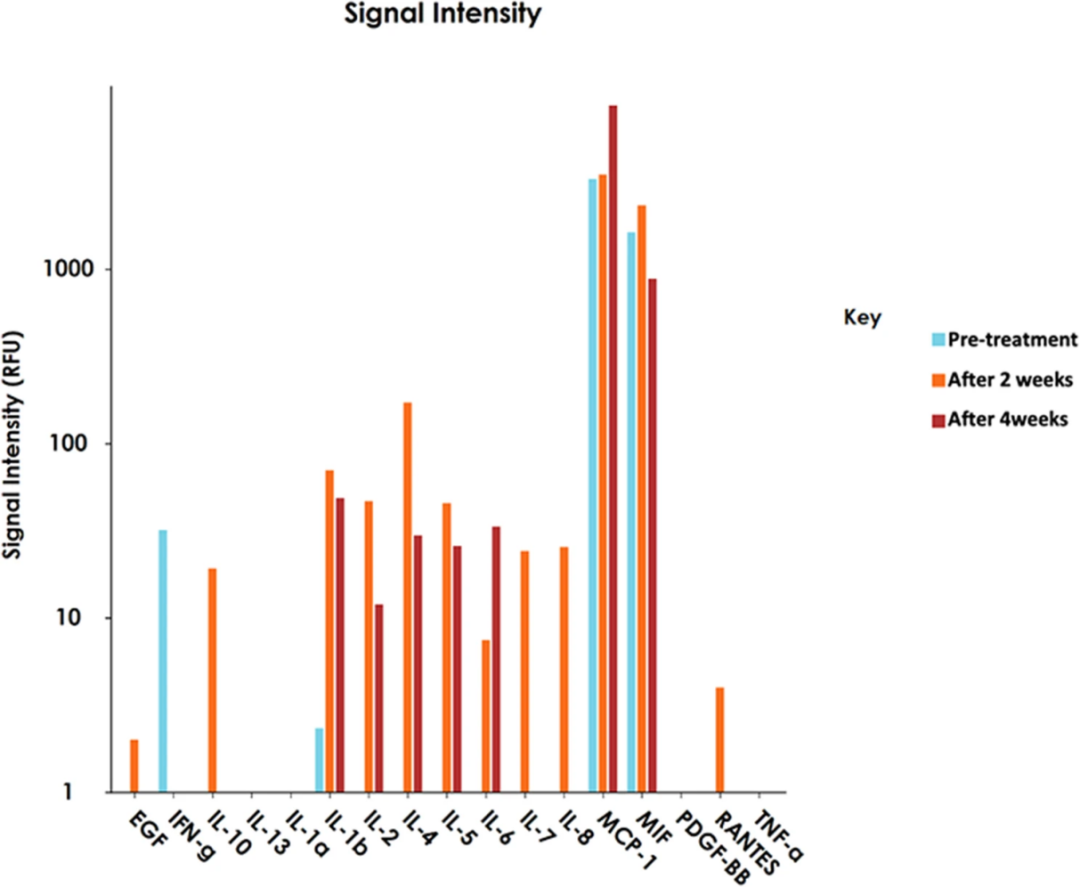
图5. 治疗前后脑脊液中炎症细胞因子浓度的动态变化[6]
本研究通过对一例HER2+乳腺癌软脑膜转移患者的系列脑脊液样本进行多模态分析,证实了整合脑脊液循环肿瘤细胞检测、单细胞RNA测序及细胞因子谱的纵向监测策略的潜在价值。研究发现,治疗后脑脊液中肿瘤细胞减少与影像学改善相符。单细胞测序动态揭示了肿瘤与免疫细胞组成的演变,并观察到与肿瘤侵袭迁移相关的TNBC特征基因表达下调。同时,研究刻画了治疗相关的炎症微环境变化,并检测到可能介导耐药的持续存在的免疫抑制因子及高增殖肿瘤细胞亚群。综上,该多模态脑脊液分析体系能为乳腺癌脑转移提供一种非侵入性的实时监测工具,在评估疗效、揭示机制及指导个体化治疗方面具有重要前景。
编辑:Citrea
审校:KIKI
排版:Ben
执行:KIKI
医脉通是专业的在线医生平台,“感知世界医学
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)