文献来源:中华炎性肠病杂志,2026年第10卷第1期
作者:中华医学会消化病学分会
通信作者:朱维铭,南京中医药大学附属医院肛肠科,炎症性肠病诊疗中心;
引用本文:中华医学会消化病学分会炎症性肠病学组,中华医学会外科学分会胃肠外科学组,中华医学会外科学分会结直肠外科学组.中国




【摘要】 随着“达标治疗”理念的推广及多学科协作模式的广泛应用,克罗恩病(CD)外科治疗的目标也从解除症状转向维持术后长期缓解、恢复功能与提升生活质量的综合管理方向转变。本指南由中华医学会消化病学分会炎症性肠病学组、中华医学会外科学分会胃肠外科学组和结直肠外科学组结合国内外最新研究成果和理念进展,对中华医学会消化病学分会炎症性肠病学组2020年发布的《炎症性肠病外科治疗专家共识》中CD及肛周CD部分进行全面系统的更新,旨在为外科决策提供科学严谨、循证充分、实践导向的参考依据。
【关键词】 克罗恩病; 外科治疗; 指南; GRADE分级; 德尔菲法
克罗恩病(Crohn′s disease,CD)是一种慢性、复发性、进展性肠道炎症性疾病,常伴狭窄、瘘管、肛周病变等并发症,严重影响患者生活质量和功能状态。尽管新型生物制剂和小分子药物等不断涌现,显著拓展了内科治疗手段,但超过70%的患者在疾病过程中仍需接受外科干预[1]。在“达标治疗”和多学科协作(multi⁃disciplinary team,MDT)理念日益深入人心的背景下,CD的外科治疗目标也从单纯解除症状转向追求术后长期缓解与生活质量提升,仅以症状改善作为外科治疗终点可能导致治疗不足[2⁃4]。
为进一步规范我国CD外科诊疗实践,提高治疗决策的科学性与规范化水平,中华医学会消化病学分会炎症性肠病学组联合相关学科专家,基于《中国克罗恩病诊治指南(2023年·广州)》[2]和最新循证医学证据,对2020年我国首部《炎症性肠病外科治疗专家共识》[5]肠道 CD 和肛周 CD(perianal Crohn′ s disease,pCD)部分进行全面修订,并依据中华医学会相关指导原则升级为指南,旨在为临床提供规范、系统、可操作的外科治疗参考依据。
一、方法
1.指南制定方法:本指南参考循证医学指南制定原则,遵循中华医学会《中国制订/修订临床诊疗指南的指导原则(2022版)》确立的规范化流程与方法论框架、指南研究与评价工具(appraisal of guidelines for research and evaluation,AGREEⅡ)的科学评估标准及卫生保健实践指南报告条目(reporting items for practice guidelines in healthcare,RIGHT)的规范化报告要求。制定过程中参考了证据评级与推荐分级 、制 定 和 评 价(grading of recommendations,assessment,development and evaluation,GRADE)的理念和原则。
2.指南使用者和目标人群:本指南的目标用户是从事炎症性肠病(inflammatory bowel disease,IBD)诊疗工作的临床医务工作者,其推荐意见的目标适用人群为中国CD患者。
3.指南专家组构成:指南专家组包括临床专家组、方法学组和秘书组。主要的临床专家由中华医学会消化病学分会炎症性肠病学组、中华医学会外科学分会胃肠外科学组和中华医学会外科学分会结直肠外科学组具有丰富胃肠外科或IBD治疗经验和学术影响力的医生组成,秘书组由中华医学会消化病学分会炎症性肠病学组外科俱乐部部分成员组成,方法学组由宁波诺丁汉大学GRADE中心专家组成。本指南已在国际实践指南注册 与 透 明 化 平 台(Practice guideline REgistration for TransPAREncy,PREPARE)注 册(PREPARE⁃2024CN1178)。
4.利益冲突:指南专家组成员的利益冲突管理依据世界卫生组织(World Health Organization,WHO)以及国际指南联盟(Guideline International Network,GIN)对利益冲突管理的指导原则执行。指南专家组向中华医学会报告了个人潜在的利益冲突(包含财务和专业相关的利益冲突)。所有成员均无利益冲突。
5.临床问题的遴选和确定:方法学团队与临床专家通过4次线下专家会议对肠道CD和pCD相关的临床问题进行讨论,经过对最初临床问题的多轮修改和讨论,最终确定了在本指南中要明确的32个临床问题。
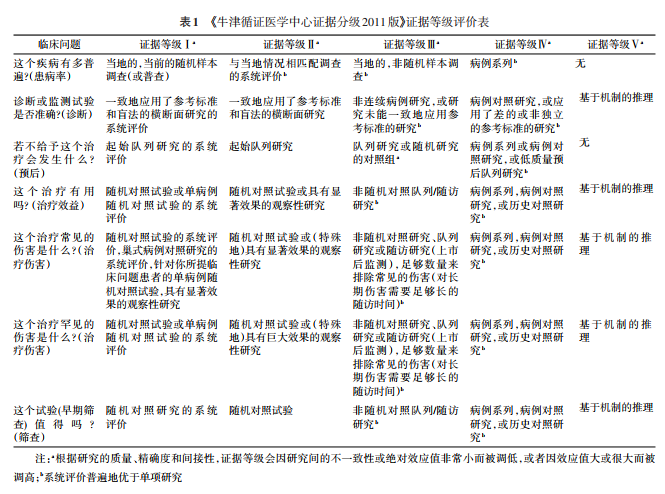
6.证据检索、分级和推荐意见形成:指南专家组在万方、维普、中国知网、PubMed、Embase、Cochrane Library数据库实施了证据检索。文献纳入标准:(1)研究对象:CD患者,年龄不限定;(2)研究类型:随机对照研究或观察性研究、荟萃分析、系统评价和先前的指南;文献排除标准:(1)重复发表的研究;(2)非中英文语言的研究;(3)综述类无具体数据的研究。文献筛选由两名指南专家组成员依据上述纳入及排除标准进行独立筛查,先根据题目和摘要进行初步纳排,进一步根据全文内容,最终确定纳入文献,并提取研究信息。对于存在争议的文献,通过讨论或咨询第三方最终达成共识。针对纳入研究,采用《牛津循证医学中心分级2011版》(OCEBM levels of evidence)[6]来具体执行证据质量评价和分级(表1),综合考虑纳入研究的质量、研究间不一致性、精确度、间接性等对证据质量评级进行调整。在形成推荐意见时参考了 GRADE 证据到决策(evidence to decision)的理念,结合证据质量将推荐强度分为强和弱两个等级(表2)。强推荐代表指南临床专家组对该推荐意见为最佳临床实践有很高的信心,建议目标用户均采纳该推荐意见。弱推荐代表指南临床专家组对该推荐意见的信心有限,应有条件地应用于目标群体,强调医患共同决策。此外,针对那些专家组认为重要,但不宜用证据级别和推荐强度表达的内容,则采用最佳临床实践(best practice statement,BPS)来表达。专家组对研究证据公开讨论后,采用德尔菲问卷调研法结合专家会议法来达成对推荐意见的共识。本指南中的推荐意见或 BPS 在专家组投票后,共识率达到 80% 视为达成共识。

7.指南传播和实施:指南的有效传播与落地实施依赖于系统化、多维度的协同努力。本指南发布后,指南工作组将主要通过以下方式对指南进行传播和推广:(1)通过权威医学期刊发表指南全文及摘要、在国家级/区域性学术会议上进行专题解读与推广;(2)利用专业学会网站、医学数据库、移动医疗APP、社交媒体精准推送指南核心推荐意见与解读材料;(3)由医院/科室组织指南培训会,确保临床医师及其他相关专业群体充分了解并正确应用该指南。
二、肠道CD
(一)手术指征
推荐意见1:对于药物治疗无效的CD相关肠道并发症,建议手术治疗。(证据等级:Ⅲ,推荐强度:强推荐)
推荐理由:CD常见的肠道并发症包括狭窄型CD导致的
早期应用生物制剂可有效控制CD炎症,延缓疾病进展,降低手术率。而在已形成纤维性狭窄的疾病进展期,药物治疗效果有限。多中心研究显示,确诊2年内启动抗肿瘤坏死因子(tumor necrosis factor,TNF)⁃α单克隆抗体(以下简称单抗)治疗的患者手术率显著低于诊断 2 ~ 5 年内启动治疗(5.7% 比 24.5%,P = 0.008)及 5 年 后 启 动 治 疗(5.7% 比30.6%,P < 0.001),但在确诊5年内与5年后、10年内与10年后启动治疗者之间手术率差异无统计学意义[7]。
目前尚无确切证据支持任何药物可显著逆转CD纤维性狭窄,使用抗TNF⁃α单抗治疗虽然可能延缓手术时间,但整体疗效仍然有限。一项单中心随机对照研究(STRIDENT研究)纳入77例伴有肠梗阻症状的狭窄型CD患者,强化治疗组52例(
对于无症状的肠内瘘,若瘘口较小,可在充分评估后使用生物制剂等药物争取瘘口闭合。一项纳入93例CD患者的多中心研究显示,抗TNF⁃α单抗治疗5年后瘘口总闭合率仅为29%,其中肠内瘘23.6%(17/72)、肠膀胱瘘56.3%(9/16)、肠阴道瘘20%(1/5),累积闭合率随时间增加,1年、2年、3年、5年和10年的累计闭合率分别为15.5%、18.1%、21.5%、27.0%和42.2%,瘘口数量是影响闭合率的独立危险因素(OR = 0.25,95%CI:0.06 ~ 0.99,P = 0.049)[9]。
对于有症状或药物治疗不能使瘘口完全闭合的CD肠瘘患者,应尽早手术干预。一项回顾性研究纳入并分析126例具有完整临床资料的CD肠瘘患者,47%于1年内接受手术,影像学特征分析显示,多发瘘(P = 0.009)、合并肠狭窄(P = 0.02)和肠膀胱瘘(P = 0.01)均显著增加手术风险,多因素分析发现合并肠狭窄是 CD 肠瘘患者需手术治疗的独立危险因(RR = 4.5,95%CI:1.23 ~ 16.3,P = 0.02)[10]。
推荐意见 2:对药物治疗效果不佳的孤立、短段的末端回肠和(或)回盲部病灶,推荐行病变肠段切除。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:孤立、短段的末端回肠和(或)回盲部病灶(包括蒙特利尔分型为非狭窄非穿透型、狭窄型、穿透型)是CD常见表现。若药物治疗(包括传统药物如
一项针对活动期非狭窄非穿透型孤立性末端回肠CD患者(病变长度≤40 cm)的多中心、开放标签、随机对照试验(LIR!C研究),比较73例早期
推荐意见3:药物和营养治疗不能控制疾病活动或生长发育受到影响的儿童和青少年CD患者,推荐手术切除病变肠管。(证据等级:Ⅲ,推荐强度:弱推荐)
推荐理由:慢性活动性炎症和
CD患儿除承受疾病本身的影响外,还面临生长和
推荐意见4:确诊CD相关肠道癌变的患者,推荐遵循肿瘤学外科原则实施手术;对于临床高度怀疑肠道癌变但难以获得病理学证据的病灶,推荐手术切除病变肠段以避免漏诊风险。(证据等级:Ⅱ~Ⅳ,推荐强度:强推荐)
推荐理由:CD患者癌变风险显著升高,以小肠癌和
CD 患者的胃肠道肿瘤风险显著升高。一项汇总 24 项Meta分析的伞状系统评价显示,CD患者发生小肠癌的风险升高约12倍(RR = 11.9,95%CI:8.07 ~ 17.7),儿童期发病者高达40倍(RR = 40.4,95% CI:4.52 ~ 362);结直肠癌风险亦显著升高(RR = 1.54,95%CI:1.28 ~ 1.86),儿童发病者风险更高(RR = 6.29,95%CI:3.73 ~ 10.6);不同部位病灶的癌变风险存在差异,
队列研究显示,CD 患者结肠狭窄发生率约为 13.5%(132/980),其中6.8%(9/132)的狭窄伴隐匿性癌变,而无狭窄患者仅为0.7%(6/848,P < 0.001)[22]。CD良恶性病变在临床表现或影像学上难以准确区分,Singh 等[23]报告 3 例术前影像和内镜未发现恶变、但术后确诊为小肠腺癌的CD狭窄病例。因此,对具备手术指征的慢性病灶,尤其是临床高度怀疑肿瘤但现有检查无法获得明确病理诊断者,建议手术切除病变肠段以避免肿瘤漏诊。
外科治疗需遵循肿瘤学原则,并充分考虑炎症范围、肿瘤部位与全身情况制定个体化方案。一项纳入 366 例 CD⁃CRC患者的研究显示,节段性结肠切除是最常采用的手术方式(68%),其5年生存率(56.2%)与全结肠切除术(61.3%)及全结肠⁃直肠切除术(59.0%)相比无显著差异(P = 0.66)[24]。一项纳入 189 例 IBD 合并进展期肿瘤患者的多中心队列研究,分析不同肠切除方式的异时性肿瘤发生率,结果显示,异时性肿瘤每百人年发生率在节段性结肠切除组为11.5、全结肠切除组为6.1,但差异无显著性,而在内镜切除组为13.7,显著高于全结肠切除组(asHR = 5.79,95%CI:1.62 ~ 20.70,P < 0.01)[25]。
推荐意见5:CD合并游离肠穿孔、绞窄性肠梗阻等急腹症,或非手术治疗无效的消化道大出血,推荐急诊手术。(证据等级:Ⅱ~Ⅲ,推荐强度:强推荐)
推荐理由:游离肠穿孔伴弥漫性
CD 肠穿孔多发生在肠系膜侧。一项研究回顾 1935 年至2021年间19份病例报告(43例CD患者,75处肠穿孔),结果显示穿孔部位主要在回肠(74.6%,56/75),其次是空肠(20%,15/75)和盲肠(2.7%,2/75),空肠穿孔病死率(11/15,P = 0.028)显著高于其他部位[26]。虽然CD急诊手术的术后病死率显著高于择期手术(3.6%比0.6%)[27],但与保守治疗患者的病死率(100%,5/5)相比,急诊手术是降低CD肠穿孔病死率的关键措施(15.8%,6/38,P < 0.001)[26]。部分CD 慢性肠狭窄可迅速进展为急性肠梗阻,对于梗阻症状严重或穿孔高风险患者,在明确手术指征后推荐尽早外科干预,延误手术时机可能导致肠管坏死、穿孔或需要广泛肠切除,影响患者预后[28]。
CD相关消化道大出血少见,出血病灶多为活动性溃疡,常见于病变最严重区域或左侧结肠,非手术治疗应作为首选策略。一项纳入34例患者的多中心研究显示,80%的首次CD相关出血可通过药物、内镜或介入治疗成功止血[29]。若内镜不能明确定位,可联合
(二)术前评估与围手术期处理
推荐意见6:对拟手术的CD患者,推荐常规进行术前全面评估,识别、并通过有针对性的预康复消除手术并发症危险因素后进行择期手术,以提高手术安全性和远期疗效。尽量避免急诊手术或没有进行充分术前评估与预康复的手术。(证据等级:Ⅱ~Ⅲ,推荐强度:强推荐)
推荐理由:需要手术的CD患者常合并营养不良、免疫力下降、合并感染和药物不能控制的活动性炎症等手术并发症危险因素,术前评估是筛查上述危险因素的关键环节。预康复通过改善患者营养状况、提高患者抗感染能力、清除感染灶、降低身体炎症负荷、撤除影响手术康复的糖皮质激素等措施,结合手术团队对腹腔解剖结构的充分了解和精心的术前准备,能够显著提高手术成功率,降低手术并发症发生风险,改善患者长期结局与生活质量。急诊手术并发症发生风险大,复发风险高。若患者不能完成预康复就必须手术,则手术方案需要遵循“损伤控制外科”原则(见推荐意见14)。
术前全面评估是筛查手术并发症风险因素的过程。现有研究证实,手术并发症危险因素包括营养不良(如血清白蛋白<35>8 mg/L)、使用糖皮质激素(如
糖皮质激素(连续使用≥20 mg/d泼尼松或等效剂量其他糖皮质激素>6周)应至少在术前4周停用或减量至免疫抑制阈值(泼尼松≤10 mg/d)以下,全肠内营养(exclusive enteral nutrition,EEN)有助于患者摆脱糖皮质激素[36]。术前使用生物制剂并未增加术后总体并发症风险,但小分子药物的围手术期安全性缺乏临床研究数据。GETECCU 研究纳入1 238例CD患者,其中46.3%术前接受生物制剂治疗,多变量分析显示,抗TNF⁃α单抗(P = 0.21)、维得利珠单抗(P = 0.17)和乌司奴单抗(P = 0.52)均与术后总体或腹腔感染性并发症不相关[37]。
腹盆腔或腹膜外脓肿是 CD 常见的并发症,发生率为10%~30%,一旦发现,应积极干预[38]。初始治疗采用口服抗生素联合EEN,对于直径≥30 mm的脓肿首选经皮置管冲洗引流,若不适合置管(难以置管、脓腔呈多腔隙、脓肿邻近重要脏器或血管等)或引流失败,则推荐手术引流。一项纳入508 例患者的多中心研究显示,抗生素联合 EEN、经皮置管引流及手术引流的感染缓解率分别为60%、53%和81%,脓肿大小是选择治疗方式的关键因素,对于直径<30 mm的脓肿,采用抗生素治疗、置管引流或手术引流效果相当;对中等(30~50 mm)或大脓肿(>50 mm),手术引流疗效显著优于其他方案(中等脓肿手术比抗生素:OR=7.8,95%CI:3.41 ~19.80;大脓肿手术比经皮引流:OR=6.63,95%CI:2.15 ~25.26),但手术并发症显著高于经皮置管引流(29% 比9.9%)[39]。合并肠瘘是经皮置管引流失败的主要危险因素,当脓肿合并持续性高引流量(>50 mL/d)时,应行瘘管造影或增强CT/MRI,了解脓肿与肠管的关系[40]。多数患者通过经皮引流能够有效控制感染,显著提高一期肠切除吻合术的安全性,手术并发症(20%比69%,P = 0.036)与造口率(10%比69%,P = 0.01)显著降低[41]。
对于有营养风险或营养不良的患者,干预措施以营养治疗为核心,推荐EEN至少6~8周,以改善营养状态、诱导活动性CD缓解(具体实施方案参见《炎症性肠病营养治疗专家共识(第三版)》[36]推荐意见8)。对于存在肠腔狭窄或高位瘘等限制实施EEN的患者,可通过内镜扩张、放置鼻肠管或内镜下胃/空肠造口等方式建立肠内营养(enteral nutrition,EN)通道,EN达不到全量者,营养不足部分可以通过肠外营养(parenteral nutrition,PN)补充。一项纳入120例患者的研究显示,与未接受EEN的患者相比,在接受腹腔镜切除的CD患者中,术前实施至少4周EEN,可显著降低术后并发症发生率(17.8%比36.0%,P = 0.033),并减少术后6个月内镜复发率(11.9%比28.4%,P = 0.044)[42]。
预康复目标是将高风险患者转化为适合手术的低风险状态。预康复的终点包括营养状况正常、全身炎症显著消退、糖皮质激素减停或降至安全剂量、影像提示不合并腹腔脓肿或复杂瘘道、局部解剖结构相对清晰[35]。达到上述条件后实施择期手术,可显著提升手术安全性和疗效。多项回顾性研究显示,择期手术较急诊手术可显著降低术后并发症、中转开腹率、再手术率和远期吻合口复发风险[43⁃45]。一项纳入22项研究的随机效应荟萃分析显示,与择期手术(6 518例)相比,急诊手术(955 例)的总体并发症风险增加约 43%(RR = 1.43,95%CI:1.09 ~ 1.87,P = 0.010),腹腔感染性并发症的发生率显著升高(RR = 1.44,95%CI:1.08 ~ 1.92,P = 0.013)[46]。一项荟萃分析纳入75 971例CD患者显示,CD患者择期手术的死亡率远低于急诊手术(0.6% 比 3.6%)[27]。
推荐意见7:对合并肠梗阻的CD患者,推荐通过肠道减压等措施缓解梗阻症状,以实现预康复目标。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:对于合并肠梗阻的CD患者,推荐采用肠道减压(如经鼻肠梗阻导管或经肛导管)替代传统鼻胃管减压,以有效缓解梗阻症状、减轻肠壁水肿、恢复肠道通畅。梗阻缓解后及时启动以EN为主的营养治疗策略,争取改善营养状况,缓解活动性炎症,实现预康复目标。
人群队列研究显示,在确诊CD后10年内,超过50% CD患者将发展为狭窄或穿透型,其中 24% ~ 40% 患者因肠梗阻需接受手术治疗[47⁃48]。经内镜辅助置入肠梗阻导管较鼻胃管能够更有效地缓解 CD 相关肠梗阻症状。前瞻性队列研究纳入27例经鼻肠梗阻导管组和42例鼻胃管组患者,结果显示,经鼻肠梗阻导管组在避免急诊手术(21.4% 比44.4%,P = 0.043)、降低临时造口率(20.0% 比 54.5%,P =0.032)、术后切口感染率(6.7%比36.4%,P = 0.04)均显著低于鼻胃管组,术后 1 年内的再梗阻率亦显著低于鼻胃管组(8.3% 比55.5%,P = 0.046)[49]。一项针对CD 合并炎症性狭窄的前瞻性研究显示,肠道减压后,81.4%(48/59)患者肠梗阻症状缓解,64.6%(42/59)达到临床缓解,84.7%(50/59)完成12周 EEN治疗[50]。系统评价表明,经过12周 EEN治疗的CD 纤维性狭窄患者,60%~71% 实现肠梗阻症状缓解,53.8%~59.3%达到影像学缓解,完全缓解率46.1%[51]。
推荐意见8:择期手术的CD患者,推荐遵循加速康复外科理念。(证据等级:Ⅱ~Ⅳ,推荐强度:弱推荐)
推荐理由:基于循证医学的加速康复外科(enhanced recovery after surgery,ERAS)理念核心是通过减少治疗措施和不必要的干预造成的身体应激反应以及对康复过程的不利影响,以达到促进患者早日康复、减少手术并发症、改善手术结局的目的。这一理念同样适用于IBD手术患者。
前瞻性研究显示,遵循 ERAS 路径的腹腔镜 CD 回盲部切除术能够加快胃肠功能恢复,缩短住院时间,并且未增加术后并发症或再入院风险[52⁃53]。一项纳入977例因IBD接受结直肠切除术的研究显示,实施 ERAS 组手术切口感染率(5.5% 比 14.7%,P = 0.003)、肠麻痹发生率(8.9% 比 20.1%,P<0.001)以及吻合口漏发生率(0比4.7%,P = 0.01)显著低于未实施ERAS组[54]。一项纳入16项研究共2 347例IBD患者的系统综述证实,ERAS显著改善了手术患者短期预后,中位住院时间缩短至5.2 d,手术部位感染率降至3.1% ~ 23.5%,吻合口瘘发生率低至0 ~ 3.4%,总体并发症发生率为5.7% ~48%,死亡率未超过1.0%[55]。
预防静脉血栓栓塞症(venous thromboembolism,VTE)是ERAS的重要内容之一。IBD患者常伴有VTE的危险因素,建议术前进行风险评估,高风险患者给予抗凝治疗。一项纳入10 431例IBD手术患者的研究显示,术后30 d内VTE总体发生率2.3%,其中CD患者发生率为1.4%,平均发生时间为术后10.8 d[56]。另一项涉及7 078例IBD手术患者的研究表明,出院后 VTE 的总体发生率高达 3.3%,但仅 42 例(0.6%)患者出院后接受VTE预防,延长VTE预防至2 ~ 3周能有效降低 VTE 的发生率[57]。因此建议对具有 VTE 危险因素(年龄 > 65岁、长期使用糖皮质激素、BMI > 30 kg/m2、美国麻醉医师协会分级 ≥ 3级和营养不良)的患者术后实施至少2周预防血栓措施[58]。
(三)手术方式
推荐意见9:对于无明确禁忌证的CD患者,推荐采用腹腔镜等微创手术方式。(证据等级:Ⅲ,推荐强度:强推荐)
推荐理由:腹腔镜等微创技术较传统开腹手术具有创伤小、并发症少、术后恢复快、住院时间短等优势。即使复杂或复发性CD手术,采用微创技术亦具有良好的安全性与可行性,除非患者存在不能耐受气腹等明确禁忌证。
一项基于美国全国住院样本数据库(2000—2004年)的研究共纳入49 609例接受回盲部或结肠切除的CD患者,结果显示,腹腔镜手术在手术并发症(8% 比 16%)、住院时间(6 d比9 d)、住院费用(27 575美元比38 713美元)及围手术期死亡率(0.2% 比 0.9%)方面均显著优于开放手术(P 均<0.01)[59]。基于倾向性评分匹配的回顾性研究显示,腹腔镜 手 术 总 并 发 症 发 生 率 显 著 低 于 开 放 手 术(13.7% 比32.4%,P=0.003),感染性并发症(1.0%比14.7%,P<0.001)、吻合口漏发生率(0.0% 比 6.9%,P=0.014)和再手术率(0.0%比5.9%,P=0.029)均显著减少,但5、10年无复发生存率无显著差异[60]。
腹腔镜技术在复杂及复发性CD手术中也体现出可接受的安全性和可行性。回顾性研究显示,与初次手术相比,对再手术患者实施腹腔镜手术尽管手术时间更长(125 min 比85 min,P<0.001),但术后进食时间、住院时间、手术并发症和再入院率与初次手术组无显著差异[61]。一项纳入124例复杂CD(合并瘘管、脓肿和复发病例)患者的前瞻性研究显示,尽管手术时间[(214 ± 73 )min 比(191 ± 53)min,P<0.05]、中转开腹率(37%比14%,P<0.01)和临时造口率(39%比9%,P<0.001)显著高于非复杂CD,但术后并发症、住院时间和再手术率与非复杂CD相当[62]。一项纳入301例腹腔镜手术的回顾性研究证实,65例(21.6%)中转开腹手术的主要原因为致密粘连(34%)、瘘管合并盆腔感染(26%)、炎性包块(18%)、肠系膜增厚(9%)和病变范围广(7%)[63]。
推荐意见10:对于病变范围局限的小肠病变,首选病变肠段切除;多节段、长段小肠病变或既往多次肠切除、剩余小肠长度有限的患者,推荐综合采用肠切除与狭窄成形术,以降低短肠综合征风险。小肠或回结肠吻合推荐采用吻合器侧侧吻合术。(证据等级:Ⅱ~Ⅲ,推荐强度:强推荐)
推荐理由:CD术式选择在追求达标治疗的基础上要兼顾肠管保留原则。对于病变范围局限的小肠狭窄、穿透性病变、消化道出血或有癌变风险的病灶,首选病变肠段切除术;病变范围广泛(>100cm)、多节段受累、术后复发性CD或剩余肠管有限的小肠CD,需要综合应用病灶切除与狭窄成形术,以降低短肠综合征风险。研究显示,侧侧吻合术较端端吻合术或端侧吻合术在降低术后并发症、复发率和再手术率方面表现更优。
肠切除术在控制术后复发方面具有显著优势,并未增加不良事件风险。一项纳入7项研究688例小肠受累CD患者的荟萃分析,比较了肠切除术和狭窄成形术的疗效,结果显示短期总并发症(12.7%比19.1%,P = 0.13)和复发率(37.8%比 31.0%,P = 0.09)差异无统计学意义,但肠切除术后无复发时间长于狭窄成形术(HR = 1.08,95%CI:1.02 ~ 1.15,P =0.01)[64]。另一项纳入12项研究1 026例CD肠纤维化狭窄患者的荟萃分析进一步证实,与狭窄成形术相比,肠切除术的总复发率(25.8%比35.3%,OR = 1.57,95%CI:1.02 ~ 2.42,P =0.04)和再手术率(29.4%比39.7%,OR = 1.62,95%CI:1.19 ~2.19,P = 0.002)更低,术后无复发时间更长(HR = 1.47,95%CI:1.08 ~ 2.01,P = 0.02),两者的安全性指标无显著差异[65]。
一项纳入87例广泛末端回肠受累(≥20 cm)的CD 患者的单中心回顾性研究显示,狭窄成形术在术后并发症指数(8.5分比9.1分,P = 0.48)、术后复发率(12.5%比17.0%,P =0.393)及深度缓解率(22.5% 比 41%,P = 0.34)等方面与肠切除术相当,说明狭窄成形术是一种安全、有效、可保留肠管的手术策略[66]。另一项回顾性研究纳入110例空肠受累CD患者,结果显示肠切除术、狭窄成形术与二者联合手术三组患者在手术并发症(P = 0.72)与复发率(P = 0.24)方面差异无统计学意义,狭窄成形术或联合术式在保留肠管长度的同时未增加术后复发风险[67]。
肠吻合方式是影响术后复发和长期结局的重要因素。一项荟萃分析纳入8项研究(包括3项随机对照试验)共821例接受回结肠切除术的CD患者,结果显示吻合器侧侧吻合术可显著降低CD术后吻合口漏发生率(OR = 0.45)、吻合口复发率(OR = 0.20)和再手术率(OR = 0.18)[68]。另一项系统综述也显示,与手缝端端吻合术相比,吻合器侧侧吻合术在减少吻合口漏(OR = 0.45,P = 0.05)、总体并发症(OR = 0.54,P = 0.03)发生率、吻合口复发率(OR = 0.20,95%CI:0.07 ~0.55,P = 0.002)和再手术率(OR = 0.18,95%CI:0.07 ~ 0.45,P = 0.000 2)方面具有显著优势[69]。
推荐意见 11:CD 合并肠内瘘手术时,推荐切除原发病灶。受累器官根据具体情况选择修补或切除等治疗方案。(证据等级:Ⅲ,推荐强度:弱推荐)
推荐理由:肠内瘘是CD穿透性病灶侵犯邻近肠管或脏器所致,常见类型包括肠⁃肠瘘、肠⁃膀胱瘘及肠⁃阴道瘘。外科治疗的关键是切除原发病灶,并依据受累部位瘘口解剖特征、组织条件及功能保留需求实施相应治疗,若受累器官瘘口较小、周围组织相对健康,可进行修补;若瘘口较大或周围组织受累严重,应将受累部位局部切除。
一项纳入 54 例瘘管型 CD 患者的回顾性分析发现,肠⁃肠瘘最常见(53.7%),其次为肠⁃皮瘘(35.2%)、肠⁃膀胱瘘(7.4%)和直肠⁃阴道瘘(3.7%),其中,96.8%有症状肠瘘患者接受手术治疗,主要术式为病变肠段切除和受累部位修补术[70]。一项纳入90例回肠⁃乙状结肠瘘CD患者的回顾性研究显示,瘘口修补组(47.8%)与切除组(35.6%)在术后并发症发生率方面差异无统计学意义(7.1%比15.6%,P = 0.28),但修补组由于受累器官病变较轻,所以平均住院时间更短(8.3 d比9.9 d,P = 0.015)[71]。对于回结肠十二指肠瘘,在充分预康复的基础上将回结肠原发病灶切除加原位十二指肠修补的成功率可达97%(33/34)[72]。瘘口无法修补时可采用十二指肠旷置加胃空肠吻合术[73]。针对肠⁃膀胱瘘,一项回顾性研究纳入74例CD患者,发现46例(62.2%)患者仅切除原发病变肠管,28例(37.8%)切除原发病变肠管联合膀胱修补术,手术成功率95.95%,术后复发率为4.05%[74]。相比之下,直肠⁃阴道瘘的治疗更具挑战性,应遵循个体化原则,以诱导疾病缓解和控制临床症状为核心(详见推荐意见29)。
推荐意见 12:CD 小肠切除推荐遵循节约肠管的原则,以肉眼无病变部位作为肠管切缘,扩大肠切除范围不能降低术后复发率。对于术中发现无症状的狭窄或非穿透性肠道炎症病变,首选术后积极药物治疗。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:CD具有节段性、跳跃性分布和复发倾向,手术切除并非治愈手段,扩大切除范围不能减少术后复发,反而增加短肠综合征发生风险。因此,遵照节约肠管的原则,推荐以肉眼无病变部位为切缘;对无症状狭窄或非穿透性炎症病变,不推荐术中一并切除,建议术后通过药物治疗控制病情。
切缘肌间神经丛炎、神经胶质细胞增生、肠系膜淋巴管密度升高及镜下炎症等病理特征均与 CD 术后复发显著相关,微观切缘炎症状态在术后复发预测中具有重要意义[75⁃77]。一项系统综述与荟萃分析发现,切缘组织学阳性与术后总体复发率(OR = 1.7,95%CI :1.3 ~ 2.1,P < 0.001)、临床复发率(OR = 1.7,95%CI:1.0 ~ 2.8,P = 0.04)和吻合口复发率(OR =1.6,95%CI:1.0 ~ 2.3,P = 0.03)显著相关[78]。但随机对照试验发现,广泛肠管切除(距病变边缘12 cm)与限制性肠管切除(距病变边缘 2 cm)的临床复发率(28.6% 比33.3%,P = 0.56)、手术复发率(17.9% 比 25.3%,P = 0.31)和累积复发率(P = 0.38)差异无统计学意义,表明广泛肠管切除不能降低术后疾病复发[79]。
节段性、跳跃性分布是CD的特征。在一项纳入404例CD回结肠切除患者的回顾性研究中,202例(50%)合并小肠病变,其中108例同时进行小肠病灶手术,94例未作处理,结果显示,合并小肠病变是CD再手术的危险因素(P = 0.041);亚组分析表明,对于术中未处理的小肠病变,术后给予抗TNF⁃α 单抗治疗,其再手术率与无小肠病变患者相当(P =0.605),术后抗TNF⁃α单抗治疗可逆转残留小肠病变的不良影响(HR = 0.20,95% CI:0.04 ~ 0.90,P = 0.040)[80]。另一项回顾性研究显示,对于需要手术的CD多节段病灶患者(中位随访65个月),切除主要病灶、术后采用生物制剂控制术中残留病灶,术后 6~12 个月临床缓解率 59%,24 个月达到71%,仅20%(6例)患者因出现肠梗阻症状需要再次手术[81]。
推荐意见 13:广泛肠系膜切除和对系膜缘吻合降低术后复发的临床证据尚不充分,建议根据术者经验及患者情况酌情选择。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:广泛肠系膜切除术和对系膜缘吻合术(Kono⁃S吻合)具有潜在的降低术后复发的趋势,但其临床研究结果尚存在争议,建议术者在充分评估患者病情及自身技术可行性基础上,权衡风险与获益后酌情采用。
广泛肠系膜切除是否降低手术复发率存在分歧。最近的一项随机对照试验显示,与限制性肠系膜切除组相比,广泛肠系膜切除显著降低回结肠切除术后内镜复发率(23.8%比46.5%,P = 0.03),且术中和术后短期并发症、住院时间等无显著差异[82]。然而,另一项随机对照试验(randomized controlled trial,RCT)显示,广泛肠系膜切除组术后6个月内镜复发率(42% 比43%,P = 1.0)、吻合口瘘率(8%比2%,P = 0.208)及术后药物维持治疗率(52%比52%,P = 1.0)等方面与限制性肠系膜切除无明显差异[83]。
Kono⁃S吻合术的要点是将肠吻合口建立在肠管的对系膜侧以避开肠系膜组织对吻合口炎症的影响。随机对照试验显示,Kono⁃S吻合术在术后6个月和18个月的肠吻合口内镜复发率分别为22.2%与25%,显著低于传统侧侧吻合术的62.8% 与 67.4%(P<0.001)。在临床复发方面,Kono⁃S 吻合术的复发率在术后12个月为8.0%(对照组11.1%,P = 0.20),24 个月为 18.0%(对照组 30.2%,P = 0.04)[84]。荟萃分析显示,Kono⁃S 吻合术后 6 个月及以上肠吻合口内镜复发率显著低于传统吻合术(24.7%比42.6%)[85]。然而,最近的一项多中心回顾性研究结果表明,经倾向性评分匹配后,Kono⁃S吻合术与传统吻合术在术后吻合口瘘发生率(1.6%比2.5%,P = 1)、6 个月肠吻合口内镜复发率(47.5% 比 44.3%,P =0.674)及临床复发率(16.1% 比 16.0%,P = 1)方面均无显著差异[86]。
推荐意见14:对预康复不能达标、手术并发症危险因素没有消除的CD手术患者,推荐综合考虑患者全身及腹部状况,采用肠造口术以减少吻合口相关并发症。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:对拟手术的CD患者,如果合并手术并发症风险因素,推荐进行有针对性的预康复(见推荐意见6)。如果因为某些原因无法完成预康复,或需要急诊手术时,推荐行病变肠段切除加肠造口术,避免肠吻合,以减少肠吻合相关并发症和再手术率。
系统综述与荟萃分析显示,CD患者肠吻合术后吻合口并发症的发生率为 3%~13%,吻合口漏相关病死率高达12.9%,吻合口漏的危险因素包括术前体质量下降>5% ~10%、血清白蛋白<3.0 mg/dL、腹腔脓肿、急诊手术、既往手术史和糖皮质激素使用>4周[87]。一项多中心回顾性研究中,92%(4 172/4 537)的 CD 手术患者接受一期吻合,8%(365/4 537)接受一期吻合术联合保护性回肠造口,吻合口漏发生率分别为4.5%和2.7%(P = 0.12),多因素分析显示未行肠造口是吻合口漏的独立危险因素(OR = 0.4,95%CI:0.20 ~0.77,P = 0.006),存在≥3个危险因素的高危患者行保护性肠造口可显著减少吻合口漏(8.2%比3.7%,P = 0.03),倾向评分匹配显示,肠造口术将吻合口漏发生风险降低55%(P = 0.005)[88]。另一项回顾性研究比较了CD病变肠段切除+远近端外置造口,与切除病变肠段行肠吻合的同时做保护性肠造口患者的术后结局,发现肠切除后远近端外置造口显著降低了术后30 d内的总手术并发症发生率(30.2%比51.4%,P = 0.028)及肠吻合相关不良事件(2.3%比37.1%,P < 0.001),提示肠切除后直接将远近端外置造口较肠吻合后进行保护性造口具有更好的安全性[89]。
推荐意见15:术后有造口高排量风险的CD手术患者,推荐在肠造口的同时建立肠液回输途径。术后管饲肠内营养有助于肠液回输。(证据等级:Ⅲ,推荐强度:弱推荐)
推荐理由:高位小肠造口术后常发生造口高排量,导致水电解质紊乱、营养不良和肾功能损伤。肠液回输能减少体液、电解质及胆盐丢失,减少或避免静脉输液,维持内环境稳定和营养状态,降低转流性肠炎及造口还纳术后肠麻痹等并发症的发生率。管饲肠内营养不仅便于肠液回输,还能改善机体营养状态,促进肠功能恢复。
造口高排量不仅增加患者对静脉输液的依赖,还可能导致低蛋白血症、酸碱失衡及肾功能损伤[90]。前瞻性队列研究显示,实施肠液回输后较实施前显著减少造口液丢失[(370 ±457)mL/d比(2 444 ± 933)mL/d,P < 0.001)],改善营养状况[体质量增加 4.6 kg± 8.6%、BMI 增加 3.8 kg/m2 ± 7.7%、血浆白蛋白升高(6.2 ± 6.1)g/L],91%(126/139)的患者在(2±8)d内停用PN[91]。国内一项回顾性研究证实,与未行肠液回输者相比,肠液回输显著降低了术后肠麻痹的发生率(11.5% 比42.3%,P = 0.012),并有效缩短住院时间(6.2 d 比 7.6 d,P =0.008);多因素回归分析表明,肠液回输是术后肠麻痹(OR =0.218,P = 0.042)和住院时间延长(Coef = ⁃0.191,P = 0.019)的独立保护因素[92]。
推荐意见 16:伴有幽门或十二指肠梗阻的狭窄型 CD,若内镜治疗失败或禁忌,推荐狭窄成形手术,无法实施狭窄成形者可选择胃空肠吻合术等短路手术作为替代方案。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:幽门或十二指肠狭窄是CD少见但挑战性较大的并发症,治疗目标为缓解梗阻、改善进食受限状态。内镜下球囊扩张术(endoscopic balloon dilation,EBD)是治疗幽门或十二指肠狭窄安全有效的方法。如果EBD失败或存在禁忌,推荐通过狭窄成形手术解除梗阻,其手术相关并发症发生率低,疗效肯定。对于局部条件不适宜做狭窄成形术的患者,胃空肠吻合术等短路手术可作为替代方案。
系统回顾和荟萃分析显示,EBD适用于短段、非穿透性、无活动性溃疡的狭窄病变,技术成功率为100%,短期临床缓解率 87%,并发症仅 2.9%;然而,中位随访 23.1 个月后,70.5%患者症状复发,59.6%需要多次扩张,30.8%最终需要手术干预[93]。一项回顾性研究比较 30 例仅接受 EBD 与 18例接受手术(包括狭窄成形术12例、胃空肠吻合术6例)患者的治疗效果,结果显示,与EBD 组相比,手术组症状改善率更高(100% 比 63.33%,P = 0.003),无复发生存期更长(6.31年比 2.96 年,P = 0.01),但术后不良事件发生率高(16.67%比 0.74%,P = 0.001),初始接受EBD治疗的患者最终26.83%(11/41)需手术干预[94]。另一项回顾性研究比较了21例行胃空肠吻合术与13例行狭窄成形术治疗CD十二指肠狭窄患者的疗效,平均随访3.5年的结果显示,两组术后并发症和复发率均较低,但胃空肠吻合组有吻合口溃疡(2/21)及倾倒综合征(2/21)等并发症,提示在技术可行的前提下,狭窄成形术是首选的手术方式[95]。
推荐意见17:对结肠CD手术患者,推荐根据病变范围选择节段性结肠切除、结肠次全切除或全结肠切除术。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:节段性结肠切除术(segmental colectomy,SC)在控制术后复发方面与全结肠切除术(total colectomy,TC)相当,但手术并发症发生率、肠道功能状况和生活质量方面更具优势,适用于病变范围相对局限的患者,当病变范围广泛时,可选择结肠次全切除(subtotal colectomy,STC)或TC。
一项回顾性研究比较了SC与TC治疗局限性结肠CD的疗效,结果显示 SC 显著减少术后并发症(36.8% 比 90.9%,P = 0.002)、提高Ⅰ期肠吻合成功率(63.2%比9.1%,P = 0.001)并降低了永久性肠造口率(15.8%比54.5%,P = 0.022),两种术式的住院时间、症状缓解率和术后外科复发率无显著差异[96]。一项纳入500例SC、510例STC 和426例全结肠直肠切除(total proctocolectomy,TPC)联合末端回肠造口术三种术式治疗结肠CD的荟萃分析显示,SC与STC在术后总复发率(OR = 1.24,95%CI:0.85 ~ 1.80)和手术复发率(OR = 1.19,95%CI:0.81 ~ 1.74)方面差异无统计学意义,但SC在降低永久性肠造口率(OR=0.52,95%CI:0.35 ~ 0.77,P= 0.001)及改善生活质量方面优于STC和TPC[97]。另一项多中心、前瞻性全国队列研究(SCOTCH 研究)比较了 285 例行 SC 与 402 例行TC治疗的CD患者的长期结局,结果显示SC组5年(15%比 22%)、10 年(22% 比 34%)和 15 年(27% 比 44%)复发率上升幅度小于TC组,Log⁃rank检验显示,TC术后长期复发率更高(P=0.006)[98]。
推荐意见18:药物治疗失败的广泛结肠CD合并难治性直肠炎或肛门功能丧失患者,推荐实施全结肠直肠切除及永久性回肠造口术;对于直肠炎症可控、有生育需求、保肛意愿强烈的患者,可考虑保留直肠;部分经过严格筛选的小肠未受累且直肠炎症可控的患者可以实施全结肠直肠切除加回肠储袋肛管吻合术。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:广泛结肠型CD的手术策略需兼顾复发风险、长期结局和生活质量。伴有难治性直肠炎或复杂肛周病变(如肛门失禁、严重肛管直肠狭窄)的患者需接受TPC加永久性回肠造口;有生育需求或者拒绝永久性回肠造口的CD患者,如果直肠及肛周炎症通过积极的药物治疗能够缓解,在充分告知复发风险的前提下可以选择STC保留直肠,术后进行积极的药物治疗控制直肠炎症复发。回肠储袋肛管吻合术(ileal pouch anal anastomosis,IPAA)用于CD患者中储袋失败率显著升高,仅适用于严格筛选且愿意接受储袋失败风险的患者。
一项回顾性研究比较了394例广泛结肠CD患者行不同手术方式的远期效果,结果显示,TPC加回肠造口术或SC或TC加回肠直肠吻合术(ileorectal anastomosis,IRA)3种术式术后10年症状复发率分别为37%、47%、58%(P = 0.0002),多因素分析显示 IRA(RR = 2.9,95% CI:1.5 ~ 5.5)和 SC(RR =3.0,95% CI:1.5 ~ 6.0)均为CD复发的独立危险因素[99]。系统综述与Meta分析显示,中位随访7.4年,TPC加回肠造口术后总体临床复发率为28%,合并回肠病变是复发独立危险因素(RR = 3.2,95%CI:1.8 ~ 5.6),无回肠病变患者临床与手术复发率仅为11.5%与10.4%[100]。
接受IBD相关手术(尤其是开腹IPAA)的女性不孕风险显著升高(RR = 5.45,95%CI:0.41 ~ 72.57)[101],腹腔镜 TC加IRA由于显著减少了盆腔手术操作,术后盆腔粘连程度明显减轻,有助于降低女性不孕风险。CD患者IRA术后直肠癌患病率(0.7%,95%CI:0.2% ~ 1.6%)显著低于UC患者(3.2%,95%CI:2.3% ~ 4.3%),其发生风险相差约10倍(OR = 10.3,95%CI:2.5 ~ 41.9,P = 0.001)[102]。
系统回顾与Meta分析显示,CD患者行IPAA术后储袋失败(24.7% 比 5.7%,P < 0.000 1)、储袋瘘(23.3%比4.5%,P = 0.006)和吻合口狭窄(19.9%比13.3%,P = 0.02)发生率均显著高于 UC 患者[103]。一项包括 3 707 例(含 150 例 CD,2 953例 UC)患者的队列研究显示,CD 患者 IPAA 术后 10 年有13.3%储袋功能丧失、15.6%切除储袋并永久造口,储袋保留率显著低于UC(80% 比 95%,P < 0.001)。然而,在储袋功能良好的前提下,两者生活质量评分差异无统计学意义[104]。
(四)预防术后复发
推荐意见19:对CD术后患者需要进行规范化管理。存在复发危险因素的患者,推荐在术后恢复良好的前提下及时启动药物治疗预防复发。(证据等级:Ⅱ,推荐强度:强推荐)
推荐理由:存在复发危险因素的患者术后需要及时进行药物治疗以降低复发风险。为避免生物制剂或小分子药物可能增加术后感染风险,推荐在术后患者恢复良好(窗口期2 ~ 4周)的前提下及时启动预防复发药物治疗,并结合治疗药物监测与规范化随访机制,实现疾病长期缓解。
术后复发的危险因素包括(1)疾病特征,如吸烟、年轻发病、穿透性病变、肛周病变、广泛小肠病变(累及肠管长度≥50 cm);(2)手术病理学特征,如切缘透壁性炎症、肌间和黏膜下神经丛炎及肉芽肿;(3)既往肠道手术史及残留病变等。为减少术后复发,具备上述复发风险因素的患者术后应及时采用药物预防措施(参见《中国克罗恩病诊治指南(2023 年·广州)》[2]推荐意见 38)。多个随机对照试验显示,术后2~4周是启动生物制剂或免疫制剂的窗口期,能够兼顾药物疗效与手术安全[105⁃107]。
术后6个月或出现复发症状的患者应及时进行内镜检查以评估是否复发,具体措施见《中国克罗恩病诊治指南(2023年·广州)》[2]推荐意见39。RCT(POCER和PREVENT研究)显示,治疗药物浓度监测指导下的药物调整可有效降低术后内镜复发风险(IFX浓度 >7.77 µg/mL、阿达木单抗浓度 >5 μg/mL时内镜复发率显著降低)[106⁃107]。
三、肛周CD
推荐意见20:推荐对所有确诊或疑诊CD的患者进行肛周病变规范化评估。(证据等级:Ⅱ,推荐强度:强推荐)
推荐理由:pCD 具有高度异质性,甚至是部分 CD 患者的首发表现,也是影响 CD 患者长期预后的重要因素之一。肛周瘘管型CD(perianal fistulizing Crohn′s disease,pfCD)是pCD最常见且最具有挑战性的病变类型,病情复杂,复发率和致残率高,显著增加患者疾病负担和心理压力。因此,无论是否有肛周症状,所有确诊或疑诊CD患者均应常规接受肛周病变筛查和规范化评估。
pCD包括瘘管性病变(如肛瘘、直肠阴道瘘)和非瘘管性病变(如肛周皮赘、肛管直肠溃疡、狭窄等)。2013年亚太地区的流行病学调查结果表明,中国大陆pCD患者约占CD总人群的33% ~ 60%[1]。pCD患者的规范化评估包括病史(含既往用药及手术情况)、疾病分型和活动度、解剖特征(瘘管/脓肿/狭窄)、括约肌功能等关键要素。盆腔或直肠增强MRI是pCD首选影像学检查,用于了解pCD解剖学特征、疾病分型和活动度,以及括约肌结构等。若MRI检查受限,经肛直肠腔内超声可作为替代手段[2]。推荐采用Cardiff分类[108]、肛周病变活动指数(perianal disease activity index,PDAI)[109]、Van Assche评分[110]和MAGNIFI⁃CD指数[111]作为肛周病变类型及活动度的评估工具。综合应用这些工具有助于全面了解 pCD 患者病变活动性及治疗效果。TOpCLASS 分类系统克服了传统pfCD分类的局限性,根据患者瘘管进程和严重程度从多个维度提供精准分层管理,包括局部治疗、转流性肠造口和直肠切除等干预时机[112]。
推荐意见21:肛周皮赘、肛管溃疡、外阴转移性CD及症状性痔,推荐采用非手术治疗。影响肛周护理的皮赘或非手术治疗失败的症状性痔在CD缓解期可考虑手术。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:在CD活动期对肛周皮赘、肛管溃疡、外阴转移性病变和症状性痔实施手术显著增加创口不愈合、肛门失禁及狭窄等并发症风险。有效控制活动性CD,结合饮食调节和局部外用药治疗,上述病变常可以缓解。在活动性CD得到有效控制后对症状性痔进行手术是安全的。
肛周皮赘、肛管溃疡、外阴转移性CD的发生频率随着肠道受累程度增加而上升,手术干预显著增加创面不愈合及肛门功能障碍风险,推荐采用非手术治疗。免疫调节剂和生物制剂如抗TNF⁃α单抗等早期干预有良好疗效[113]。增加膳食纤维和水分摄入、适度使用大便松软剂或缓泻剂,以及坐浴联合甲硝唑栓、硝酸甘油软膏或他克莫司软膏等,均能有效缓解临床症状[113⁃114]。
一项涵盖跨度近 40 年病例的系统评价与荟萃分析显示,IBD患者(119例CD和103例UC)痔手术总体并发症发生率为9%(95%CI:3% ~ 16%),其中CD显著高于UC(11% 比5%)[115]。对保守治疗无效的肛周皮赘及症状性痔,有效控制活动性炎症能显著提升手术安全性[114⁃116]。Mckenna等[116]分析了97例(49例CD和48例UC)痔和皮赘手术病例,包括胶圈套扎术(35例)、皮赘切除术(27例)、痔切除术(21例)及血栓切除术(14例)等,术后仅5例患者接受直肠切除术,并且直肠切除与局部手术无直接相关。
推荐意见22:未愈合的皮下瘘、低位括约肌间或经括约肌瘘,在直肠炎症得到有效控制且无肛门失禁风险时,推荐瘘管切开术。(证据等级:Ⅲ,推荐强度:弱推荐)
推荐理由:与拆除引流挂线、各种保留括约肌手术相比,瘘管切开术的长期愈合率更高。多项临床研究表明,对于药物治疗未愈合的低位瘘管,若无活动性直肠炎,且手术不影响括约肌功能,瘘管切开术通常能获得满意的疗效。
一项纳入66例症状性pCD患者的研究证实,35例低位瘘管(包括皮下瘘、低位括约肌间瘘和低位经括约肌瘘)接受瘘管切开术,瘘管愈合率为88.6%(31/35),所有患者术后未出现控便功能下降[117]。另一项研究包含29例无直肠炎、排便功能正常且瘘管内口上方至少保留1.5~2 cm功能正常的肛门括约肌的 CD 患者,瘘管切开术后创口愈合率 100%,6 例(20.7%)出现轻度可接受的肛门失禁[118]。然而,van Koperen 等[119]研究显示,28 例接受瘘管切开术的 pCD 患者中,瘘管愈合率 82.1%(23/28),但肛门失禁发生率为 60.9%(14/23),肛门失禁的原因包括多次肛瘘手术导致的括约肌损伤和瘢痕,以及腹泻及长期直肠炎引起的直肠顺应性下降。
推荐意见23:pfCD常合并肛周感染,推荐充分外科引流控制感染,并在感染控制后尽早启动生物制剂治疗。(证据等级:Ⅱ~Ⅳ,推荐强度:强推荐)
推荐理由:生物制剂或免疫调节剂可能通过抑制局部免疫监视,导致瘘管外口过早闭合而增加肛周脓肿发生率,但在充分外科引流控制感染的基础上,早期启动生物制剂可避免延误疾病治疗,有助于瘘管愈合。
与免疫调节剂一样,合并感染是生物制剂的使用禁忌。一项纳入94例pfCD患者的RCT发现,接受IFX治疗的患者肛周脓肿发生率 11%,而安慰剂组为 3%[120]。Jones[121]分析了1993—2004年美国全国住院患者样本数据库(NIS)CD外科手术趋势,结果显示随着IFX的临床应用,肛周脓肿发生率增加了3倍。因此,在使用生物制剂前必须对肛周脓肿进行充分引流以控制感染,避免在免疫抑制状态下感染加重。生物制剂对肛周创面愈合起着重要驱动作用。肛周感染得到控制后,应尽早启动生物制剂,避免治疗延误。英国一项调查显示,77.7%(80/103)的 IBD 专科医生在肛周感染控制后的4周内启动药物治疗(抗生素除外)[122]。法国的一项研究显示,启动IFX距手术间隔时间超过6周对瘘管长期闭合产生不利影响[123]。近期一项回顾性研究进一步证实,手术后早期(平均治疗间隔时间9 d)启动IFX患者的瘘管长期愈合率61.6%,平均随访36个月,1年、2年和3年累积复发率分别为23%、32%、34%[124]。
推荐意见 24:推荐生物制剂联合非切割挂线作为复杂pfCD的标准治疗方案,不推荐单一治疗手段(药物治疗或挂线引流)或切割挂线治疗 pfCD。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:相较于单纯药物或手术治疗,生物制剂联合非切割挂线引流显著改善了 pfCD 瘘管应答率和长期愈合率,推迟复发时间,降低再手术率。相较之下,单纯挂线引流再手术率高,而切割挂线显著增加肛门失禁风险,应避免用于pfCD。
一项多中心随机对照试验(PISA)比较了单纯挂线引流、抗TNF⁃α单抗治疗和抗TNF⁃α单抗联合挂线引流3种治疗方式对pfCD的疗效,结果显示单纯挂线组因再手术率显著高于其他两组(10/15 比 6/15 比 3/14,P = 0.02)而提前终止研究,提示单纯挂线引流不应作为pfCD唯一治疗手段[125]。另一项回顾性研究比较IFX联合挂线引流与IFX单药治疗,结果显示联合治疗组瘘管应答率更高(100%比79%,P = 0.001),复发率更低(44% 比 79%,P = 0.001),瘘管复发间隔显著延长(13.5个月 比 3.6个月,P = 0.001)[126]。系统评价与荟萃分析显示,抗 TNF⁃α 单抗联合挂线引流的瘘管愈合率达 64%(95%CI:55% ~ 73%),显著优于抗 TNF ⁃ ɑ 单抗单药治疗(47%,95%CI:41% ~ 53%)[127]。国际多中心回顾性研究显示,接受多模式(手术与生物制剂联合应用)治疗的患者瘘管完全愈合率为 52%(86/165),再手术风险显著降低(OR = 0.35,95%CI:0.17 ~ 0.57,P = 0.001),直肠切除及转流性肠造口手术率亦显著下降(OR = 0.21,95%CI:0.05 ~ 0.81,P = 0.02)[128]。一项纳入24个研究的系统评价显示,349例接受多模式治疗患者的瘘管完全缓解率(52% 比 43%)和无应答率(23% 比34%)均明显优于448例接受单一治疗患者,多模式治疗的临床获益较单一挂线引流(66% 比36%)抑或瘘管切开挂线引流(55% 比 25%)更为显著[129]。
荟萃分析显示,腺源性肛瘘行切割挂线后肛门失禁率高达 16%(95%CI:5% ~ 38%)[130]。最近一项多中心横断面研究指出,22.3%(134/600)的CD患者存在肛门失禁[131]。如果采用切割挂线治疗pfCD,肛门失禁率势必更高,因此必须强调,对pfCD严禁应用切割挂线术。
推荐意见25:建议采用MRI评估瘘管纤维化程度用于指导引流挂线拆除时机。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:研究显示,瘘管纤维化程度超过 60% 或MAGNIFI⁃CD指数低于6分,均能较为准确地预测瘘管长期愈合。将MRI影像参数与定量评分系统联合应用于临床实践,可以优化引流挂线的管理策略。
引流挂线最佳移除时机仍不明确,现有研究结果不一致[123,132]。最近一项随机对照研究(PISAⅡ)比较了单纯IFX治疗或IFX联合瘘管闭合手术的瘘管长期愈合情况,结果表明,MRI显示的瘘管纤维化程度和MAGNIFI⁃CD指数在预测瘘管长期闭合方面具有重要临床价值,MRI显示100%纤维化的患者在随访12个月时瘘管均实现了临床闭合,而纤维化程度低于40%患者长期闭合率较低。纤维化程度超过60%表现出良好预测价值(AUC = 0.90,95%CI:0.82 ~ 0.99),IFX治疗组有2/3实现长期闭合,联合治疗组则全部实现长期闭合[133]。此外,MAGNIFI⁃CD指数在预测瘘管长期闭合方面表现出高度准确性。治疗后,临床闭合患者的MAGNIFI⁃CD指数中位数为 0(IQR 0 ~ 5)分,而未闭合患者为 16(IQR 10 ~20)分;MAGNIFI⁃CD指数 < 6 分被认为是瘘管长期闭合的有力预测指标(AUC =0.95,95%CI:0.89 ~ 1.00),敏感性87%,特异性91%[133]。
推荐意见 26:推荐经直肠推移瓣手术和经括约肌间瘘管结扎术作为CD合并复杂肛瘘的治疗手段,联合使用生物制剂能够改善治疗效果。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:瘘管预期无法闭合或引流挂线移除后未闭合、解剖位置不适合瘘管切开术的pfCD患者,在生物制剂治疗基础上实施经直肠黏膜瓣推移术(endorectal advancement flap,AF)和经括约肌间瘘管结扎术(ligation of the intersphincteric fistula tract,LIFT)为主流的瘘管闭合术,能显著提高瘘管长期闭合率,降低再手术风险,并有效维护肛门控便功能。
早期的系统综述显示,AF治疗pfCD的成功率为64.0%(33.3% ~ 92.9%)、肛门失禁率9.4%(0 ~ 28.6%)[134]。2019年一项系统回顾与荟萃分析证实,AF治疗pfCD成功率为61%(45/76),LIFT手术成功率为53%(9/17)。尽管AF组的失禁率略高于LIFT组(7.8% 比 1.6%),但两种术式总体失禁风险均在可接受范围[135]。相较于AF,LIFT的理论优势在于不涉及对患病肠黏膜部位的手术操作,因而更适合 pfCD。前瞻性队列研究显示,LIFT 治疗 pfCD 长期治愈率 65%(30/46),吸烟是治疗失败的危险因素(HR = 3.18,P = 0.02),合并活动性直肠炎虽与疗效下降相关,但差异无统计学意义(HR = 1.97,P = 0.19)[136]。
PISAⅡ研究纳入 94 例单一内口、单一瘘管的活动性pfCD 患者,其中 38 例在瘘管闭合术的同时联合 4 个月抗TNF⁃α单抗治疗,56例接受1年的抗TNF⁃ɑ单抗治疗,18个月影像学随访结果显示,与单纯药物治疗组相比,联合治疗组影像学愈合率更高(32% 比 9%,P = 0.005),再手术率显著降低(13% 比 43%,P = 0.005);中位随访时间5.7年,临床愈合率(72% 比 62%,P = 0.18)、影像学愈合率(42% 比 18%,P =0.014)和再手术率(15% 比 53%)均证实抗TNF⁃α单抗联合瘘管闭合术是治疗pfCD的有效策略[137⁃138]。
推荐意见27:不推荐纤维蛋白胶和肛瘘栓作为pfCD的常规治疗手段。瘘管激光闭合术和视频辅助瘘管治疗术用于pfCD尚缺乏足够的高质量、长期随访研究支持。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:尽管现有文献提示纤维蛋白胶、肛瘘栓、瘘管激光闭合术和视频辅助瘘管治疗术对复杂肛瘘具有一定的疗效,但用于治疗pfCD还缺乏足够样本量的高质量、长期随访结果,无法证实其疗效。
一项多中心RCT表明,71例经挂线引流的pfCD患者随机分配至纤维蛋白胶治疗组或对照组,短期(8周)疗效显示治疗组临床缓解率显著高于对照组(38% 比 16%,P = 0.04)[139]。另一项回顾性研究显示,纤维蛋白胶治疗 pfCD 1年临床缓解率为 45.4%,联合抗 TNF⁃α 单抗和免疫制剂治疗组为63%,但5年随访期间累积复发率达54%[140]。一项随机对照试验将挂线引流后的患者随机分配至肛瘘栓组(54例)与单纯拆除挂线组(52例),术后12周,肛瘘栓组瘘管闭合率与拆除挂线组差异无统计学意义(P = 0.19),基于瘘管复杂程度进行分层后优势亦未体现(P = 0.45);此外,肛瘘栓组不良反应发生率显著升高(17% 比 8%,P = 0.07)[141]。
瘘管激光闭合术(fistula⁃tract laser closure,FiLaC)的疗效证据主要源于小样本、回顾性研究。一项系统回顾纳入6 项研究共 50 例 pfCD 患者,FiLaC 术后瘘管闭合率 68%(95%CI:53.0%~84.0%)[142]。最近一项回顾性研究报告了FiLaC 术后 50(39.5~54.0)个月的随访结果,瘘管治愈率63.3%(31/49),但 30.6%(15/49)的患者瘘管未愈合或复发[143]。 视 频 辅 助 瘘 管 治 疗 术(video ⁃ assisted anal fistula treatment,VAAFT)治疗 pfCD 的结果亦来自小样本回顾研究。一项纳入84例患者(包含11例pfCD)的研究显示,平均随访8(1~46)个月,pfCD瘘管愈合率仅为27%(3/11)[144]。另一项研究纳入经多次手术和生物制剂治疗失败的复杂性pfCD患者,在VAAFT手术同时置入引流挂线,术后6周 84%(21/25)患者症状改善,1 例患者术后 2 周需要再次手术干预[145]。上述研究显示VAFFT能够改善pfCD临床症状,但治愈率低。
推荐意见 28:异体脂肪来源间充质干细胞治疗复杂pfCD 的疗效存在争议。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:多项随机临床试验、系统评价及荟萃分析显示,异体脂肪来源间充质干细胞在治疗难治性pfCD方面展现出较好的临床疗效,52周的瘘管临床缓解率明显优于安慰剂组,且未观察到严重不良反应。然而,近期一项全球随机、双盲、安慰剂对照临床研究结果却显示,间充质干细胞在瘘管愈合方面没有统计学优势,提示其疗效仍存在争议。
一项国际多中心Ⅲ期临床研究纳入212例经挂线引流处理后的难治性pfCD患者,分别接受异体脂肪来源间充质干细胞(Cx601,Darvadstrocel)或生理盐水局部注射,52周治疗组瘘管综合缓解率(外口闭合,MRI无>2 cm的脓肿)显著优于安慰剂组(56.3% 比38.6%,P = 0.01),未出现严重并发症;随访至 104 周,治疗组 56%(14/25)维持临床缓解,安慰剂组为 40%(6/15)[146⁃147]。来自西班牙 14 个中心的回顾性观察研究显示,接受Darvadstrocel治疗的患者86.3%(63/73)获得临床应答,68.5%(50例)临床缓解,69.2%(45/65)的患者影像学愈合,无严重不良反应[148]。一项综合了 11 项临床观察(9 项异体脂肪来源间充质干细胞和自体、异体来源骨髓间充质干细胞各1项)的系统评价及荟萃分析结果显示,与对照组相比,间充质干细胞提高了 6 ~ 24 周(OR = 3.06,95%CI:1.05 ~ 8.90,P = 0.04)及24 ~ 52周(OR = 2.37,95%CI:0.90 ~ 6.25,P = 0.08)的pfCD愈合率,未增加不良反应[149]。
然而,2024 年欧洲克罗恩和结肠炎组织学术年会报道的 ADMIRE⁃CD Ⅱ与Ⅲ期全球 RCT 结果对上述结论提出了挑战,研究纳入 568 例临床控制良好、处于缓解期或轻度活动期、对免疫调节剂或生物制剂治疗应答不佳的复杂 pfCD 患者,按 1∶1 随机接受 Darvadstrocel 单次局部注射(120×106个细胞/24 mL)或安慰剂治疗。所有患者在治疗前 2 ~ 3 周进行瘘管清创和挂线引流,注射前去除挂线、清创并闭合内口。24 周时,治疗组与安慰剂组的临床缓解率无显著差异(48.8% 比 46.3%),安全性结果与既往研究一致[150]。
推荐意见29:CD相关直肠阴道瘘首选药物治疗。药物治疗效果不佳且症状明显的患者推荐在经验丰富的外科中心进行手术治疗。(证据等级:Ⅱ~Ⅲ,推荐强度:强推荐)
推荐理由:CD相关的直肠阴道瘘采用抗TNF⁃ɑ单抗显示出与手术相当的临床疗效。与药物治疗相比,手术致残风险高,仅限于药物治疗未缓解、症状明显的患者,并且当活动性直肠炎得到有效控制后可考虑在有经验的外科中心进行手术修复。
CD相关的直肠阴道瘘(rectovaginal fistulas,RVF)推荐由经验丰富的多学科团队进行病情管理,首选药物治疗。ACCENTⅡ研究针对直肠阴道瘘的亚组分析显示,IFX诱导治疗的患者中,第10周瘘管闭合率为60.7%(17/28);维持治疗期间,IFX 组第 14 周和第 46 周的瘘管持续闭合率分别为54.5%和90.0%,显著优于安慰剂组(28.6%和42.9%)[151]。一项系统评价纳入16项RVF研究,其中13项评估了药物治疗的效果,结果显示,接受抗TNF⁃α单抗治疗的患者中,完全缓解率 41%(32/78),部分缓解率 21.8%(17/78),无应答率37.2%(29/78),另外 3 项研究评估了药物联合手术治疗,完全缓解率44.2%(19/43),部分缓解率20.9%(9/43),未改善者34.9%(15/43)[152]。
药物治疗无效、症状明显且瘘管条件允许的患者建议在外科经验丰富的中心实施个体化手术修复。一项纳入9项CD相关直肠阴道瘘手术治疗的系统评价显示,瘘口愈合率为50%~75%,但多数研究样本量小,人群特征和手术类型差异较大[153]。Otero⁃Piñeiro等[154]报道了目前规模最大的一组患者手术结果,166例患者共进行360次手术,44.0%患者围手术期接受生物制剂治疗,中位随访时间 5.5 年,瘘管总愈合率71.7%,患者平均接受 2 次手术,首次手术愈合率 33.1%,第2次和第3次手术的愈合率分别为51.8%和62.1%;不同术式疗效差异明显,经腹直肠切除吻合术成功率49.0%(48/98)、股薄肌置入术50.0%(4/8)、经阴道推移黏膜瓣40.0%(6/15)、经直肠推移瓣32.4%(22/68)、挂线引流18.0%(18/100),50.6%(84/166)的患者需接受转流造口术。
推荐意见 30:有症状的肛管直肠狭窄首选药物治疗联合麻醉下扩肛。器械扩肛、内镜治疗失败的纤维化狭窄建议手术。(证据等级:Ⅲ,推荐强度:弱推荐)
推荐理由:由于临床证据有限,针对肛管直肠狭窄的治疗策略缺乏明确、统一的指导意见。研究显示,抗TNF⁃α单抗联合器械扩肛能有效控制狭窄进展,降低直肠切除及永久性造口的风险。对严重、不可逆的纤维化狭窄,如果器械扩张、内镜治疗失败,建议做经肛狭窄成形或狭窄弧形切除术。上述治疗均失败的患者,最终选择直肠切除联合永久性造口。
肛管直肠狭窄的局部干预首选麻醉状态下器械扩张,从能够容纳的最大直径扩肛器开始,逐渐扩张到16 ~ 18 mm,扩张成功后指导患者居家扩肛以维持疗效。早期研究显示,33 例接受扩肛治疗的 CD 患者中(15 例仅需 1 次扩肛,8 例2 次,10例3次或以上),最终14例患者长期缓解,3例接受转流造口,14例接受直肠切除[155]。一项纳入102例CD相关肛管直肠狭窄患者的回顾性研究显示,平均随访 2.8 年,32%患者需接受肠造口或直肠切除。抗TNF⁃α单抗治疗联合扩肛的患者中,3 年随访时54.5%处于缓解期,多因素分析显示抗TNF⁃α单抗治疗显著降低不良结局的风险[156]。
对于长度小于2 cm的短段纤维性狭窄,可考虑Heineke⁃Mikulicz(H⁃M)狭窄成形术。一项回顾性研究纳入15例(含7 例 CD)因肛管直肠狭窄行 H⁃M 成形术的患者,平均随访21 个月,2例失败(含1例CD患者)[157]。作为难治性肛管直肠狭窄患者永久造口术前的挽救性治疗手段,最近一项新技术,经肛直肠狭窄后侧弧形切除术显示出良好的长期疗效,但需要进一步验证[158]。上述治疗均失败的患者,最终需要接受直肠切除术联合永久性造口[159]。
推荐意见 31:药物难治性直肠炎和局部手术治疗失败且严重影响生活质量的复杂pCD患者,建议实施转流性肠造口术。(证据等级:Ⅱ,推荐强度:弱推荐)
推荐理由:对于充分药物治疗和局部手术干预仍无法控制的难治性直肠炎、持续性肛周感染、肛门组织结构严重破坏或功能丧失的复杂pCD患者,转流性肠造口能显著改善患者的临床症状和生活质量。然而,转流性肠造口后只有不足20%的患者能够成功进行造口还纳,约40%患者需接受直肠切除。
两项系统评价探讨了转流性肠造口术治疗难治性pCD患者的临床结局,60.5% ~ 63.8%患者术后早期肛周症状获得缓解,然而,长期随访数据显示,仅16.6% ~ 21%患者最终成功恢复肠道连续性,生物制剂的使用并未显著提高造口还纳率(生物制剂组比非生物制剂组:24% 比 21%),34% ~41.6%患者最终需行直肠切除术[160⁃161]。因此,临床医生在决定转流性肠造口前应与患者进行详尽的讨论,确保其深入了解手术疗效的局限性和无法改变的最终结局,在充分知情的基础上做出决策。
推荐意见32:对不可逆性肛门功能丧失、转流性肠造口术后炎症持续不缓解的难治性肛周病变、或确诊pCD相关恶性肿瘤的患者,建议行直肠肛门切除术。(证据等级:Ⅱ~Ⅳ,推荐强度:弱推荐)
推荐理由:难治性pCD患者,若肛门功能已经不可逆丧失、转流性造口后肛周与直肠炎症仍未缓解,或确诊癌变,行直肠肛门切除联合永久性肠造口可有效改善患者生活质量。推荐术前充分控制肛周感染、选择经括约肌间入路切除直肠,以降低会阴创面不愈合的风险。合并恶性肿瘤时需遵循肿瘤治疗原则以确保手术疗效。
一项回顾性研究纳入119例接受过肛周手术的pCD 患者,平均随访93个月,结果显示25%患者最终需接受腹会阴联合直肠切除手术。多因素分析表明,pCD发病年龄>30岁(P<0.02)、肛瘘为首发表现(P<0.04)、随访期间肛周病变发作次数≥3 次(P<0.01),以及直肠受累(P<0.000 1)是直肠切除伴永久性肠造口的独立危险因素,同时具备上述4项危险因素的8例患者最终均接受了腹会阴联合直肠切除手术,保留肛门的患者中,44%(39/89)出现肛门失禁[162]。最近一项研究评估了因难治性pCD行暂时性转流肠造口患者的长期结局,中位随访90.1个月,36%(19/53)最终行腹会阴联合直肠切除术,手术指征为持续性肛周感染(58%,11/19)和药物难治性直肠炎合并复杂性肛瘘(26%,5/19)[163]。
接受直肠切除术的pCD患者会阴创面愈合不良发生率较高。最近一项纳入333例患者的系统评价与荟萃分析显示,术后 6 个月和 12 个月会阴创面愈合率分别只有 65%(95%CI:52% ~ 80%)和 70%(95%CI:63% ~ 83%)[164],建议在手术前通过转流造口或引流挂线等方式控制肛周感染,以降低术后会阴伤口并发症风险。多个研究推荐选择经括约肌间入路行直肠切除(intersphincteric resection,ISR)[165-166],然而,高达 78% pCD 患者因局部瘢痕和广泛纤维化导致括约肌间隙解剖不清,增加了手术难度[167]。
迁延不愈的肛管直肠炎症显著增加恶性肿瘤的发生风险。法国一项全国性IBD队列研究表明,肛周病变是IBD患者发生肛管直肠恶性肿瘤的唯一危险因素(OR = 11.2,95%CI:1.18 ~ 551.51,P = 0.03),将肛管直肠恶性肿瘤的风险提高了 9.36 倍(95%CI:2.61 ~ 33.54)[168]。德国一项多中心回顾性研究结果显示,CD癌变的患者中,90%(36/40)接受了标准肿瘤切除手术,其中R0切除率80.5%,术后1年和5年生存率分别为87.5%和65%,总生存期为(45 ± 28.6)个月,无进展生存期为(31.5 ± 32.5)个月[169]。
四、展望
随着IBD基础研究的不断深入和临床经验的不断积累,CD 外科治疗的目标已经从以处理并发症为核心的传统模式,向维持长期缓解、保全器官功能与提高生活质量方向转变。本指南的制定是推动我国CD外科治疗走向标准化、规范化的重要举措。未来CD的全程管理,仍将以内科治疗做为基石,外科治疗将更加着眼于从疾病治疗全周期中科学界定干预目的与时机,避免手术时机把握不当或内、外科过度治疗所造成的不良结局。规范、高效的MDT模式将在外科决策与围术期管理中发挥关键作用,实现从术前评估、预康复、规范化手术、手术并发症处理、术后维持与随访的一体化管理流程,全面提升我国 CD 的综合诊治水平,使患者长期获益。