

全球胃癌发病率存在巨大地域差异,但胃癌前病变是否以相似的速度进展为浸润性胃癌仍不清楚。该系统综述和meta分析,筛选
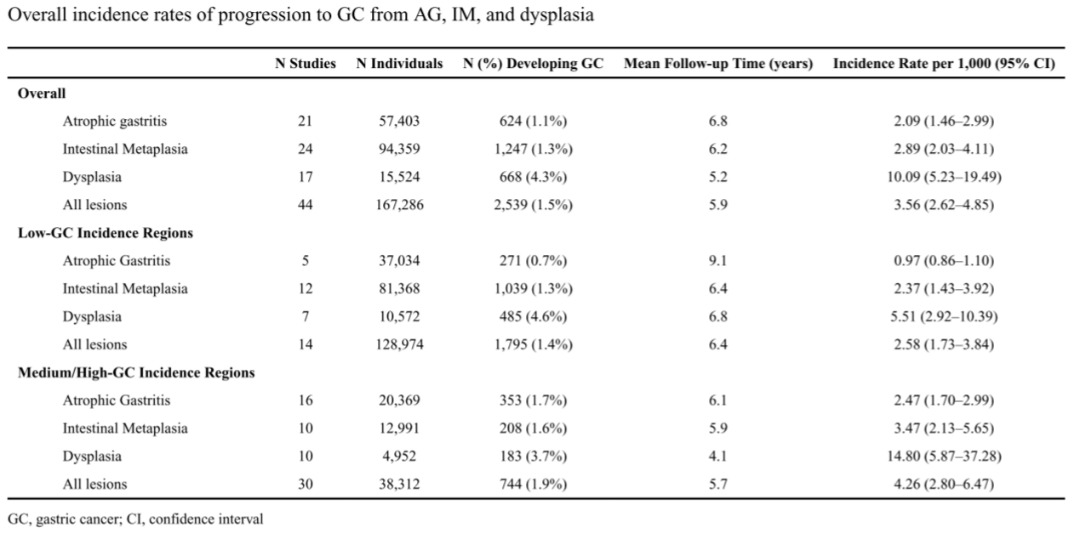
结果显示,全球萎缩性胃炎、肠化生和异型增生向胃癌的年化进展率分别为(单位:每1000人年):2.09(95% CI:1.46-2.99)、2.89(2.03-4.11)和10.09(5.23-19.49)。胃癌低发病率国家和中/高发病率国家的进展率分别为(单位:每1000人年):萎缩性胃炎:0.97(0.86-1.10) vs 2.47 (1.70-2.99)(P<0.01);肠化生:2.37(1.43-3.92) vs 3.47 (2.13-5.65)(P=0.29);异型增生:5.51(2.92-10.39) vs 14.80(5.87-37.28)(P=0.08)。当比较32篇高质量研究时,萎缩性胃炎的组间进展没有差异(2.02 vs 2.30,P=0.84)。
综上,在胃癌低发病率和中/高发病率国家中观察到相似的肠化生和异型增生向胃癌进展率。这表明,在胃癌低风险地区监测这些病变的潜在效益可能与在高风险地区进行全民干预的潜在效益相当。但仍需要进一步的前瞻性研究来证实这些发现,并为全球筛查和监测指南提供依据。
原文链接:Clin Gastroenterol Hepatol.2025 Aug;23(9):1514-1524.e13.DOI:10.1016/j.cgh.2024.09.003

该研究对来自6个国家超过1500例胃黏膜肠化生样本进行深度靶向测序(>270个基因),共鉴定出47个显著突变基因,包括与高危人群和较差预后相关的驱动基因(ARID1A)、KRAS/MAPK信号传导(KRAS、BRAF、MAP2K1、MAP3K1和MAP2K4)以及粘膜免疫改变相关基因(PIGR)。
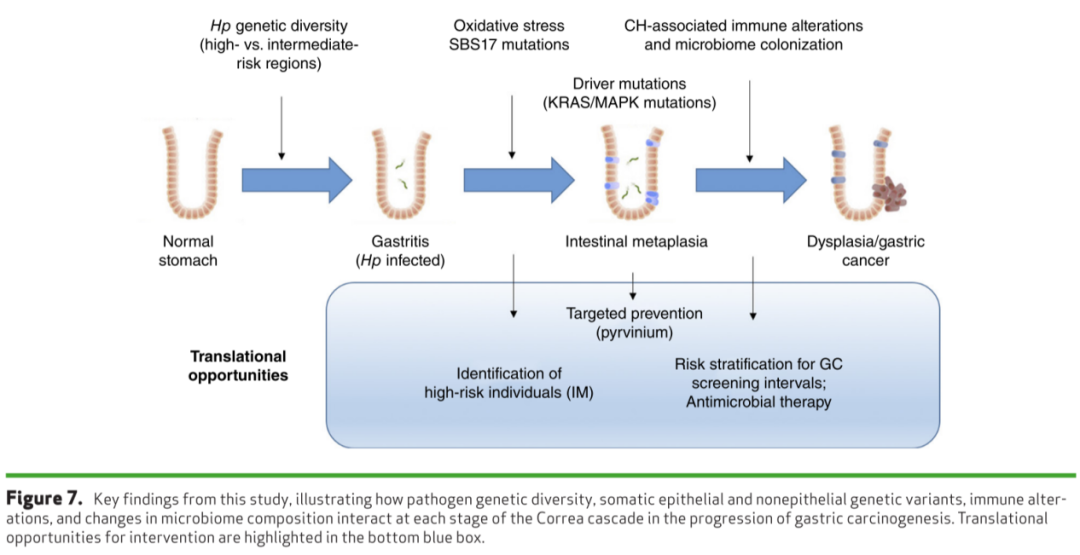
研究发现,突变基因存在地域差异,中国人群SOX9截短突变尤为突出,日韩人群中ARID1A、ARID2突变更为常见。在多种驱动基因的突变中,发现RAS/MAPK信号通路异常,其在胃干细胞和肠道干细胞/过渡扩增细胞中更为常见,提示该通路激活可能驱动肠化生发生发展。研究还通过肠化生全基因组测序和DNA甲基化分析发现,SBS17是一种区分肠化生与正常胃组织的特定突变基因,且与晚期DNA复制、基因组低甲基化和烟草暴露有关。除了上皮源性体细胞突变外,研究还观察到胃黏膜肠化生患者的克隆性造血升高与年龄、吸烟和进展为胃癌的风险增加有关。克隆性造血扩增的患者表现出同时发生肠化生PIGR截短突变和更多的咽峡炎链球菌等口腔菌群定植,表明克隆性造血可能通过调节宿主微生物粘膜免疫来促进肠化生进展。
综上,这项国际研究确定了肠化生驱动基因、特异性突变特征以及肠化生相关免疫图谱和微生物组的变化,并强调了非上皮体细胞改变(如克隆性造血)在肠化生进展为胃癌中的作用,为早癌检测和阻断提供了新的转化机会。
原文链接:Cancer Discov.2026 Jan 14:OF1-OF24.DOI:10.1158/2159-8290.CD-25-0778

胃泌素由胃窦G细胞分泌,通过结合胆囊收缩素-2/胃泌素受体(Cck2r)调节胃酸分泌和上皮细胞更新,在维持胃黏膜完整性中发挥重要作用。Cck2r在峡体祖细胞、肠嗜铬样细胞和壁细胞中表达,调节酸分泌和细胞更新。然而,胃泌素在黏膜再生过程中对Cck2r祖细胞的作用仍有待探索。
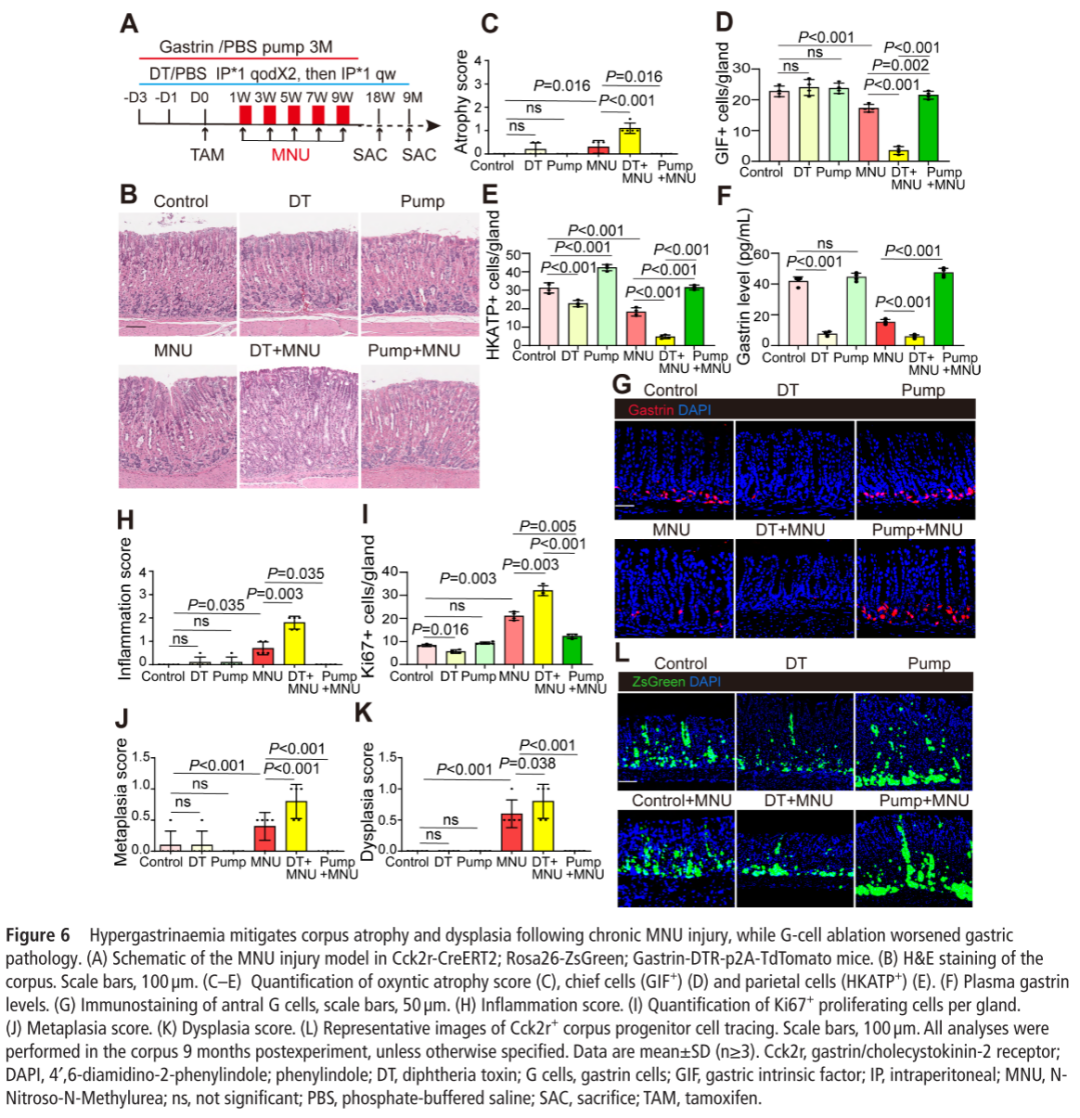
这项研究通过动物模型实验和临床队列分析,发现高胃泌素血症显著促进Cck2r+峡部祖细胞增殖,低胃泌素血症则抑制其数量(p<0.05)。慢性幽门螺杆菌相关性胃炎损伤中,G细胞消融会增加幽门螺杆菌定植,加剧胃黏膜炎症、萎缩、肠化生及异型增生,高胃泌素血症则具有保护作用(p<0.05)。在由N-亚硝基-N-甲基脲(MNU)造成慢性胃损伤的模型中,G细胞消融会加重胃病理损伤,而高胃泌素血症可减轻该损伤(p<0.05)。临床上观察到萎缩性胃炎患者胃窦G细胞计数显著低于非萎缩者,且在
综上,G细胞分泌的胃泌素在胃黏膜损伤后的再生和修复过程中发挥重要作用。低胃泌素血症是胃体萎缩及潜在的胃癌发生危险因素,而生理性胃泌素反应和胃泌素信号传导可能具有预防胃癌癌前病变的作用,为高风险人群胃癌前病变提供了新的预防和干预策略。
原文链接:Gut.2026 Jan 8;75(2):265-277.DOI:10.1136/gutjnl-2025-335103

胃癌发生存在明显的性别差异,推测性类固醇激素与胃癌的风险有关,但尚未在前瞻性研究中得以证实。该研究旨在中国男性前瞻性队列中分析性类固醇激素代谢物与胃癌和癌前病变风险之间的关联。
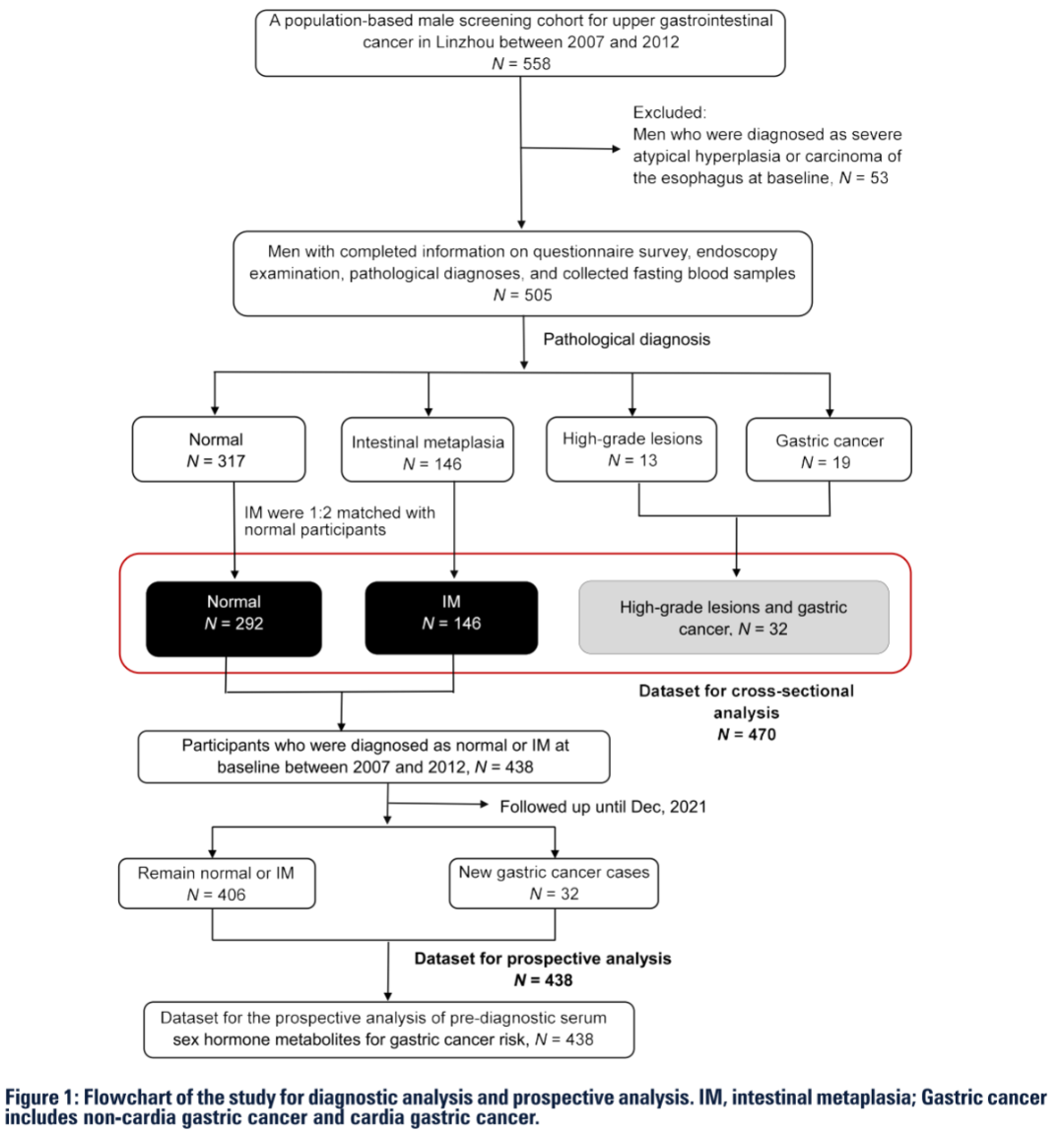
研究纳入2007-2012年包括高级别病变或胃癌(32例)、肠化生(146例)及1:2匹配的正常对照(292例)的470名男性,检测其血清中的20种性类固醇激素代谢物和性激素结合球蛋白(SHBG)。结果表明,
对基线时被诊断为正常或肠化生的438名参与者随访至2021年底(含32例新发胃癌病例),分析该队列中性激素与新发胃癌风险的关联,发现SHBG(HR=2.57,95% CI:1.04-6.36)、表睾酮(HR=2.10,95% CI:1.07-4.15)和孕烯醇酮(HR=1.30,95% CI:1.03-1.63)水平与新发胃癌风险显著正相关。按幽门螺杆菌状态分层的亚组分析显示,雄烯二酮、17α-羟基孕酮、孕酮、雌酮、SHBG、孕烯醇酮和胃癌风险之间存在相似的关联。
综上,多种性激素代谢物与胃癌及其癌前病变显著相关,表明性激素在胃癌发生中的关键作用,有望为胃癌高危人群的识别和风险预测提供新的生物标志物。
原文链接:J Transl Int Med.2025 Oct 16;13(5):436-455.DOI:10.1515/jtim-2025-0041

这项研究首先在动物模型中证实MEK抑制剂可阻断胃癌前病变Correa级联演变进程;后开展一项单臂、开放标签、多中心、前瞻性I期临床试验,评估了短期低剂量MEK抑制剂曲美替尼治疗胃癌前病变患者的安全性与耐受性,为此类患者提供了首个疾病修饰疗法。
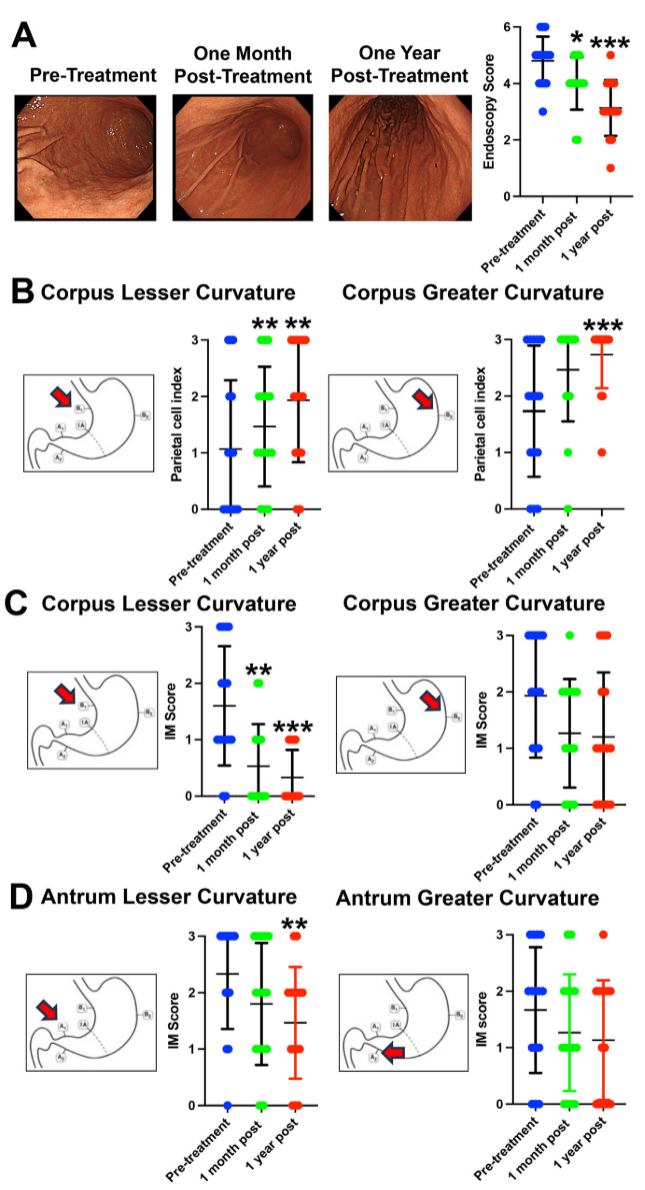
研究共纳入15例患者,所有患者均完成了为期2周的曲美替尼治疗疗程(每天口服1mg),并在治疗后1个月和1年进行2次内窥镜检查以随访胃癌前病变逆转效果。结果显示,患者在1个月和1年的内镜评分均显著改善,胃体部肠化生程度显著减轻,胃窦部肠化生程度有所减轻,但不如胃体部显著。安全性评估中,仅1例患者出现轻度血压升高,于停药后恢复正常。未观察到
综上,MEK抑制剂的有限持续治疗可能有效改善胃癌前病变。后续仍需开展更深入的研究,确定MEK抑制剂治疗的最佳剂量方案,以降低胃癌发生的风险,同时保证其应用的安全性。
原文链接:Gastroenterology.2025 Sep;169(4):722-725.DOI:10.1053/j.gastro.2025.05.023

对于幽门螺杆菌阴性的胃黏膜肠化生患者,治疗手段仍较为匮乏。该研究为了评估二甲双胍逆转肠化生的有效性和安全性,首先探究了二甲双胍在逆转小鼠胃黏膜肠化生的作用,证实了二甲双胍可有效改善小鼠胃黏膜肠化生。随后在中国一家三级医院进行了一项开放标签、前瞻性、随机对照临床试验,前瞻性纳入140例非
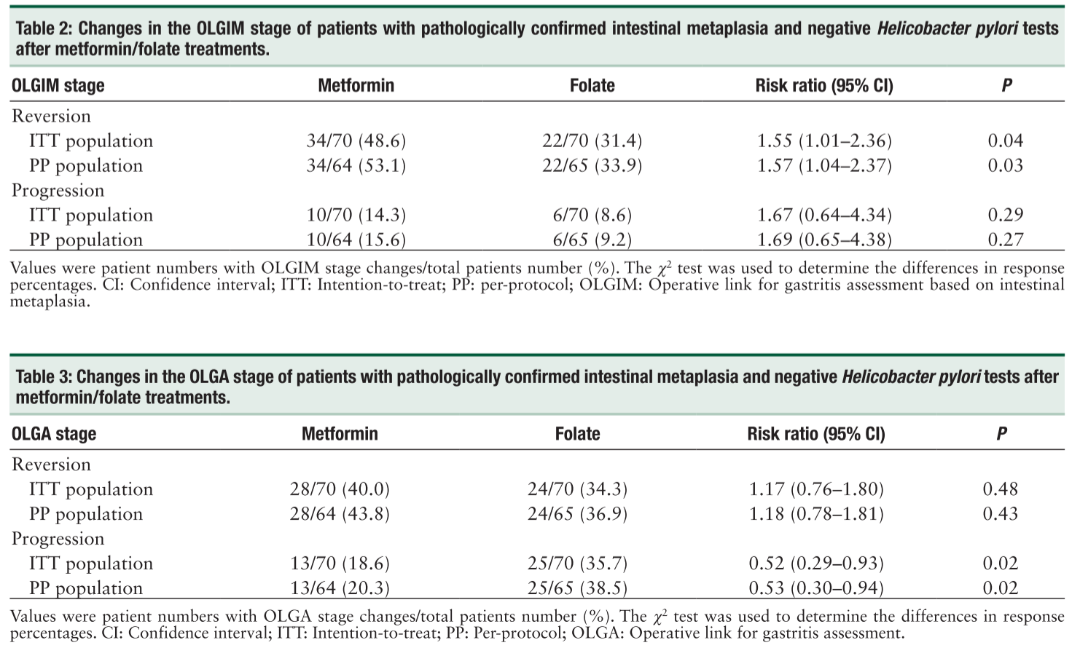
结果表明,相比于叶酸组,二甲双胍组肠化生逆转率显著更高(意向性治疗分析:48.6% vs 31.4%,RR=1.55,95% CI:1.01-2.36;P=0.04;符合方案集分析:53.1% vs 33.9%,RR=1.57,95% CI:1.04-2.37;P=0.03)。安全性方面,二甲双胍组报告13例不良事件均为自限性,血糖监测中未观察到低血糖现象,证实500mg/d二甲双胍在非糖尿病人群中的安全性。
综上,二甲双胍可安全、有效地促进非糖尿病、幽门螺杆菌阴性人群胃黏膜肠化生逆转,且安全性良好,为幽门螺杆菌阴性的肠化生患者提供了新的治疗选择。
原文链接:Chin Med J (Engl).2025 Jun 16.DOI:10.1097/CM9.0000000000003675

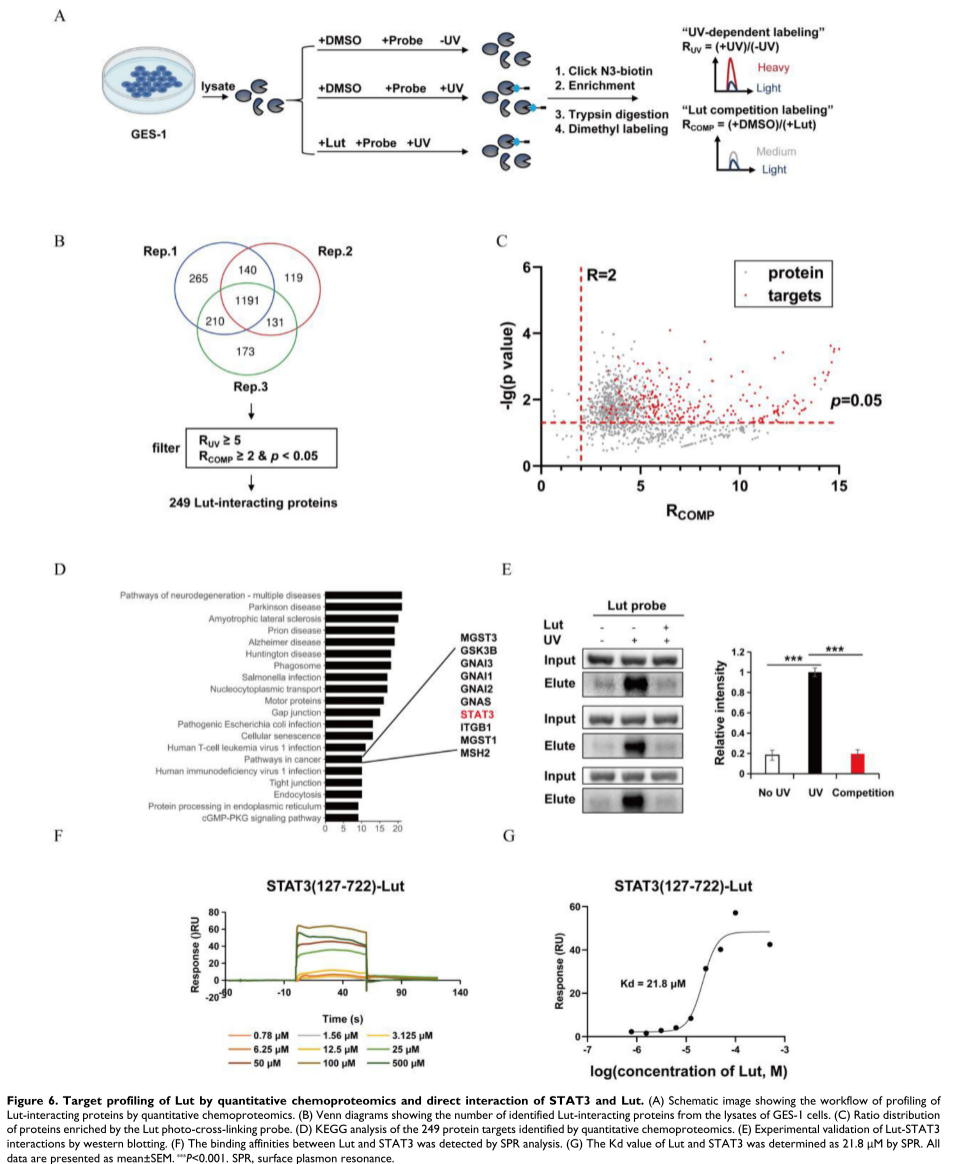
木犀草素(Luteolin)作为一种天然黄酮类化合物,已被证实具有抗炎、抗氧化和抗凋亡活性,可抑制胃癌细胞增殖。本研究旨在探究木犀草素能否改善胃癌前病变,并揭示其具体的作用靶点和信号通路。
研究团队在采用
综上,木犀草素可能是一种治疗胃黏膜损伤和癌前病变的候选药物,这一发现为胃黏膜癌前病变的治疗提供了新的靶点和策略。
原文链接:Int J Biol Sci.2025 May 7;21(8):3397-3415.DOI:10.7150/ijbs.111636

胃黏膜肠化生内镜分级(EGGIM)分类与胃黏膜肠化生的组织学评估相关,并且能够对胃癌风险进行分层。该研究开发并评估了用于EGGIM实现自动化内镜分级的人工智能(AI)方法。
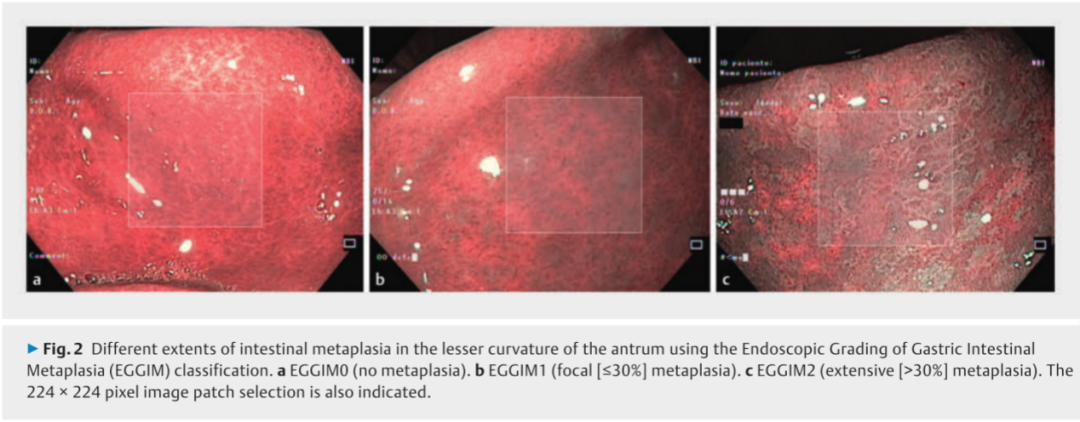
研究采用回顾性和前瞻性双数据集策略共收集1280张窄带成像(NBI)图像,基于ResNet-50构建深度神经网络(DNN)模型,通过留一患者交叉验证方法,将图像分为EGGIM 0(无化生)、1(局灶性化生:≤30%)、2(广泛化生:>30%)三类,最终决策结果由每位患者胃部五个不同解剖位置的EGGIM评分综合计算所得的EGGIM总分(0~10分)确定。
模型结果显示,该AI决策系统对每幅图像分析的准确度为87%(95% CI:71%-100%),每名患者EGGIM估计的平均误差为1.15(满分:10分)。当EGGIM≥5时,监测临床决策的准确率为88%(95% CI:80%-96%),特异性为85%(95% CI:75%–94%),无假阴性,阳性预测值和阴性预测值分别为62%(95% CI:32%-92%)和100%(95% CI:100%-100%)。
综上,该研究所开发的AI工具能够高精度估计EGGIM评分。而EGGIM的自动评估可能为胃癌风险分层、前瞻性研究和干预试验提供依据。
原文链接:Endoscopy.2025 Nov;57(11):1254-1260.DOI:10.1055/a-2657-9906

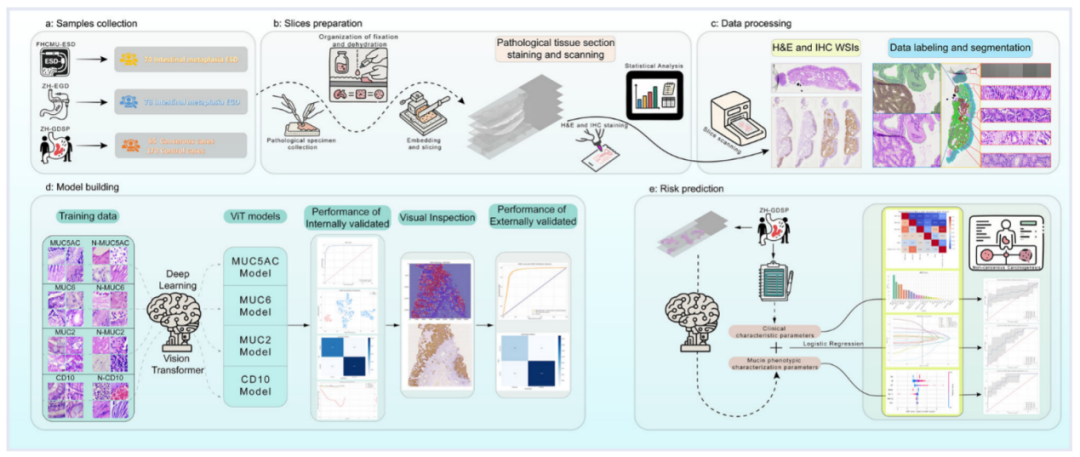
目前临床中尚缺乏针对胃癌前病变动态风险预测的专用工具,黏液表型系统在区分不同胃黏膜肠化生(GIM)亚型中具有重要价值。这项研究依托中国胃癌高发区建立的长期随访队列与生物样本库,基于UNI-2预训练的Vision Transformer(ViT)架构,采用部分微调和对抗学习热图生成策略,整合病理与临床信息,经多种机器学习模型完成特征筛选与优化,构建了MPMR-IMCP多模态风险预测模型。
结果表明,MPMR-IMCP模型在纵向队列中实现了高效能GIM癌变风险预测结果(AUC=0.814),较纯临床模型(AUC=0.764)显著提升。该模型无需免疫组化即可从H&E图像精准量化4种黏蛋白。通过黏蛋白动态演化分析,证实其动态变化规律是胃癌前病变的核心生物标志物,胃型标志物MUC5AC与MUC6随疾病进展逐渐下降,而肠型标志物MUC2与CD10则呈现非线性“峰谷”动态,即在GIM阶段达峰值,至癌变阶段骤降,揭示不完全型GIM(II、III型)的高恶性潜能。
该研究成功开发了首个基于H&E图像的双功能MPMR-IMCP风险预测模型,成为首个无需特殊染色即可完成GIM亚型分类与风险分层的工具,并揭示了黏蛋白“胃型丢失-肠型峰形”双轨动态,推动胃癌前病变分子分型临床化,有望用于指导胃癌前病变内镜监测频率与化学预防,为GIM的精准管理提供了可行的技术方案。
原文链接:NPJ Precis Oncol.2025 Dec 12;10(1):40.DOI:10.1038/s41698-025-01224-w

胃肠化生是一种癌前阶段,其形态学谱很少被人类细胞系模型所代表。这项研究通过建立并表征人胃肠化生细胞,以深入研究肠化生向胃癌的进展机制。
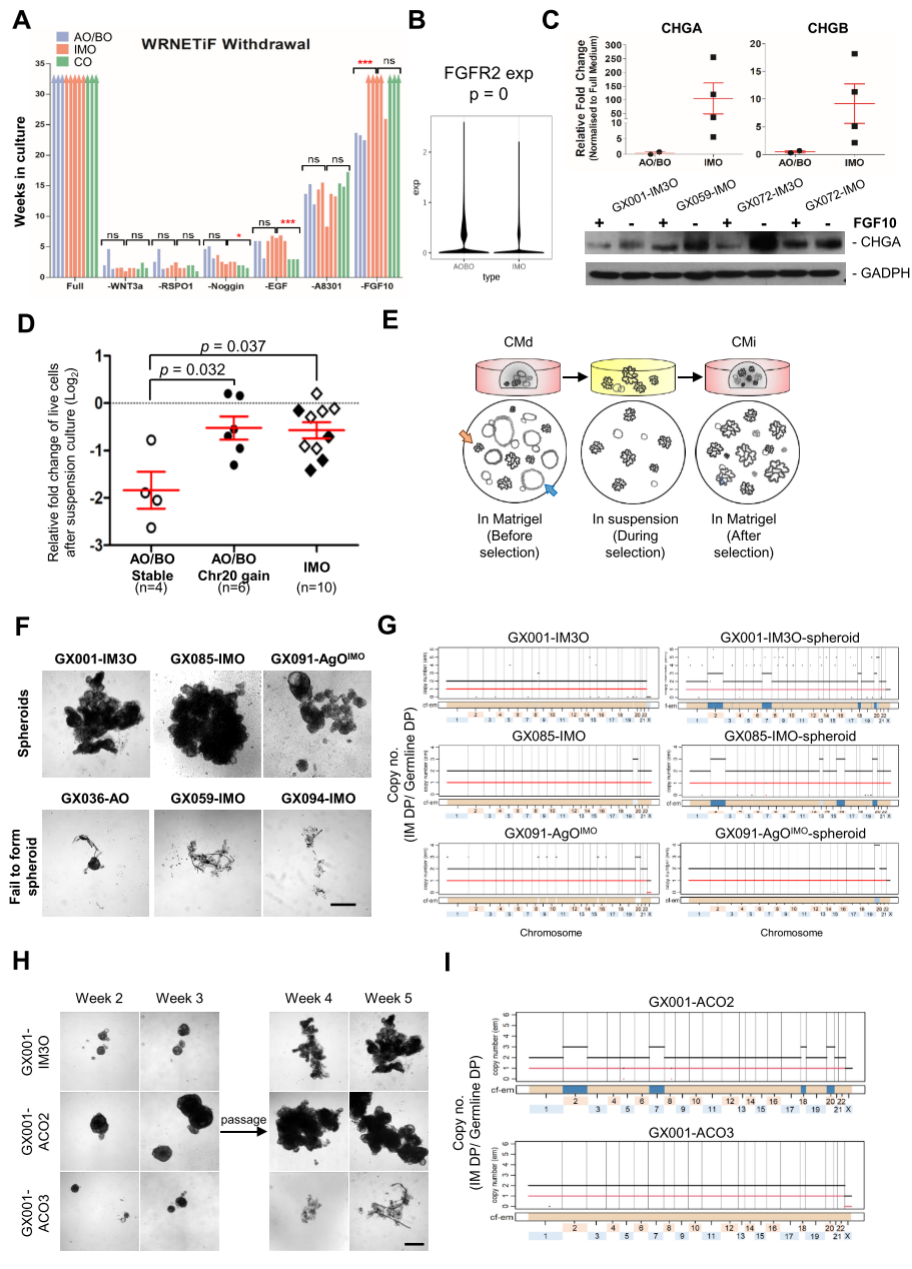
研究建立了一个大型人胃肠化生类器官(IMO)队列(n=28),以正常胃类器官(n=42)作为对照,进行全面的多组学分析和功能表征。单细胞转录组揭示了IMO细胞的范围涵盖了从混合胃/肠分化到高级肠分化的谱系,它们的谱系轨迹连接了不同的循环和静止干细胞和祖细胞,突出了它们在胃组织向肠化生转变中的差异以及STMN1循环峡部干细胞的肠化生的潜在起源。
混合型IMO表现出受损的分化潜力、显著的谱系可塑性和胎儿基因程序重激活,与之高度相似的是,肠化生和胃癌组织中的细胞群也表现出胎儿特征。基因组学分析显示,IMO表现出突变负担增加、20号
综上,该研究在胃IMO生物库捕获了肠化生的异质性,确立了20号染色体增益与CMi作为肠化生恶性转化的关键驱动力,为研究早期胃癌转化和化学预防提供了新的理论依据与实验支撑。
原文链接:Gut.2025 Mar 6;74(4):522-538.DOI:10.1136/gutjnl-2024-332594