作者:刘冰怡 谢敏
第一作者单位:华中科技大学同济医学院附属同济医院急诊和危重症医学科
通信作者:谢敏,华中科技大学同济医学院附属同济医院急诊和危重症医学科
引用本文:刘冰怡, 谢敏. 人工智能在呼吸罕见病诊疗中的应用和研究进展[J]. 中华
摘要
随着信息化、智能化进程的不断加快,人工智能(artificial intelligence,AI)在医学领域已逐步从理论研究走向临床实际应用。人工智能具备强大的数据处理与建模能力,能够在大量医学数据中发现潜在规律,辅助疾病的精准诊断、个体化治疗以及患者管理。在罕见病此类传统方法难以高效应对的场景中,人工智能为实现呼吸罕见病管理提供了新的视角和手段。
一、人工智能技术简介
人工智能是一类通过模拟人类智能,通过输入大量数据通过不同的算法从数据中挖掘规律,从而实现智能化决策的技术。
1. 传统机器学习:人工智能在医疗领域的应用早期以传统机器学习为主。支持向量机、随机森林、梯度提升树等经典算法已经广泛应用于医学影像,实验室检查等多模态数据的分析,并在诊断,治疗,预后评估等领域得到了广泛的应用[5, 6]。
2. 深度学习:近年来,深度学习作为机器学习的分支迅速崛起,其核心特征在于模拟人脑神经连接,通过多层神经网络结构对复杂数据进行特征提取和模型构建。深度学习领域目前已开发了多种经典模型。例如,卷积神经网络在医学影像识别分割中表现优异[7];循环神经网络在时序预测和序列分析上有较强表现,常应用于呼吸频率、
与此同时,大语言模型和视觉语言模型如GPT、DeepSeek的出现进一步拓宽了人工智能在医疗中的应用场景。这类模型基于Transformer架构,通过对大规模文本的学习,实现了强大的语言理解和生成能力,在临床诊断,患者管理等领域已有多项应用,展现了颠覆性的潜力[9, 10]。
此外,强化学习、迁移学习、多任务学习等前沿方法也正被引入医疗研究与实践中,为提升模型泛化能力与临床可用性提供技术支撑[11, 12]。
3. 国内外人工智能工具对比:尽管核心算法相通,但人工智能在医疗领域的落地应用因数据资源、监管政策及市场环境的不同,在国内外呈现出部分差异[13, 14, 15]。(表1)

二、人工智能在呼吸罕见病诊治中应用的最新进展
IPF是一种原因不明的慢性进行性纤维化性
1. 生物标志物和诊断模型:人工智能在筛选IPF潜在诊断标志物起到了重要的作用,2024年的一项研究利用机器学习算法分析了1 599例结缔组织病相关
Raghu等[24]在2019年的研究中纳入237例间质性肺病患者,通过经支气管
2. 人工智能构建影像模型在IPF诊断、疗效评估和预后预测中的应用:CT影像在IPF的诊断中扮演着关键角色,人工智能影像分析的引入有助于挖掘IPF患者影像资料中的高维信息如细微的结构改变、纹理特征及动态变化规律等,推动疾病精准诊断的实现[25, 26]。2024年由Imvaria公司开发的人工智能Fibresolve在美国获批,可通过分析CT成像数据进行评分,辅助IPF诊断和病情评估,降低需要肺活检的患者数量,并有多项研究验证了其实用性和有效性(表2)。
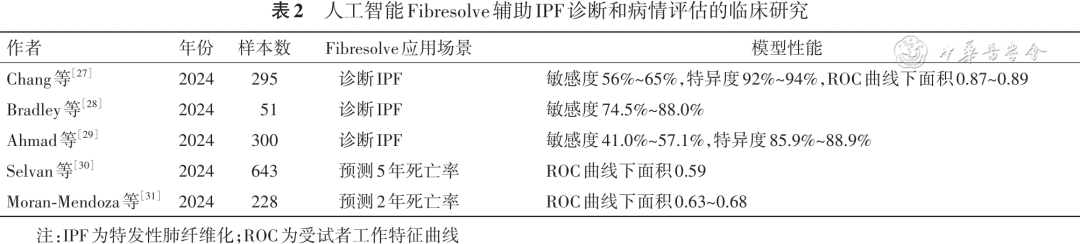
Kim等[32]利用基于机器学习的定量肺纤维化评分评估了IPF患者对LPA1受体拮抗剂的治疗反应,发现肺纤维化定量评分的变化与治疗前后肺功能指标改善显著相关,为临床试验的疗效评估提供了新的影像学人工智能评价手段。
2023年的一项研究中,研究者开发了一种基于胸部X光片的深度学习模型,用于估计肺总量,结果显示该模型预测的肺总量与肺功能检测结果高度一致,并能有效预测IPF患者的生存率,为资源有限地区的疾病管理提供了可行方案[33]。类似地,Thillai等[34]的一项前瞻性研究中利用基于UNet架构的深度学习模型对446例CT影像数据进行自动分割,并量化了肺体积、血管体积和纤维化体积等指标,发现肺体积每增加0.1 L,5年死亡风险降低2%;血管体积每增加0.1 L,5年死亡风险增加37%;纤维化体积每增加0.1 L,5年死亡风险增加17%,可通过定期复查纵向检测上述指标识别疾病进展,进行临床预后评估,辅助制定治疗策略。
3. 治疗药物筛选:人工智能在辅助药物开发方面同样极具潜力,2024年的一项研究中研究者通过机器学习结合分子对接技术,从 TCMSP 数据库筛选出Herbacetin、swertiamarin、vicenin-2等5个经体外证实具有抗IPF潜力的活性成分,为开发新型抗纤维化药物开辟了途径[35]。
CF是一种常
1. 快速汗液收集和测定:CF临床症状复杂多样,诊断困难,其确诊依赖于汗液氯离子检测技术和基因检测,但均具有一定局限性。针对汗液氯离子检测技术耗时长,汗液收集困难的缺陷,Zhou等[37] 结合解吸电喷雾电离质谱和梯度提升决策树机器学习算法,通过分析汗液中的代谢物和脂质特征实现CF诊断,开发了2 min内完成CF患者汗液收集和检测的方法,准确率高达98%,为无创快速诊断CF提供了新的手段。
2. CFTR 基因致病性评估:Lee等[38]开发的CryptSplice算法通过机器学习预测隐性剪接位点激活,成功识别了CFTR中未被注释的致病剪接变异,完善了基因变异的致病性评估,为CF分子诊断提供了重要工具。
3. 影像学评估和分型:Zucker等[39]开发了深度卷积神经网络模型,用于自动完成CF胸部X光片的Brasfield评分,其总分预测与放射科医生接近一致,显著提升了临床工作效率。Campredon等[40]在2022年的研究中纳入了283例CF患者,基于治疗前 CT 的影像组学特征采用k-means 聚类进行无监督机器学习分析,结果显示聚类分析识别的3个形态学亚群中,C群患者的FEV1改善≥5%的比例显著高于其他亚群,有助于预测患者肺功能改善潜力,为CF 患者的个体化治疗决策提供依据。
4. 患者管理:人工智能也为CF患者的自主监测和智能管理提供了更大的可能。2024年Tzavelis等[41]设计了一种微型机械声学传感器,结合卷积神经网络算法,实现了儿童CF患者的
5. 人工智能模型辅助预测预后风险:Alaa van der Schaar[42]开发的自动化机器学习模型通过贝叶斯优化集成多种机器学习算法,基于英国CF注册患者遗传学、肺功能等数据进行训练,预测CF患者3年内死亡、
此外,人工智能还能识别CF常见并发症的风险因素,及时干预并发症高危人群有助于提高CF患者生存率和生存质量[44]。
肺动脉高压是一种血流动力学疾病,其特征是平均肺动脉压升高>25 mmHg,特发性肺动脉高压是动脉型肺动脉高压疾病的特发类型,具有肺血管阻力增加、肺动脉压力进行性升高的特点,可导致右心衰竭甚至死亡[45]。
1. 人工智能辅助组学分析探索疾病异质性:IPAH虽被归为同一疾病类别,但患者在生存预后、治疗反应上存在显著差异,传统临床分类难以精准分层,Kariotis等[46]通过无监督机器学习对全血转录组数据进行分析,将IPAH患者分为预后差异显著的三个亚组型,揭示了IPAH的内部异质性,为个体化治疗策略的制定提供了分析依据。
2. 辅助筛选生物标志物:人工智能可以分析IPAH代谢组学特征,筛选代谢标志物,有助于IPAH的鉴别诊断[47, 48, 49]。Bordag等[50]利用高分辨率质谱和机器学习基于脂质代谢谱开发的可解释的脂质比值模型,诊断IPAH的受试者操作特征曲线下面积达0.90,在揭示脂质代谢紊乱在IPAH肺血管病理重塑中的潜在作用的同时为IPAH的诊断提供了更加智能全面的工具。
Gao等[51]通过机器学习分析了1 121例PAH患者的血清抵抗素水平,发现高抵抗素与6 min步行距离缩短、心脏指数降低及死亡风险升高显著相关,为临床风险分层提供了新工具。
LAM是一种以平滑肌样LAM细胞弥漫性增殖为特征的罕见全身性低度恶性肿瘤疾病,与肺囊性破坏、乳糜液积聚和肾脏血管平滑肌脂肪瘤有关[52]。
1. 生物标志物挖掘:在LAM的分子层面研究中,人工智能正成为挖掘潜在生物标志物和构建精准诊断模型的重要工具。Mustafina等[53]基于呼气挥发性有机物建立了非侵入性诊断模型,利用质子转移反应飞行时间质谱结合极端梯度提升算法筛选出乳酸及质荷比113.13特征离子等关键标志物,模型的受试者工作特征曲线下面积达到0.922,可用于疾病分层及
Kirkpatrick等[54]针对LAM患者蛋白酶失调及酸性微环境的特点,开发了一种尿液蛋白酶活性纳米传感器,借助随机森林算法分析传感器数据区分LAM疾病模型与对照小鼠,并可评估
2. 疾病危险分层和进展预测:LAM患者肺功能变化是其病情监测的重要指标,多项研究用机器学习方法围绕LAM患者FEV1的动态变化构建预测模型,识别出西罗莫司治疗、VEGF-D、肺
Chernbumroong等[57]对359例LAM患者采用无监督机器学习进行聚类分析,得到3个聚类集群,聚类1以气胸和呼吸困难为主,预后最差;聚类2多并发
此外,人工智能还可以通过分析LAM患者CT影像,辅助定性囊性病变性质以及量化肺内受累程度,提供更加便利的鉴别诊断和长期监测手段,通过减少LAM的诊断延迟,评估疾病进展和治疗反应助力临床调整治疗方案,提高患者生存质量[58]。
PAP是一种弥漫性肺部疾病,以肺泡和细支气管腔内充满过碘酸雪夫染色阳性的富磷脂蛋白质样物质为特征[59]。
在PAP的诊疗评估中,传统CT评估主要依赖医师经验判断,存在主观性强、难以精确量化等问题。基于人工智能的CT定量分析技术为此提供了新的解决方案。McCarthy等[60]应用CALIPER软件对一例PAP患者进行自动化肺实质分析,通过无监督聚类算法将肺组织划分为8类放射学模式,用于评估该患者治疗前后疗效。Shi 等[61]在2022年的一项研究中纳入50例PAP患者,采用基于卷积神经网络的CT定量分析方法,评估患者接受他汀类药物治疗前后全肺及各肺叶的磨玻璃影占比的变化,结果显示深度学习量化的磨玻璃影变化与多种关键临床指标的变化显著相关,能更好地反映病情改善与肺功能变化的关联,证实了人工智能在精准诊疗和疗效监测的潜力。
三、人工智能在呼吸罕见病诊治领域的挑战
在监管与支付层面,针对此类工具的伦理审批路径尚未成熟,监管框架仍在完善过程中,加之技术验证体系尚不健全,目前获批的人工智能医疗器械均被归为Ⅲ类高风险器械,面临严格的审批要求和较长的审评周期。同时绝大多数人工智能产品尚未被纳入医保支付范围,缺乏明确的收费路径,均极大地限制了产品的市场渗透率和医院的投资意愿,阻碍了人工智能辅助诊疗工具在临床环境中的实际落地应用[13, 14, 15]。
未来需加强数据标准化与共享机制建设,积极推动多中心学习和联邦学习,完善监管与审批政策,推动医工交叉合作,提升人工智能系统的可解释性与临床适用性。同时构建面向医患的智能信息整合平台,提高人工智能服务的可及性,推动其在实际诊疗中的规范化与普及化。
四、总结
参考文献(略)
