肝移植是终末期肝病最有效的根治性手段。尽管肝脏存在的独特免疫学微环境导致肝移植后排斥反应发生率及严重程度明显低于其他实体器官移植,但排斥反应仍是肝移植术后常见的并发症,发生率约15%-25%,严重影响移植物功能与受者生存。抗胸腺细胞免疫球蛋白是一种纯化的多克隆抗体γ球蛋白混合物,应用于肾移植、肝移植等实体器官移植中的免疫抑制诱导治疗与排斥反应时免疫抑制治疗,以提高移植器官和受者的存活率。中华医学会器官移植学分会肝移植组织专家讨论,总结国内外相关研究最新进展,并结合国际指南和临床实践,详细阐述了抗胸腺细胞免疫球蛋白的作用机制、临床应用场景及使用注意事项,旨在为肝移植受者中抗胸腺细胞免疫球蛋白的临床应用提供指导建议。
肝移植(liver transplantation,LT)是终末期肝病最有效的根治性手段[1,2]。随着外科手术技术、围术期管理体系的发展完善,肝移植受者围术期死亡率明显下降,预后显著改善。但急性排斥反应(acute cellular rejection,AR)发生率仍达15-25%,严重影响移植物生存与受者预后,是亟待解决的临床瓶颈难题[3,4]。尤其是近年来脂肪变性供肝、ABO血型不相容供肝等边缘性供肝临床应用、以及合并肝肾综合征等并发症的危重受者复杂肝移植占比的增加导致AR发生风险进一步升高[5-8]。因此,肝移植受者的免疫抑制方案亟需进行进一步调整、优化以降低AR发生风险。
抗胸腺细胞免疫球蛋白(anti-thymocyte globulin,ATG)是一种主要作用于T淋巴细胞的免疫抑制剂,是免疫抑制方案中重要的组成部分,主要应用于免疫抑制诱导治疗与排斥反应时免疫抑制治疗[9,10]。1963年,Woodruff等发现兔源抗淋巴细胞血清能抑制大鼠的淋巴细胞,并能延长大鼠同种异体皮肤移植物的存活时间[11]。1968年,Starzl报道了ATG类药物应用于肝移植免疫抑制治疗[12]。之后,ATG广泛应用于肾移植、肝移植等实体器官移植免疫抑制治疗中;但目前ATG在肝移植受者中的临床应用尚未形成统一标准。为了规范化肝移植受者中抗胸腺细胞免疫球蛋白的临床应用,中华医学会器官移植学分会肝移植学组组织专家讨论,充分借鉴国内外相关文献,并结合循证医学依据和我国临床实践经验,制定了《中国肝移植受者抗胸腺细胞免疫球蛋白临床应用指南》。本指南的证据级别和推荐强度级别参照英国牛津大学循证医学中心制定的证据分级和推荐强度分类,见表1。
表1 英国牛津大学循证医学中心制定的证据分级和推荐强度标准
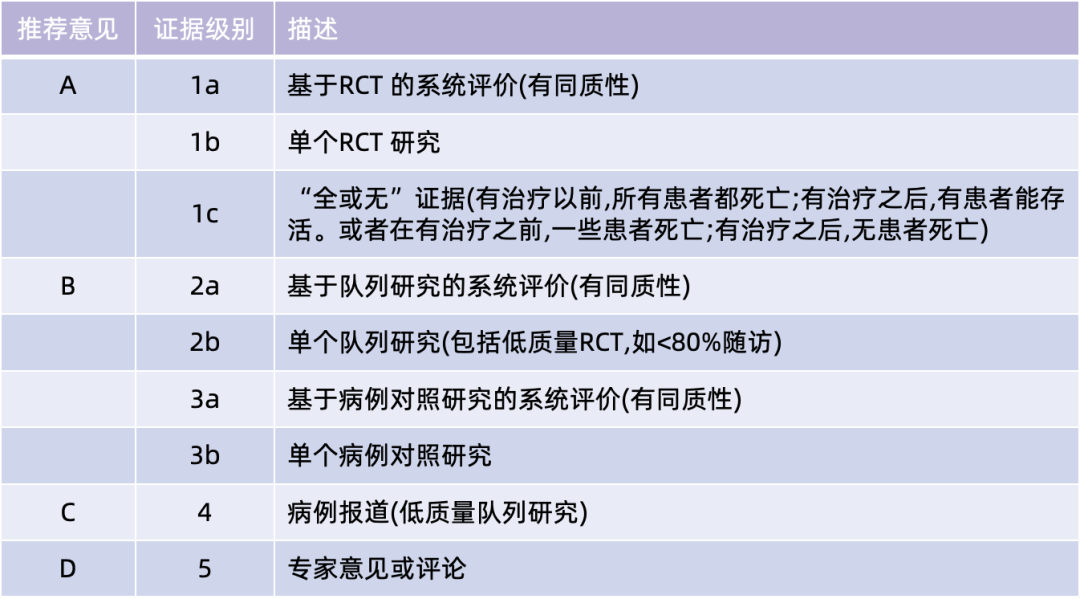
注:RCT:随机对照试验;SR:系统评价
1. 抗胸腺细胞免疫球蛋白的作用机制
抗胸腺细胞免疫球蛋白ATG是一种纯化的多克隆抗体γ球蛋白混合物,从对人胸腺细胞或其他淋巴细胞免疫的动物(如兔、猪、马等)血清中提取获得[9,13,14]。兔抗人胸腺细胞免疫球蛋白(rabbit anti-human thymocyte immunoglobulin,rATG)和猪抗人胸腺淋巴细胞球蛋白(亦称抗人淋巴细胞猪免疫球蛋白)已在国内上市,主要用于免疫排斥反应的预防、治疗等。目前,临床主要应用的ATG制品包括即复宁、ATG-Fresenius等。
ATG可结合不同的抗原决定簇,包括CD3、CD4、CD8、CD25等多种T细胞和B细胞抗原[15]。ATG通过T淋巴细胞耗竭来抑制机体的免疫功能,具体作用机制包括:(1)通过补体依赖的裂解和T细胞凋亡途径耗竭血液和外周淋巴组织中的T细胞;(2)调控白细胞-内皮细胞间互作的关键细胞表面分子;(3)诱导B淋巴细胞的凋亡;(4)干扰树突细胞的功能;(5)诱导调节性和自然杀伤T细胞的产生[9]。
2. ATG在肝移植受者免疫抑制诱导治疗中的应用
免疫抑制诱导治疗是指在移植术前或术后短期加强应用免疫抑制剂以增强对受者免疫系统的抑制,从而预防排斥反应的发生[16]。免疫抑制诱导治疗在肾脏、心脏和肺脏等实体器官移植领域得到了广泛的应用;2021年《中国器官移植发展报告》显示,接受免疫抑制诱导治疗的实体器官移植受者占60.6%。肝移植受者中,免疫抑制诱导治疗占比也呈现出增长的趋势;美国OPTN/SRTR 2022年度数据报告显示,30.4%的成人肝移植受者接受了免疫抑制诱导治疗[3]。
多项研究表明,免疫抑制诱导治疗可有效预防AR,并且是移植物长期存活的独立预后因素[17-19]。一项基于UNOS数据库43,407例肝移植受者的回顾性研究分析了免疫抑制诱导治疗与受者/移植物生存的相关性,结果显示接受免疫抑制诱导治疗的受者5年总体生存率显著优于未接受诱导治疗受者(73% vs. 70%),且5年移植物生存率亦优于未接受治疗受者(68% vs. 64%)[20]。此外,rATG诱导治疗可减轻肝脏缺血-再灌注损伤(ischemia reperfusion injury,IRI),减少钙调磷酸酶抑制剂(calcineurin inhibitor,CNI)使用剂量,并帮助免疫抑制方案向无激素或早期激素撤除方案转变,从而降低肿瘤复发转移、肾功能损伤等相关不良反应的发生[10,21-23]。
2.1 ATG与急性排斥反应
肝移植受者AR的发生受到了移植肝质量、受者基础状态等多种因素影响(表2)。而规范的免疫抑制治疗可有效降低AR发生,提升移植疗效[24-26]。
表2 肝移植受者AR发生的危险因素
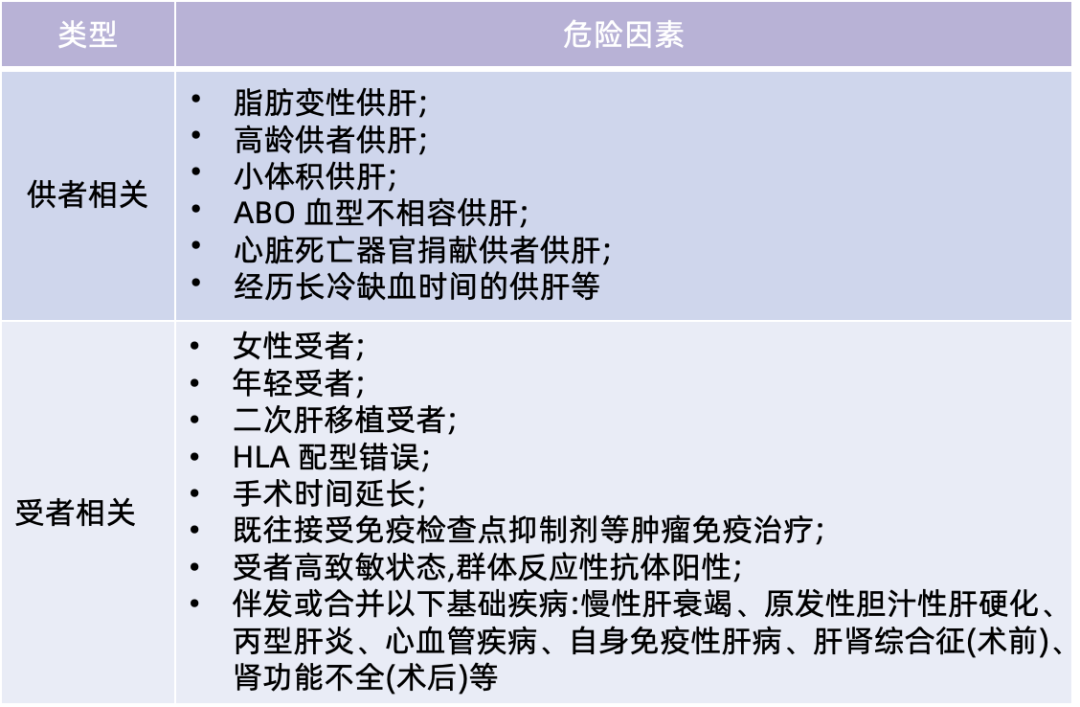
来自美国南卫理公会大学医院的一项前瞻性RCT研究纳入了194例均采用rATG诱导治疗(1.5 mg/kg,首剂于无肝期开始,第2剂为移植后第2天,共用药2次)的肝移植受者,随后分别接受他克莫司或缓释他克莫司联合抗代谢药物的免疫抑制方案,受者总体AR发生率为15.5%,低于同期文献报道[27,28]。另一项回顾性研究(n=391)发现,rATG诱导治疗组(2.5 mg/kg,首剂于移植后6小时开始,连续使用3天,共用药3次)总体1年AR反应发生率为14.5%,显著低于未经rATG诱导治疗组的31.8%;同时研究发现,两组严重AR发生率虽然未见统计学意义,但存在明显差异(3%:12%),需要进一步研究证实[29]。
国际上不同研究团队比较了肝移植受者不同免疫抑制诱导治疗方案的临床获益。来自华盛顿大学的一项回顾性队列研究(n=595)探究了不同免疫诱导方案联合他克莫司和吗替麦考酚酯(mycophenolate mofetil,MMF)的AR发生率。研究结果显示,接受rATG诱导治疗(rATG,1.5 mg/kg/次,首剂于术后第二天开始,在术后的2-5天内共给药3次)受者的AR发生率(18%)显著低于IL-2RA[白介素-2受体拮抗剂(Interleukin 2 receptor antagonists,IL-2RA),20 mg,首剂于移植当天开始,第2剂为移植后第4天,共用药2次]诱导组(27%)[10]。另一项前瞻性随机对照研究纳入了119例成人肝移植受者,分为接受rATG诱导免疫抑制治疗(rATG,1.5 mg/kg,首剂于无肝期开始,第2剂为移植后第1天,共用药2次,n=60)及激素诱导免疫抑制治疗(甲泼尼龙,首剂1000mg,无肝期使用,激素剂量阶梯式降低,术后3月内停止,n=59)。研究显示,rATG组的排斥发生率(25%)低于激素组(31%),且rATG组仅1名需要激素冲击治疗的AR受者;而激素组有9名受者需要进一步激素冲击治疗[30]。国内尚缺少相关的高质量循证医学证据。
肝癌是我国肝移植的主要适应证之一,占比约40%[2];免疫检查点抑制剂(immune checkpoint inhibitors,ICIs)等肿瘤免疫治疗是肝癌肝移植术前重要的降期治疗手段[31,32]。然而,ICIs可增强T细胞介导的细胞免疫,因此可能会增加移植物排斥风险[33-35];而rATG或可作为一种关键的免疫抑制药物用于高危排斥风险受者的围手术期免疫抑制诱导治疗以预防AR的发生。目前相关研究的报道仍较为有限,加利福尼亚大学的一项回顾性研究报道了5例移植前接受纳武利尤单抗治疗的肝癌受者;其中2例受者出现AR,提示了最后一剂ICIs到移植术后的时间可能是排异的关键因素;在仅有的5例中,唯有一例未行rATG诱导治疗的患者出现了严重的免疫介导的肝坏死(大量坏死),并进行了二次移植,其余4例均使用rATG诱导排异,1例出现免疫介导肝坏死(20%),并在后续的rATG治疗中成功避免了二次移植,rATG在这些受者的免疫抑制诱导治疗和AR治疗中发挥了重要的作用[36]。但未来仍需要更高级别的循证医学证据进一步明确rATG在该受者人群中的应用价值。根据《器官移植免疫抑制剂临床应用技术规范(2019版)》,结合国内各移植中心的临床经验,rATG免疫诱导治疗推荐单次剂量为0.4-1.5 mg/kg,首剂用药时间一般为无肝期,共用药2-4次,疗程于移植术后3-7天内结束[10,27,37,38];亦有临床案例和移植中心报道,rATG的首剂使用剂量可加倍,并且首剂用药时间可介于移植术前至术后第2天[10,27,29]。同时,实际临床中应基于不同免疫抑制剂组合方案,结合淋巴细胞计数等实验室检查结果等进行剂量调整,使外周血中CD3+T淋巴细胞占淋巴细胞比例<10%为宜。
推荐意见1:肝移植围手术期可应用抗胸腺细胞免疫球蛋白以预防急性排斥反应发生,并可降低急性排斥反应的严重程度;推荐单次剂量为0.4-1.5 mg/kg,共用药2-4次,疗程于移植术后3-7天内结束,具体剂量及用药频率应根据受者不同免疫抑制方案进行调整(推荐意见:A;证据级别:1b级)。
推荐意见2:对于术前应用免疫检查点抑制剂等存在高危排斥风险的肝移植受者,推荐应用抗胸腺细胞免疫球蛋白等进行免疫抑制诱导治疗(推荐意见:C;证据级别:4级)。
2.2 ATG与移植肝缺血-再灌注损伤
移植肝IRI是指在肝脏移植手术过程中缺血后的肝脏重新得到血液再灌注造成的损伤,作用机制涉及微循环障碍、缺氧、氧化应激和细胞死亡等。IRI可能导致早期移植物功能不全、原发性移植物无功能,甚至移植物衰竭[39,40]。一项随机对照试验探究了rATG在移植肝IRI中的保护作用,22例尸体供肝肝移植受者随机分配至接受rATG诱导治疗组(1.5 mg/kg/次,无肝期,D2,D4使用,用药3次)或未接受诱导治疗组[41]。两组术后3月的移植物与总体存活率均为100%,也均未发生原发性移植物无功能或需要再次移植的情况。但是,接受rATG诱导治疗受者术后丙氨酸氨基转移酶(alanine transaminase,ALT)峰值水平(301±65 mg/dL)较未接受诱导治疗组(1052±330 mg/dL)存在显著差异(P=0.04)。此外,相关研究显示rATG还可通过直接抑制白细胞迁移、下调白细胞表面粘附分子的表达等多重机制减轻IRI引起导致的炎症反应,进而起到保护移植肝的作用[42]。
推荐意见3:应用抗胸腺细胞免疫球蛋白免疫抑制诱导治疗可减轻因缺血-再灌注损伤所导致的炎症反应、移植肝损伤(推荐意见:A;证据级别:1b级)。
2.3 ATG与围术期肾损伤
肝移植术前肾损伤包括肝肾综合征(hepatorenal syndrome,HRS)、病毒性肝炎相关性肾病等,且易在术后进一步恶化发展为慢性肾脏病(chronic kidney disease,CKD)[43-45]。临床研究提示,术前已合并肾损伤的肝移植受者,术后早期采用免疫抑制诱导治疗并联合使用霉酚酸(mycophenolic acid, MPA)类药物(吗替麦考酚酯MMF,500-1000 mg,2次/日;或麦考酚钠EC-MPS,360-720 mg,2次/日)可以在保证免疫抑制强度的同时延迟使用CNI或降低CNI使用剂量,在不增加AR发生风险的同时又可减少肾脏损伤与肾脏替代治疗的使用。一项单中心回顾性临床研究(n=298)比较了接受rATG诱导(总量为7.8±4.6 mg/kg,平均使用8.1±5.4天)和未接受rATG诱导对排斥反应发生率和受者肾功能的影响[23]。结果显示,在rATG诱导组1年移植物无排斥生存率显著优于未接受rATG诱导组的基础上,肾功能较差的受者接受rATG诱导组延迟引入CNI初始应用的时间显著长于未接受rATG诱导组(10.8d vs. 2.4d);同时,与未接受rATG诱导治疗受者(n=67)相比,接受rATG诱导治疗受者(n=231)在移植术后第14、30和180天时的血清肌酐较基线降幅更大。
肝移植术后肾损伤主要包括急性肾损伤(acute kidney injury, AKI)和CKD。由于定义标准和随访时间的不同,文献报道肝移植术后肾损伤发生率差异较大,AKI和CKD的发生率分别为8.0%-81.0%和17.1%-80.0%[46]。其中,含CNI类药物(他克莫司、环孢素等)的免疫抑制方案是发生肝移植后肾损伤的重要危险因素[46,47]。因此,优化免疫抑制方案是肝移植术后肾损伤防治的关键环节。多项研究发现,术后延迟使用CNI或予以低剂量CNI,有助于预防肾损伤发生[46,48]。肝移植受者接受rATG诱导免疫抑制治疗可延迟应用CNI(3-10天)且有效降低CNI使用剂量[23,29,49,50]。一项开放标签、多中心、随机对照II-B期试验,纳入110例肝移植受者(血清肌酐<2 mg/dL);其中,接受rATG(1.5 mg/kg,首剂于移植当天开始,隔天使用,共用药3次)诱导治疗的受者(n=55)术后10天开始应用CNI,未接受rATG诱导治疗的受者(n=55)术后2天内使用CNI。在肝移植后9个月时,接受rATG诱导治疗受者的血肌酐较基线的上升幅度显著更低(P=0.03)[49]。未来的临床研究也值得进一步探索rATG在延迟CNI应用时间(>10天)或采用更低暴露量的CNI中应用的可能性。
推荐意见4:对于术前合并肾功能不全、术后发生肾损伤或易发生肾损伤的肝移植受者,使用抗胸腺细胞免疫球蛋白进行免疫抑制诱导治疗,可延迟使用CNI或减少CNI使用剂量进而保护肾功能(推荐意见:A;证据级别:1b级)。
2.4 ATG与感染性并发症
肝移植后超过50%的受者可能会发生超过1种病原体感染导致的并发症(infectious complication,IC),以细菌感染最为常见,其次为真菌与病毒感染。其中,肝移植术后CMV感染发生率为23-85%,可诱发排异反应;严重感染者可引起器官衰竭甚至死亡[57,58]。一项纳入了34例亲属活体供肝肝移植受者的研究,他克莫司作为免疫维持期治疗用药基础上,分为激素免疫诱导组和rATG联合减量激素免疫诱导组[53]。结果显示,rATG联合减量激素免疫诱导组的CMV发生率低于激素诱导组方案(11.7% vs. 41.1%)。一项前瞻性随机研究[30]纳入了119例肝移植受者,比较了rATG免疫诱导治疗或激素免疫抑制诱导治疗对受者CMV感染的影响,结果显示,rATG组受者的CMV感染发生率显著低于激素诱导组受者(5% vs. 23%)。同时与IL-2RA诱导治疗相比,相关研究显示接受rATG诱导治疗受者的严重细菌、真菌及CMV感染的发生率无显著性差异[54];但其淋巴细胞增殖性疾病的发生率显著更低[10]。同时,与未采用免疫抑制诱导治疗相比,接受rATG诱导治疗并不增加CMV感染的发生率[49]。
丙型肝炎病毒(Hepatitis C Virus,HCV)再感染是影响移植肝和受者长期存活的重要因素[55-57]。临床研究显示,糖皮质激素的应用与移植术后HCV复发率有关[58,59]。一项研究纳入了64例HCV复发的肝移植受者,分为接受rATG(1.5 mg/kg,首剂于无肝期开始,第2剂为移植后第1天,共用药2次)免疫抑制诱导治疗组及激素免疫抑制诱导组,两组均使用他克莫司维持免疫抑制治疗;结果显示,大多数受者(rATG组:74%,激素组:75%)在治疗复发丙肝前3-6个月的活检中仅出现1级炎症;但在严重炎症发生率(2级或以上,组织学活动指数)上,激素组受者发生率为25%,高于rATG联合无激素组(15%)[60]。另一项前瞻性研究也发现,rATG诱导治疗可避免激素的使用并降低HCV复发风险,rATG诱导组中有18例(62%)在移植后出现了HCV复发,而非诱导组中有24例(73%)在移植后出现HCV复发,rATG诱导治疗未增加HCV复发风险[30]。
推荐意见5:肝移植受者可应用抗胸腺细胞免疫球蛋白进行免疫抑制诱导治疗以安全减少或撤除激素,有助于降低激素相关感染性并发症发生风险(推荐意见:B;证据级别:2a级)。
2.5 ATG与移植后新发糖尿病
肝移植受者术后新发糖尿病(post-transplantation diabetes mellitus,PTDM)是常见的术后代谢并发症,发生率为9.8-63.3%,与排斥反应、心血管疾病等不良事件发生率升高相关,显著影响受者的生活质量以及长期生存[61-63]。PTDM的发生受糖皮质激素、CNI类药物使用等多种因素影响[64,65]。其中,糖皮质激素可通过降低葡萄糖敏感性和损害胰岛素分泌导致胰岛β细胞功能障碍,进而诱导胰岛素抵抗、PTDM发生[65]。一项前瞻性随机对照研究提示,采用rATG诱导联合无激素的免疫抑制方案受者的移植后新发糖尿病的发生率显著低于激素逐渐减量组(2% vs. 14%);同时,ATG的应用可有效减少治疗AR所需的激素[30]。
推荐意见6:肝移植受者应用抗胸腺细胞免疫球蛋白免疫抑制诱导治疗或治疗AR时可降低术后激素使用剂量,进而在一定程度上降低术后新发糖尿病的发生风险(推荐意见:B;证据级别:2a级)。
3. ATG在排斥反应时免疫抑制治疗中的应用
排斥反应时免疫抑制治疗是指发生急性细胞介导排斥反应(acute cellular rejection,ACR)、急性抗体介导性排斥反应(acute antibody-mediated rejection,AMR)等AR时,应用大剂量免疫抑制剂或多种免疫抑制剂组合以到达临床缓解。大剂量糖皮质激素(甲泼尼龙等)冲击治疗是目前肝移植受者AR治疗的一线治疗方案;当糖皮质激素冲击治疗无效时,即发生激素抵抗型AR时,可应用抗胸腺细胞免疫球蛋白制剂甚至需再次肝移植[66-68]。韩国延世大学一项回顾性研究共纳入了11名激素抵抗型AR受者,其中10例为急性细胞排斥反应,1例为早期慢性排斥反应,结果显示,接受1次rATG(2.5mg/kg)治疗后,11名患者的中位天冬氨酸氨基转移酶(aspartate aminotransferase,AST)水平从138 IU/L(45-406 IU/L)降至63 IU/L(15-152 IU/L),中位ALT水平在rATG治疗后1天从327 IU/L(57-486 IU/L)降至70 IU/L(32-233 IU/L);治疗1个月后,中位AST、ALT和总胆红素水平显著下降[69]。一项前瞻性研究报告了20例接受rATG治疗的肝移植受者,包括激素抵抗型排斥反应、严重排斥反应以及严重排斥反应合并复发性自身免疫性肝炎;rATG的治疗对上述所有受者均显示出一定临床疗效[经过4天rATG治疗后(1.5mg/kg/d),中位AST从172 U/L(61-1172 U/L)降至34 U/L(11-250 U/L),中位总胆红素从9.1 mg/dL(1.1-38.9 mg/dL)降至1.3 mg/dL(0.6-23.1 mg/dL)][70]。另一项回顾性研究中,13例激素抵抗型肝移植受者中有10名受者接受rATG治疗有效且耐受性良好。rATG可以有效地逆转严重和激素抵抗型排斥反应,可用于糖皮质激素治疗无效的AR的冲击治疗[71]。治疗AR时,rATG的累积剂量(7.5-26.25 mg/kg)和治疗持续时间(5-13天)差异较大,可由移植团队根据受者不同的免疫抑制剂方案,结合移植物活检结果、实验室检查、CD3阳性淋巴细胞计数等进行剂量调整[72]。
推荐意见7:激素抵抗型急性排斥反应可使用抗胸腺细胞免疫球蛋白治疗,具体剂量应根据受者不同的免疫抑制方案,结合移植物活检结果等动态调整(推荐意见:B;证据级别:2a级)。
推荐意见8:肝移植受者发生严重排斥反应或排斥反应合并自身免疫性肝炎复发,可采用含抗胸腺细胞免疫球蛋白的免疫抑制方案(推荐意见:B;证据级别:3a级)。
4. ATG的常见临床不良反应
ATG在肝移植受者中用于免疫抑制诱导治疗和AR治疗中的有效性已初步得到证实,但在临床实践中仍需重视相关的不良反应,以预防并尽早干预不良反应。
4.2.1 免疫相关反应
使用ATG可出现严重的免疫相关反应,包括速发过敏反应或者严重的细胞因子释放综合征[73,74]。如果发生速发过敏反应,必须立即停止滴注,同时必须采取急救措施。对于有rATG过敏史的患者再次使用时,必须慎重斟酌其临床风险和获益后再使用。
4.2.2 感染
ATG主要通过T淋巴细胞耗竭来抑制机体的免疫功能,且常与CNI、MMF等免疫抑制剂联合使用,临床应用过程中,可能会引起过度免疫抑制,进而增加发生细菌、真菌、病毒、原虫等多种类型病原体感染的风险。应仔细监测受者炎症指标及是否发生感染并发症,并采用合适的预防性抗感染治疗。
4.2.3 输液反应
输液反应可能出现在rATG给药后和第一次或第二次单剂输液治疗期间。首次剂量过高以及持续输注时间过长会增加输液反应的发生及其严重程度[75]。因此,采用推荐剂量、选择合适的输液速度(rATG总输液时间不短于4小时,建议首次滴注开始时10滴/分钟,静滴1小时上未观察到不良反应后可适当增加滴速)[76]、预防性使用非甾体类抗炎药物(如异丁苯丙酸、对乙酰氨基酚)、糖皮质激素和/或抗组胺药物(如苯海拉明、异丙嗪)可减少输液反应发生率和严重程度。
4.2.4 血液系统不良反应
rATG的血液系统不良反应主要包括血小板减少症和/或白细胞减少症(特别是淋巴细胞减少症和中性粒细胞减少症)。在排除基础疾病导致的血小板减少和/或白细胞减少、或确定其由使用rATG相关时,建议按照以下方案进行剂量调整:如果血小板计数在50,000-75,000/mm3或者白细胞计数2,000-3,000/mm3须考虑减少用量;如果发生持续、严重的血小板减少(<50,000/mm3)或者白细胞减少(<2,000/mm3),建议认真评估临床获益与潜在风险,可考虑停止使用rATG[77,78]。实体器官移植受者术后,应对监测淋巴细胞不同亚群数量及其占比,并根据CD3淋巴细胞计数调整rATG的剂量[79,80]。
推荐意见9:抗胸腺细胞免疫球蛋白应用期间或者之后,须监测受者白细胞和血小板计数(推荐意见:A;证据级别:1b级)。
推荐意见10:抗胸腺细胞免疫球蛋白治疗期间,应监测关键淋巴细胞亚群占比及数量(推荐意见:B;证据级别:2b级)。
5. 结语
针对不同肝移植受者制定个体化免疫抑制方案对于提升移植疗效至关重要。ATG是一种抗胸腺细胞免疫球蛋白制剂,是肝移植个体化免疫抑制方案的重要组成部分。本临床实践指南针对ATG在肝移植受者免疫抑制诱导治疗及排斥反应时免疫抑制治疗中的临床应用,及各类常见不良反应的判断与处理提供合理建议。但肝移植受者ATG的应用仍有赖于更多大样本、多中心随机对照研究等高级别循证医学证据支持。
参考文献
[1] 中国医师协会器官移植医师分会, 中华医学会器官移植学分会肝移植学组. 中国肝癌肝移植临床实践指南(2021版) [J]. 中华移植杂志(电子版), 2021, 15(06): 321-328.
[2] Ling S, Jiang G, Que Q, et al. Liver transplantation in patients with liver failure: Twenty years of experience from China [J]. Liver Int, 2022, 42(9): 2110-2116.
[3] Kwong A J, Kim W R, Lake J R, et al. OPTN/SRTR 2022 Annual Data Report: Liver [J]. Am J Transplant, 2024, 24(2s1): S176-s265.
[4] Mugaanyi J, Tong J, Lu C, et al. Risk factors for acute rejection in liver transplantation and its impact on the outcomes of recipients [J]. Transpl Immunol, 2023, 76: 101767.
[5] Zhou J, Wei Q, Zheng S, et al. Early allograft dysfunction after liver transplantation with donation after cardiac death donors [J]. Hepatobiliary Surg Nutr, 2019, 8(5): 566-568.
[6] Kim J M, Kim D G, Kim J, et al. Outcomes after liver transplantation in Korea: Incidence and risk factors from Korean transplantation registry [J]. Clin Mol Hepatol, 2021, 27(3): 451-462.
[7] Nemes B, Gaman G, Polak W G, et al. Extended-criteria donors in liver transplantation Part II: reviewing the impact of extended-criteria donors on the complications and outcomes of liver transplantation [J]. Expert Rev Gastroenterol Hepatol, 2016, 10(7): 841-59.
[8] Nair A, Hashimoto K. Extended criteria donors in liver transplantation-from marginality to mainstream [J]. Hepatobiliary Surg Nutr, 2018, 7(5): 386-388.
[9] Mohty M. Mechanisms of action of antithymocyte globulin: T-cell depletion and beyond [J]. Leukemia, 2007, 21(7): 1387-94.
[10] Montenovo M I, Jalikis F G, Li M, et al. Superior Patient and Graft Survival in Adult Liver Transplant with Rabbit Antithymocyte Globulin Induction: Experience with 595 Patients [J]. Exp Clin Transplant, 2017, 15(4): 425-431.
[11] Woodruff M F, Anderson N A. Effect of Lymphocyte Depletion by Thoracic Duct Fistula and Administration of Antilymphocytic Serum on the Survival of Skin Homografts in Rats [J]. Nature, 1963, 200: 702.
[12] Starzl T E, Groth C G, Brettschneider L, et al. Orthotopic homotransplantation of the human liver [J]. Ann Surg, 1968, 168(3): 392-415.
[13] Gharekhani A, Entezari-Maleki T, Dashti-Khavidaki S, et al. A review on comparing two commonly used rabbit anti-thymocyte globulins as induction therapy in solid organ transplantation [J]. Expert Opin Biol Ther, 2013, 13(9): 1299-313.
[14] Padiyar A, Augustine J J, Hricik D E. Induction antibody therapy in kidney transplantation [J]. Am J Kidney Dis, 2009, 54(5): 935-44.
[15] Bonnefoy-Berard N, Vincent C, Revillard J P. Antibodies against functional leukocyte surface molecules in polyclonal antilymphocyte and antithymocyte globulins [J]. Transplantation, 1991, 51(3): 669-73.
[16] 马葵芬, 朱雪娟, 吴寅, et al. 抗体诱导治疗在肝移植中的应用进展 [J]. 中华移植杂志(电子版), 2018, 12(02): 80-85.
[17] Cillo U, Bechstein W O, Berlakovich G, et al. Identifying risk profiles in liver transplant candidates and implications for induction immunosuppression [J]. Transplant Rev (Orlando), 2018, 32(3): 142-150.
[18] Hawksworth J S, Leeser D, Jindal R M, et al. New directions for induction immunosuppression strategy in solid organ transplantation [J]. Am J Surg, 2009, 197(4): 515-24.
[19] Best L M, Leung J, Freeman S C, et al. Induction immunosuppression in adults undergoing liver transplantation: a network meta-analysis [J]. Cochrane Database Syst Rev, 2020, 1(1): CD013203.
[20] Cai J, Terasaki P I. Induction immunosuppression improves long-term graft and patient outcome in organ transplantation: an analysis of United Network for Organ Sharing registry data [J]. Transplantation, 2010, 90(12): 1511-5.
[21] Turner A P, Knechtle S J. Induction immunosuppression in liver transplantation: a review [J]. Transpl Int, 2013, 26(7): 673-83.
[22] Petite S E, Bollinger J E, Eghtesad B. Antithymocyte Globulin Induction Therapy in Liver Transplant: Old Drug, New Uses [J]. Ann Pharmacother, 2016, 50(7): 592-8.
[23] Tchervenkov J I, Tzimas G N, Cantarovich M, et al. The impact of thymoglobulin on renal function and calcineurin inhibitor initiation in recipients of orthotopic liver transplant: a retrospective analysis of 298 consecutive patients [J]. Transplant Proc, 2004, 36(6): 1747-52.
[24] 高伟东, 杨龙龙, 尹清臣. 氧化应激反应在边缘供肝肝移植缺血-再灌注损伤中的作用研究进展 [J]. 器官移植, 2022, 13(01): 126-131.
[25] Martin J D, Cabral H, Stylianopoulos T, et al. Improving cancer immunotherapy using nanomedicines: progress, opportunities and challenges [J]. Nat Rev Clin Oncol, 2020, 17(4): 251-266.
[26] Fisher J, Zeitouni N, Fan W, et al. Immune checkpoint inhibitor therapy in solid organ transplant recipients: A patient-centered systematic review [J]. J Am Acad Dermatol, 2020, 82(6): 1490-1500.
[27] Helmick R A, Eymard C M, Naik S, et al. A report of a prospective randomized trial of extended-release tacrolimus versus immediate release tacrolimus after liver transplantation with anti-thymocyte induction in a steroid free protocol [J]. Clin Transplant, 2024, 38(1): e15172.
[28] Rodriguez-Peralvarez M, Germani G, Papastergiou V, et al. Early tacrolimus exposure after liver transplantation: relationship with moderate/severe acute rejection and long-term outcome [J]. J Hepatol, 2013, 58(2): 262-70.
[29] Soliman T, Hetz H, Burghuber C, et al. Short-term induction therapy with anti-thymocyte globulin and delayed use of calcineurin inhibitors in orthotopic liver transplantation [J]. Liver Transpl, 2007, 13(7): 1039-44.
[30] Eason J D, Nair S, Cohen A J, et al. Steroid-free liver transplantation using rabbit antithymocyte globulin and early tacrolimus monotherapy [J]. Transplantation, 2003, 75(8): 1396-9.
[31] Martin S P, Mehta N, Emamaullee J. Immune checkpoint inhibitors in liver transplantation: Current practice, challenges, and opportunities [J]. Liver Transpl, 2024, 30(7): 742-752.
[32] Tabrizian P, Abdelrahim M, Schwartz M. Immunotherapy and transplantation for hepatocellular carcinoma [J]. J Hepatol, 2024, 80(5): 822-825.
[33] Jadlowiec C C, Taner T. Liver transplantation: Current status and challenges [J]. World J Gastroenterol, 2016, 22(18): 4438-45.
[34] Llovet J M, Castet F, Heikenwalder M, et al. Immunotherapies for hepatocellular carcinoma [J]. Nat Rev Clin Oncol, 2022, 19(3): 151-172.
[35] Pinter M, Scheiner B, Pinato D J. Immune checkpoint inhibitors in hepatocellular carcinoma: emerging challenges in clinical practice [J]. Lancet Gastroenterol Hepatol, 2023, 8(8): 760-770.
[36] Schnickel G T, Fabbri K, Hosseini M, et al. Liver transplantation for hepatocellular carcinoma following checkpoint inhibitor therapy with nivolumab [J]. Am J Transplant, 2022, 22(6): 1699-1704.
[37] 中华医学会器官移植学分会肝移植学组. 器官移植免疫抑制剂临床应用技术规范(2019版) [J]. 器官移植, 2019, 10(03): 213-226.
[38] Halldorson J B, Bakthavatsalam R, Montenovo M, et al. Differential rates of ischemic cholangiopathy and graft survival associated with induction therapy in DCD liver transplantation [J]. Am J Transplant, 2015, 15(1): 251-8.
[39] Liu J, Man K. Mechanistic Insight and Clinical Implications of Ischemia/Reperfusion Injury Post Liver Transplantation [J]. Cell Mol Gastroenterol Hepatol, 2023, 15(6): 1463-1474.
[40] Ito T, Naini B V, Markovic D, et al. Ischemia-reperfusion injury and its relationship with early allograft dysfunction in liver transplant patients [J]. Am J Transplant, 2021, 21(2): 614-625.
[41] Bogetti D, Sankary H N, Jarzembowski T M, et al. Thymoglobulin induction protects liver allografts from ischemia/reperfusion injury [J]. Clin Transplant, 2005, 19(4): 507-11.
[42] Guirado L. Does Rabbit Antithymocyte Globulin (Thymoglobuline(R)) Have a Role in Avoiding Delayed Graft Function in the Modern Era of Kidney Transplantation? [J]. J Transplant, 2018, 2018: 4524837.
[43] Angeli P, Garcia-Tsao G, Nadim M K, et al. News in pathophysiology, definition and classification of hepatorenal syndrome: A step beyond the International Club of Ascites (ICA) consensus document [J]. J Hepatol, 2019, 71(4): 811-822.
[44] Parajuli S, Foley D, Djamali A, et al. Renal Function and Transplantation in Liver Disease [J]. Transplantation, 2015, 99(9): 1756-64.
[45] Hussaini T, Yoshida E M, Partovi N, et al. Early Persistent Progressive Acute Kidney Injury and Graft Failure Post Liver Transplantation [J]. Transplant Direct, 2019, 5(3): e429.
[46] 中华医学会器官移植学分会, 中国医师协会器官移植医师分会. 中国肝移植受者肾损伤管理临床实践指南(2023版) [J]. 中国医学前沿杂志(电子版), 2024(08): 1-13.
[47] Raja K, Panackel C. Post Liver Transplant Renal Dysfunction-Evaluation, Management and Immunosuppressive Practice [J]. J Clin Exp Hepatol, 2024, 14(2): 101306.
[48] Zhou J, Zhang X, Lyu L, et al. Modifiable risk factors of acute kidney injury after liver transplantation: a systematic review and meta-analysis [J]. BMC Nephrol, 2021, 22(1): 149.
[49] Nair A, Coromina Hernandez L, Shah S, et al. Induction Therapy With Antithymocyte Globulin and Delayed Calcineurin Inhibitor Initiation for Renal Protection in Liver Transplantation: A Multicenter Randomized Controlled Phase II-B Trial [J]. Transplantation, 2022, 106(5): 997-1003.
[50] Bajjoka I, Hsaiky L, Brown K, et al. Preserving renal function in liver transplant recipients with rabbit anti-thymocyte globulin and delayed initiation of calcineurin inhibitors [J]. Liver Transpl, 2008, 14(1): 66-72.
[51] Razonable R R. Cytomegalovirus infection after liver transplantation: current concepts and challenges [J]. World J Gastroenterol, 2008, 14(31): 4849-60.
[52] Sampathkumar P, Paya C V. Management of cytomegalovirus infection after liver transplantation [J]. Liver Transpl, 2000, 6(2): 144-56.
[53] Masetti M, Montalti R, Arpinati M, et al. High dose rabbit antithymocyte globulin induction in living related liver transplantation [J]. Hepatogastroenterology, 2007, 54(75): 884-8.
[54] Kamar N, Borde J S, Sandres-Saune K, et al. Induction therapy with either anti-CD25 monoclonal antibodies or rabbit antithymocyte globulins in liver transplantation for hepatitis C [J]. Clin Transplant, 2005, 19(1): 83-9.
[55] Joshi D, Pinzani M, Carey I, et al. Recurrent HCV after liver transplantation-mechanisms, assessment and therapy [J]. Nat Rev Gastroenterol Hepatol, 2014, 11(12): 710-21.
[56] Howell J, Angus P, Gow P. Hepatitis C recurrence: the Achilles heel of liver transplantation [J]. Transpl Infect Dis, 2014, 16(1): 1-16.
[57] Fagiuoli S, Ravasio R, Luca M G, et al. Management of hepatitis C infection before and after liver transplantation [J]. World J Gastroenterol, 2015, 21(15): 4447-56.
[58] Vivarelli M, Burra P, La Barba G, et al. Influence of steroids on HCV recurrence after liver transplantation: A prospective study [J]. J Hepatol, 2007, 47(6): 793-8.
[59] Samonakis D N, Germani G, Burroughs A K. Immunosuppression and HCV recurrence after liver transplantation [J]. J Hepatol, 2012, 56(4): 973-83.
[60] Nair S, Loss G E, Cohen A J, et al. Induction with rabbit antithymocyte globulin versus induction with corticosteroids in liver transplantation: impact on recurrent hepatitis C virus infection [J]. Transplantation, 2006, 81(4): 620-2.
[61] Zhang Z, Sun J, Guo M, et al. Progress of new-onset diabetes after liver and kidney transplantation [J]. Front Endocrinol (Lausanne), 2023, 14: 1091843.
[62] Ling Q, Xu X, Xie H, et al. New-onset diabetes after liver transplantation: a national report from China Liver Transplant Registry [J]. Liver Int, 2016, 36(5): 705-12.
[63] Lv C, Zhang Y, Chen X, et al. New-onset diabetes after liver transplantation and its impact on complications and patient survival [J]. J Diabetes, 2015, 7(6): 881-90.
[64] Trinanes J, Rodriguez-Rodriguez A E, Brito-Casillas Y, et al. Deciphering Tacrolimus-Induced Toxicity in Pancreatic beta Cells [J]. Am J Transplant, 2017, 17(11): 2829-2840.
[65] Chevallier E, Jouve T, Rostaing L, et al. pre-existing diabetes and PTDM in kidney transplant recipients: how to handle immunosuppression [J]. Expert Rev Clin Pharmacol, 2021, 14(1): 55-66.
[66] Charlton M, Levitsky J, Aqel B, et al. International Liver Transplantation Society Consensus Statement on Immunosuppression in Liver Transplant Recipients [J]. Transplantation, 2018, 102(5): 727-743.
[67] 中华医学会器官移植学分会. 中国肝移植免疫抑制治疗与排斥反应诊疗规范(2019版) [J]. 中华移植杂志(电子版), 2019, 13(04): 262-268.
[68] 张晋平, 朱志军, 孙丽莹, et al. 抗胸腺细胞球蛋白治疗肝移植术后耐激素急性排斥反应1例报告并文献复习 [J]. 精准医学杂志, 2022, 37(05): 396-399+403.
[69] Lee J G, Lee J, Lee J J, et al. Efficacy of rabbit anti-thymocyte globulin for steroid-resistant acute rejection after liver transplantation [J]. Medicine (Baltimore), 2016, 95(23): e3711.
[70] Schmitt T M, Phillips M, Sawyer R G, et al. Anti-thymocyte globulin for the treatment of acute cellular rejection following liver transplantation [J]. Dig Dis Sci, 2010, 55(11): 3224-34.
[71] Bijleveld C G, Klompmaker I J, Van Den Berg A P, et al. Incidence, risk factors, and outcome of antithymocyte globulin treatment of steroid-resistant rejection after liver transplantation [J]. Transpl Int, 1996, 9(6): 570-5.
[72] Palmer W C, Taner C B, Keaveny A P, et al. Antithymocyte Globulin Use for Corticosteroid Nonresponsive Rejection After Liver Transplantation [J]. Transplant Proc, 2018, 50(10): 3606-3614.
[73] Soleimanpour S A, Sekiguchi D R, Larosa D F, et al. Hypersensitivity to rabbit antithymocyte globulin in an islet transplant recipient: a case report [J]. Transplant Proc, 2011, 43(9): 3302-6.
[74] De Pietri L, Serra V, Preziosi G, et al. Perioperative effects of high doses of intraoperative thymoglobulin induction in liver transplantation [J]. World J Transplant, 2015, 5(4): 320-8.
[75] Sevrin F, Gonzales F, Machuron F, et al. Antithymocyte globulin in pediatric allogeneic hematopoietic stem cell transplantation: Infusion time and tolerability [J]. Pediatr Transplant, 2020, 24(4): e13694.
[76] 褚静茹, 杨滢, 刘育蕾, et al. 兔抗人胸腺细胞免疫球蛋白治疗肝移植术后急性排斥的观察与护理 [J]. 天津护理, 2015, 23(06): 491-492.
[77] Hardinger K L. Rabbit antithymocyte globulin induction therapy in adult renal transplantation [J]. Pharmacotherapy, 2006, 26(12): 1771-83.
[78] Burkhalter F, Schaub S, Bucher C, et al. A Comparison of Two Types of Rabbit Antithymocyte Globulin Induction Therapy in Immunological High-Risk Kidney Recipients: A Prospective Randomized Control Study [J]. PLoS One, 2016, 11(11): e0165233.
[79] Furlanetto G, Alegretti A P, Farias M G, et al. Cut-off value for absolute lymphocytes as an alternative for the immunophenotypic analysis of CD3+ T cells in the monitoring of immunosuppressive therapy with thymoglobulin [J]. J Bras Nefrol, 2017, 39(2): 181-185.
[80] Rasander R O, Sorensen S S, Krohn P S, et al. Interruption of anti-thymocyte globuline treatment in solid organ transplantation is effectively monitored through a low total lymphocyte count [J]. Front Immunol, 2024, 15: 1419726.

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)