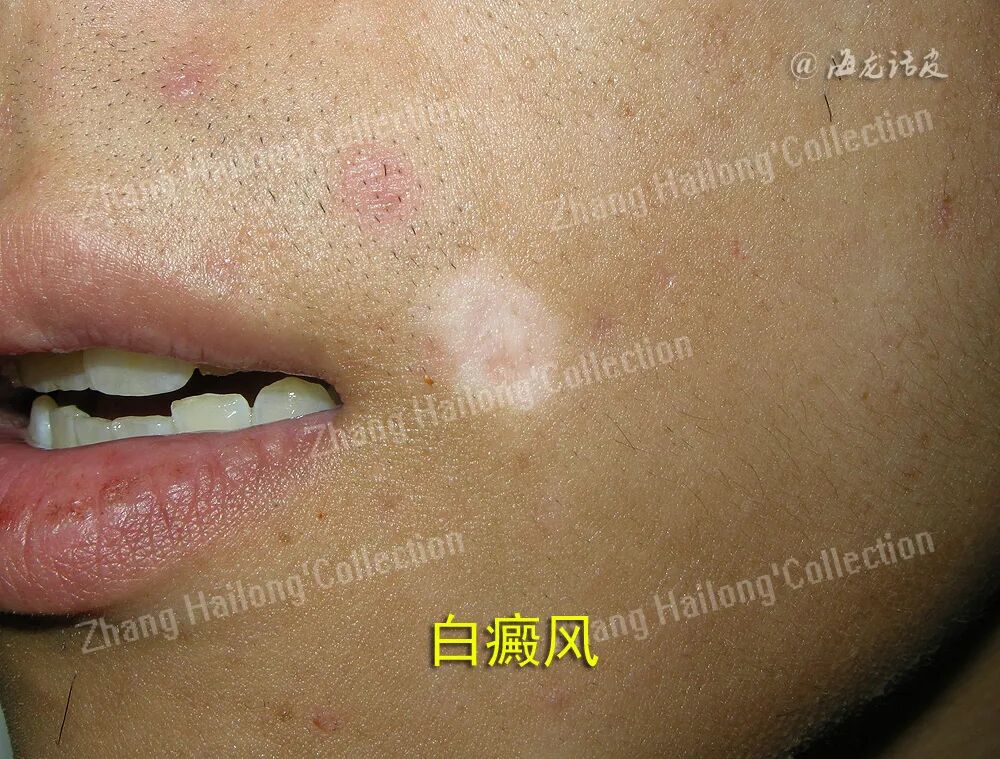
近年来,氧化应激对MCs的损伤机制不断被拓展。除凋亡、焦亡等经典途径外,其他氧化应激参与的调节性细胞死亡形式也逐渐被关注。铁死亡作为一种由铁依赖性脂质过氧化驱动的调节性细胞死亡形式,其分子调控网络与氧化应激损伤机制存在显著关联。临床研究中观察到白癜风患者铁死亡标志物异常,且铁死亡抑制剂在体外实验中展现出保护效应,提示铁死亡可能作为黑素细胞丧失的重要机制。
1.铁死亡的机制
Dixon等于2012年研究发现,铁死亡诱导剂Erastin可以特异性地诱导一种依赖于铁的新型细胞死亡形式,并将此类细胞死亡形式命名为“铁死亡(ferroptosis)”,其生化特征表现为细胞内铁蓄积、ROS水平上升和脂质过氧化。铁死亡的主要机制涉及铁代谢紊乱、脂质过氧化物的产生以及抗氧化系统的失衡。
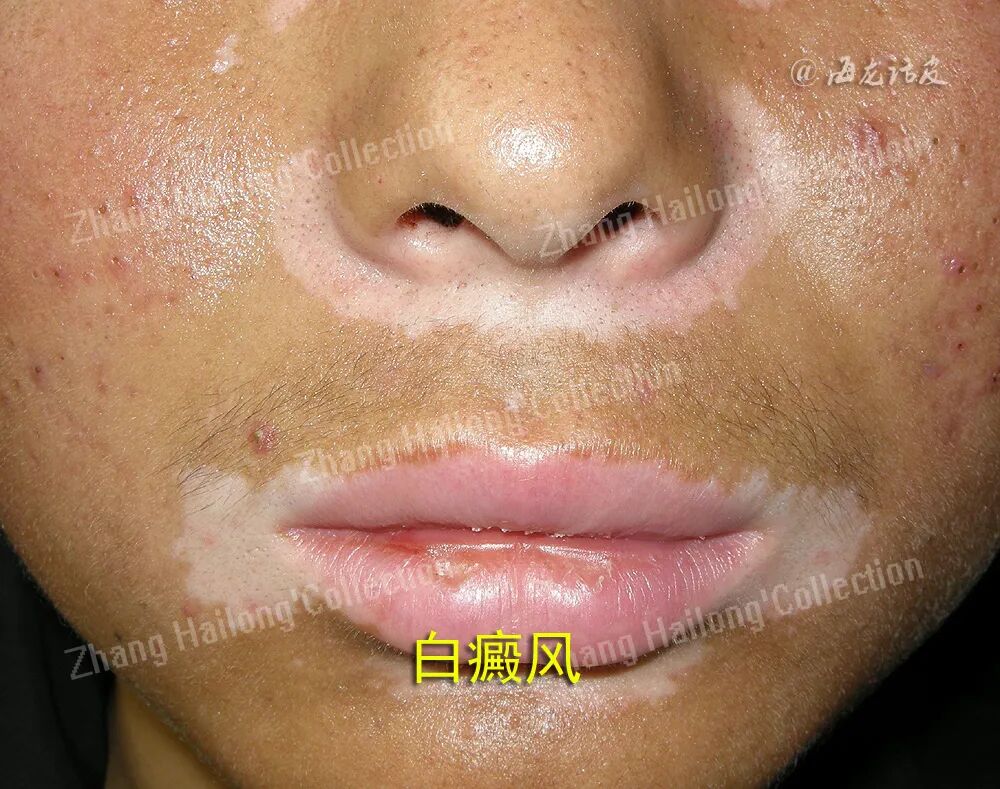
1.1.铁代谢紊乱引起游离铁蓄积与ROS生成:
铁稳态失衡是铁死亡的基本特征。细胞中游离铁的蓄积会诱导铁死亡的发生,多种参与铁离子转运和存储的蛋白均参与铁死亡的发生与发展。铁元素主要经转铁蛋白(transferrin,TRF)和转铁蛋白受体(transferrin receptor 1,TFR1)运送至细胞内,并以铁蛋白(ferritin)的形式储存和运输。铁蛋白主要由铁蛋白轻链(FTL)和铁蛋白重链1(FTH1)组成。核受体共激活因子4(nuclear receptor coactivator 4,NCOA4)可通过介导铁蛋白自噬释放游离铁。铁外排蛋白(ferroportin,FPN)是调节铁离子出胞的转运蛋白,对抑制铁死亡的发生具有重要作用。 游离态的Fe2+可通过芬顿反应(Fenton reaction)产生Fe3+和ROS,进而诱导铁死亡。
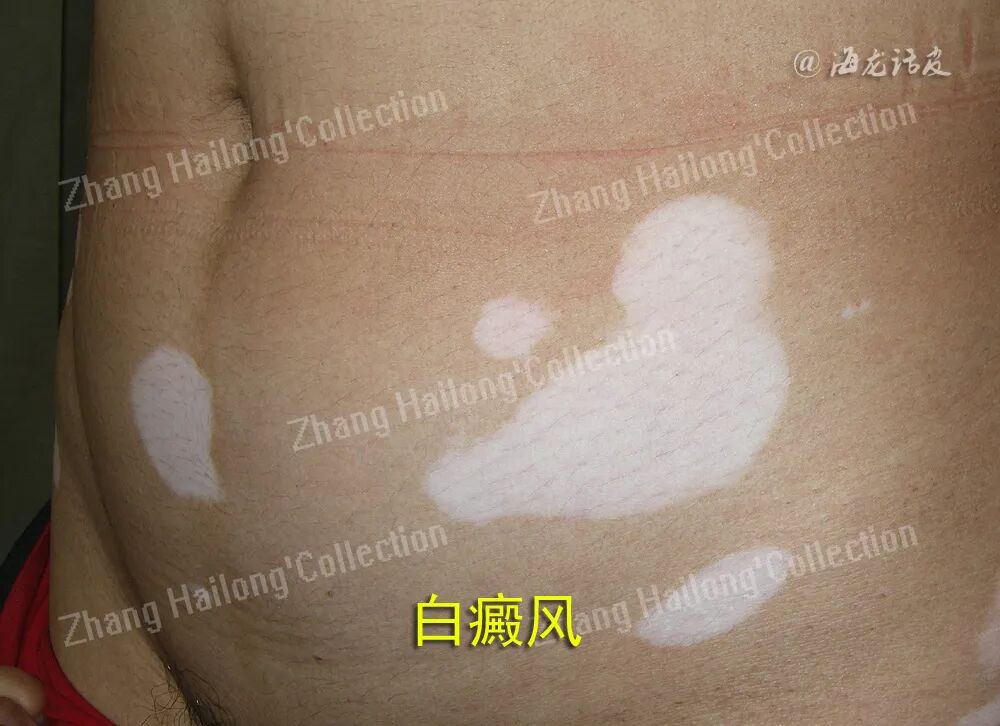
1.2.脂质过氧化是铁死亡的最终执行者:
含多不饱和脂肪酸的磷脂(PL-PUFA)可在富含铁和ROS的条件下发生过氧化,生成特异性脂质过氧化物,进而破坏嵌于双层磷脂膜的蛋白质等生物大分子,改变膜的流动性和完整性。脂质过氧化物的降解产物[如丙二醛(MDA)和4-羟基壬烯醛]可破坏细胞内的蛋白质和核酸等生物大分子。以上作用使得生物膜的脆性增加、细胞功能减退,最终促发细胞铁死亡。长链脂酰
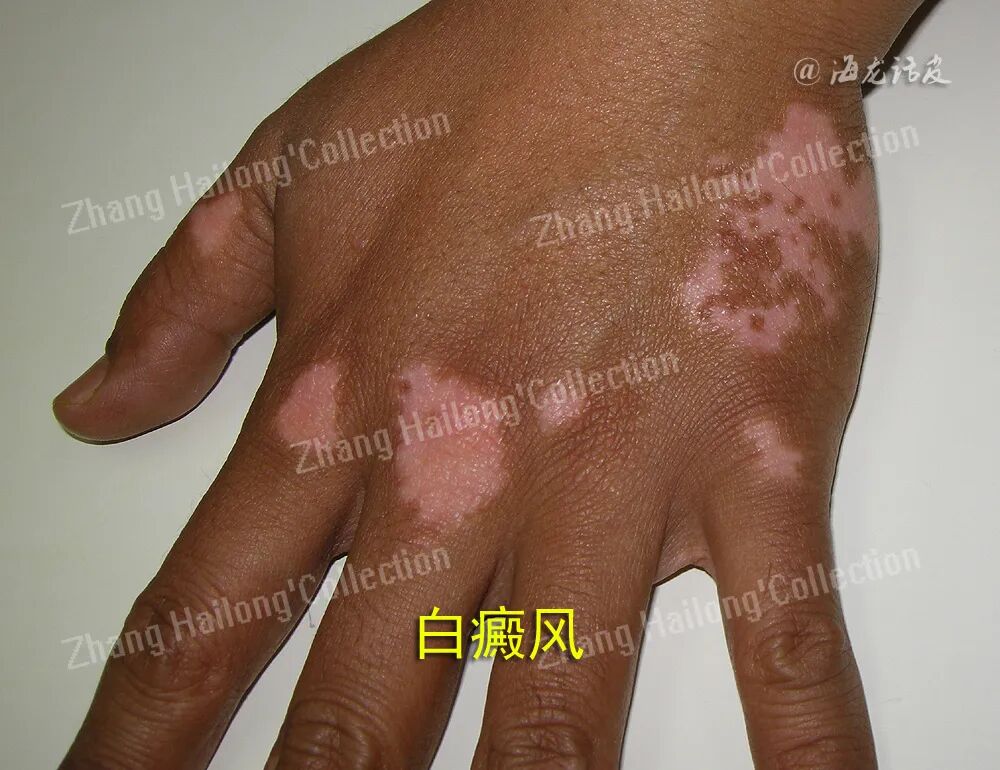
1.3.GPX4 等抗氧化系统对铁死亡的负向调控:
2.铁死亡在白癜风发病机制中的作用
2.1.铁死亡参与白癜风进展:
相较于角质形成细胞,黑素细胞内铁蓄积及DNA氧化水平更为显著,而GSH水平较低。白癜风患者黑素细胞中自发性的ROS生成和膜脂质过氧化增加,血清硬脂酸、泛酸等差异代谢物浓度异常提示不饱和脂肪酸合成代谢通路紊乱,其中硬脂酸、
白癜风患者黑素细胞中ACSL4及TFR1等铁死亡标志物表达上调且多数患者(7/10)黑素细胞具有较低的铁死亡抑制基因评分,少数患者(1/10)具有较高的铁死亡驱动基因评分,提示抑制基因功能缺失可能是导致铁死亡的核心因素,而非驱动基因的过度活跃。进展期白癜风患者血清铁代谢指标呈现血清铁与铁蛋白水平显著降低、TRF水平升高的特征性改变,而稳定期白癜风患者上述铁代谢指标无显著改变。组织学分析证实,稳定期白癜风患者皮损部位 TFR1表达显著上调,而GPX4和FTL表达水平较低,非皮损区皮肤亦存在类似趋势,提示铁死亡可能作为全身性病理改变参与白癜风进展。
2.2.IFN-γ介导的免疫-铁死亡交互作用网络:
CD8+T细胞分泌的干扰素-γ(IFN-γ)是决定白癜风进展的核心物质,白癜风患者皮损区IFN-γ表达升高,可诱导趋化因子CXC配体9(CXCL9)和CXCL10的分泌,进而促进高表达趋化因子受体3(CXCR3)的自身反应性T细胞迁移至白癜风皮损处。IFN-γ还可调节转录激活因子1(STAT1)的磷酸化,磷酸化的STAT1(p-STAT1)上调干扰素调节因子1(IRF1)的表达,进而促进ACSL4的转录,加剧脂质过氧化。此外,p-STAT1可直接结合SLC7A11转录起始位点抑制其转录。上述机制共同作用诱导黑素细胞铁死亡。铁死亡导致的ROS过量产生进一步导致皮肤免疫稳态失衡,促进白癜风的发展。特异性阻断IFN-γ信号可有效恢复黑素细胞功能稳态并逆转其铁死亡。上述发现揭示了免疫微环境与MCs铁死亡机制间的交互作用,为开发靶向IFN-γ的铁死亡调控策略提供了分子理论基础。
2.3.表观遗传调控黑素细胞铁死亡:
通过生物信息学分析,鉴定出8个白癜风特异性差异表达的铁死亡相关基因(DE-FRGs):核糖核苷二磷酸还原酶亚基 M2(RRM2)、组织蛋白酶B(CTSB)、OUT去泛素化酶1(OUTB1)、α-突触核蛋白(SNCA)、脂质运载蛋白2(LCN2)、脂氧合酶5(ALOX5)、 白介素33(IL-33)、溶质载体家族1成员4(SLC1A4)。这些基因涉及铁代谢重编程、脂质过氧化调控及免疫微环境重塑,构成白癜风铁死亡调控网络的核心分子枢纽。
表观遗传机制在黑素细胞铁死亡中发挥关键作用。黑素细胞特异性RNA结合蛋白(RBP)基因(如SLC3A2)在白癜风中呈现显著表达异常,SLC3A2下调导致细胞内Fe2+/ROS 蓄积、抗氧化酶(SOD/GSH/GPX4)活性丧失及脂质过氧化标志物(MDA/COX2)升高,最终触发铁死亡级联反应。该发现揭示了表观转录调控在铁死亡进程中的关键作用。转录组学研究表明,白癜风患者
3.基于铁死亡的白癜风治疗策略
已有研究证实,铁死亡诱导剂(如Erastin、RSL3)及中波紫外线(UVB)可通过显著提升MCs内Fe2+/ROS水平驱动铁死亡,而铁死亡抑制剂Ferrostatin-1(Fer-1)可有效拮抗此类损伤。多种中草药活性成分,例如:黄芩素、沙苑子苷、地黄梓醇、和厚朴酚、山柰酚、
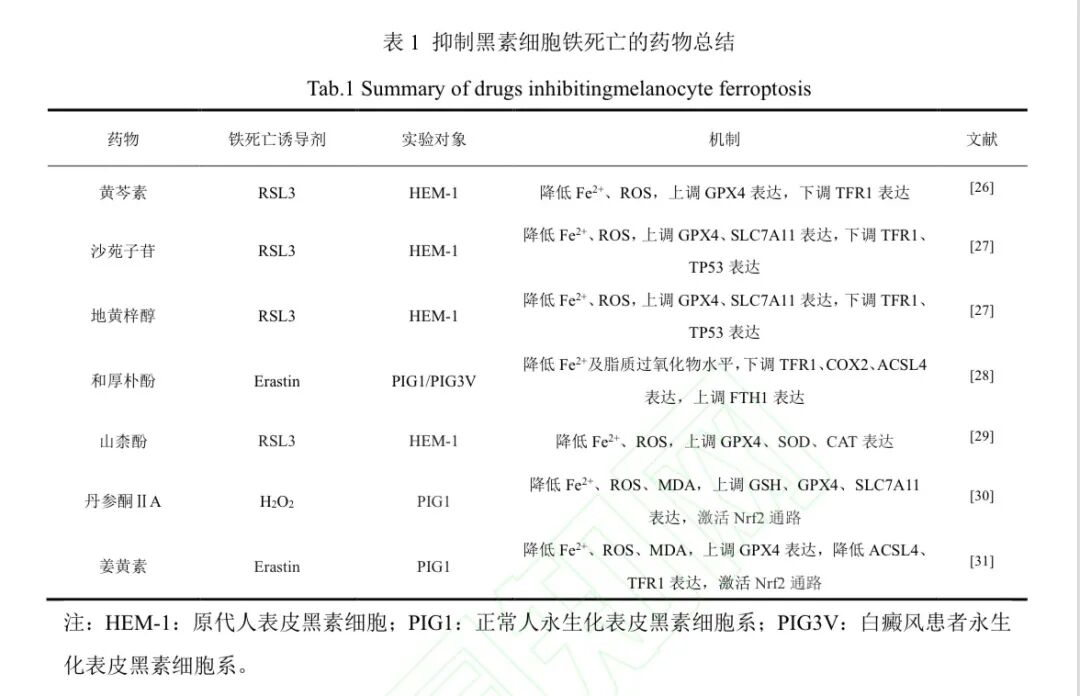
Nrf2通路作为调控氧化应激和铁代谢的核心调控因子,其介导铁死亡抑制的机制研究日益深入。研究表明,
4.小结与展望
目前白癜风的发病机制尚未完全阐明,已有诸多证据表明铁死亡参与其病理进程。白癜风患者黑素细胞内ROS蓄积可引发氧化应激及铁依赖性脂质过氧化进而诱导铁死亡。尽管目前已通过体外实验初步证实抗氧化剂对黑素细胞的保护效应,但仍缺乏
参考文献:
1.闫恒硕,顾飞雪,孙浩森,魏国黑素细胞铁死亡在白癜风发病机制及治疗中的研究进展[J/OL].中国皮肤性病学杂志. 2016,1(8).
2.李倩雯, 雷铁池. 介导氧化应激的Nrf2信号通路在白癜风发病和治疗中的研究进展[J]. 中国医药导报, 2024, 21(28): 53-57.
3.马冰砚, 董丽萍, 陆晓云, et al. 基于LC-MS非靶向代谢组学分析进展期白癜风血清代谢物差异[J].中国皮肤性病学杂志, 2023, 37(06): 652-656.
4.其他文献略。
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
