提 要
伴有远处转移的胰腺癌晚期病例,预后极差,传统上被视为手术禁忌。本文详述1例59岁女性胰尾癌伴肝转移患者的诊疗历程。患者初诊时肿瘤负荷大,且侵犯多处重要血管。经过长达11周期的系统性化疗,先后采用改良FOLFIRINOX、FOLFIRINOX及NALIRIFOX方案,并入组PD⁃L1/CTLA⁃4双特异性抗体免疫治疗临床试验,实现了显著的肿瘤降期(原发灶缩小逾40%,
全文阅读
超过半数胰腺癌患者初诊时已发生转移,其中肝脏是最常见的转移部位。目前,对于转移性胰腺癌的转化治疗策略、手术时机选择及远期生存情况,仍缺乏高质量的循证医学证据。现有病例系列研究虽报道了经高度筛选的患者在接受化疗与切除术后可获得18~56个月的总生存期,但这些数据存在人群异质性大、转移灶手术方案不统一且报道不详等问题。哪些转移性胰腺癌患者能够真正从转化手术中获益,目前尚无定论。本文报道1例初诊为胰腺癌伴多发肝转移患者,在海军军医大学第一附属医院(上海长海医院)胰腺肿瘤多学科团队的诊治下,经两轮转化治疗后达到无瘤状态并实现长期生存。本案例报道旨在为此类患者的临床决策提供参考。
第1次转化治疗病程
一、病例介绍
患者女性,59岁。因“新冠病毒感染后出现乏力、纳差2月余,伴中上腹隐痛、饱胀及进行性体重下降(2个月内下降约10 kg)”于2023年3月入院。患者无
1.临床检查:入院后完善胰腺动脉增强CT造影(contrast⁃enhanced CT of the pancreatic arteries, CTA)检查,结果显示,胰尾部可见一巨大不规则软组织肿块,大小约7.2 cm×4.8 cm,与胃后壁、左肾上极、左侧肾上腺及脾门结构分界不清,考虑肿瘤直接侵犯。肿块与腹腔干动脉、肝总动脉、脾动脉、胃十二指肠动脉及肠系膜上静脉、脾静脉接触范围均超过180°,提示血管受累严重。肝脏左叶见多发低密度转移灶。此外,影像学还提示右肾小囊肿、脾脏楔形梗死及
实验室检查示CA19‑9 7594.3 U/ml, CEA 35.71 ng/ml, CA242 499.59 U/ml, CA50>180 U/ml, CA72‑4 15.4 U/ml, CA125 134.7 U/ml。炎症指标CRP 53.8 mg/L。肝肾功能基本正常,电解质及凝血功能无显著异常。
为明确病理诊断,于2023年3月21日行超声内镜引导下细针穿刺活检(endoscopic ultrasound⁃guided fine‑needle aspiration, EUS‑FNA),胰腺病灶穿刺物病理提示:胰尾部低分化腺癌,部分区域疑有腺鳞癌成分。为确认肝脏病灶性质,于2023年3月24日行CT引导下肝脏穿刺活检,术后病理提示:肝脏腺癌,结合免疫组织化学染色结果,高度支持为胰胆管来源。至此,“胰尾低分化腺癌(cT4N0M1, Ⅳ期)伴同步肝转移”的诊断得以明确。
2.治疗经过与反应:基于晚期胰腺癌一线治疗指南及患者一般状况,于2023年4月15日起开始系统性治疗。一线治疗方案为PD⁃L1/CTLA4双特异性抗体联合改良FOLFIRINOX方案。完成4周期治疗后,复查评估显示肿瘤标志物下降不明显,遂将方案调整为PD⁃L1/CTLA4双抗联合标准FOLFIRINOX方案。该阶段治疗共计4周期,期间患者出现Ⅲ度骨髓抑制,经
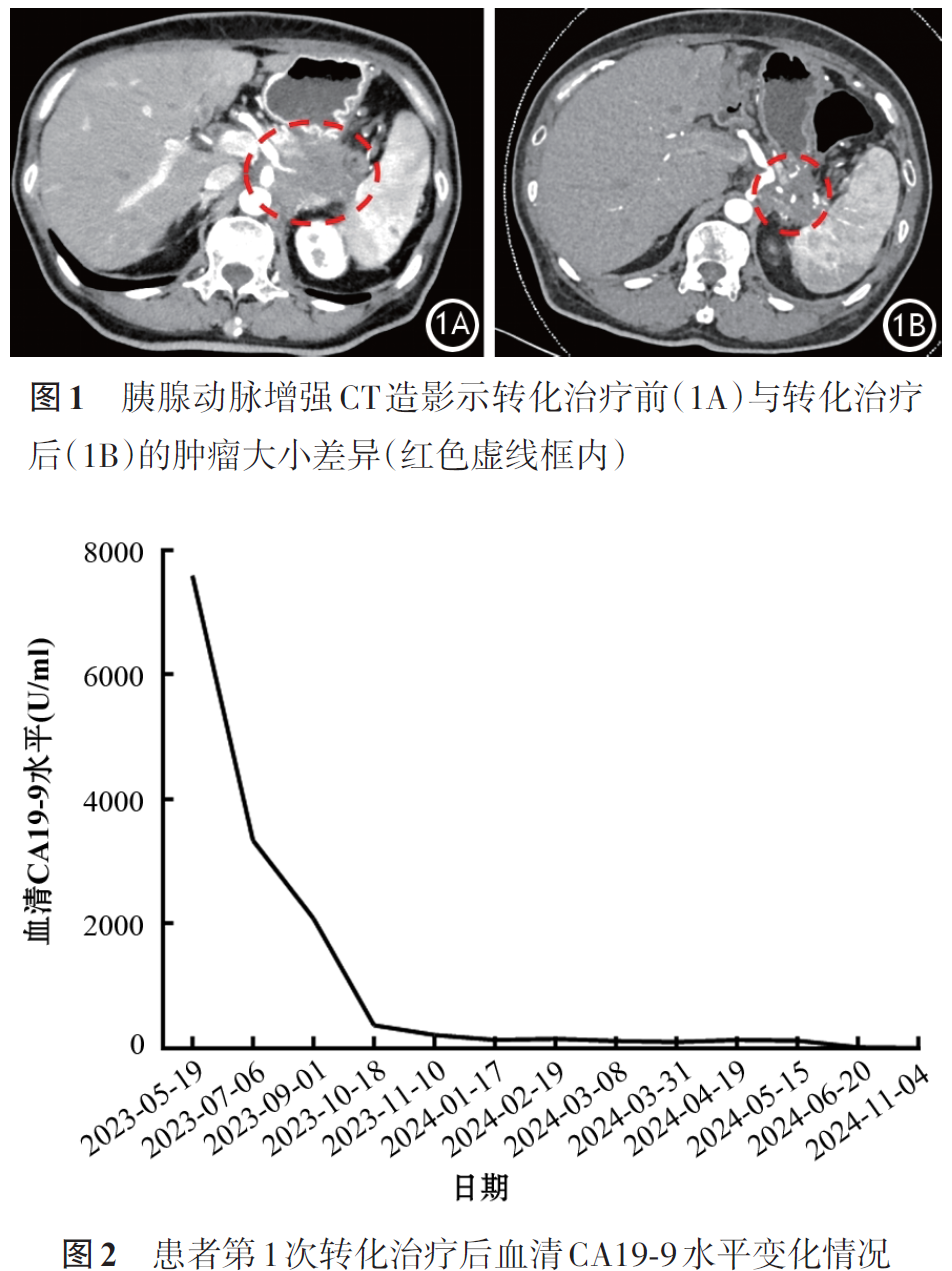
3.转化治疗后评估:经过近1年转化治疗后,于2024年4月25日对患者进行全面再评估。CTA显示,胰尾部原发肿瘤显著缩小至4.2 cm×3.0 cm(图1),与周围血管的侵犯关系较前改善;肝脏转移灶亦明显缩小、减少。肿瘤标志物显著下降,CA19⁃9降至120.54 U/ml(较基线下降约98.4%)(图2),CEA降至11.68 ng/ml,其他标志物亦有不同程度回落。根据实体瘤疗效评价标准1.1(response evaluation criteria in solid tumors 1.1, RECIST 1.1),疗效评价为部分缓解;美国东部肿瘤协作组(Eastern Cooperative Oncology Group, ECOG)评分为0分。患者虽食欲、睡眠仍较差,但体重稳定,无手术绝对禁忌证。
二、多学科协作诊断和鉴别诊断
针对此例复杂病例,长海医院组织了包括胰腺外科、消化内科、影像科、病理科在内的胰腺肿瘤多学科诊疗小组进行讨论。
胰腺外科金钢主任医师:患者“胰尾癌伴肝转移”诊断明确,诊断依据充分。根据化疗前穿刺病理结果提示为低分化导管腺癌,免疫组织化学染色显示p40、CK5及p63均为阴性,可初步判定该患者为经典样型胰腺癌。该亚型胰腺癌具有侵袭性较弱的生物学行为,通常预后较好。值得注意的是,新辅助化疗后部分患者的分子分型可能发生改变。因此,仍需依据术后病理的免疫组织化学染色结果,进一步制定后续辅助化疗方案。
影像科方旭副主任医师:从影像学角度看,CTA与PET⁃CT均高度支持胰腺导管腺癌伴肝转移。其特征包括胰尾不规则、浸润性生长的肿块,呈“乏血供”表现,延迟期可有轻度强化;与周围多支重要血管关系密切,呈“嵌壁”或“包绕”征象;肝脏转移灶表现为FDG代谢增高的实性结节。经过有效转化治疗后,影像学的改善是评估手术可行性的重要客观依据,包括肿瘤尺寸缩小、与血管界限变得清晰、转移灶活性降低等。
病理科蒋慧副主任医师:穿刺活检标本的组织学检查是胰腺癌诊断的“金标准”。本例患者EUS⁃FNA胰腺病灶穿刺物镜下见不规则、成角的腺管结构及实性癌巢,浸润于促纤维结缔组织增生的间质中,细胞异型性显著,核分裂易见,符合低分化腺癌的诊断。免疫组织化学染色显示CK7、CK19、CA19⁃9阳性,而SMAD4表达缺失,这一特征强烈支持胰腺导管腺癌的诊断,并有助于与
三、初步诊断
胰尾低分化腺癌(cT4N0M1, Ⅳ期)伴肝转移(转化治疗后),2型糖尿病
四、多学科协作诊疗计划
胰腺外科金钢主任医师:核心问题为对于初始不可切除的转移性胰腺癌患者,在经历长周期转化治疗并取得显著疗效后,是否应行手术治疗?根据美国国立综合癌症网络(National Comprehensive Cancer Network, NCCN)等国际指南,胰腺癌伴发远处转移首选全身系统治疗,一般不推荐根治性手术。然而,近年来“转化治疗”理念兴起,即通过有效的术前化疗,使初始不可切除或转移性肿瘤降期,从而为部分高度筛选的患者创造手术机会。笔者团队前期研究发现,对转化治疗反应极佳(如肿瘤标志物大幅下降、影像学显著缓解)的寡转移性胰腺癌患者,行原发灶与转移灶的同步根治性切除,其中位生存期可延长至32.6个月,远优于单纯化疗。本例患者CA19⁃9降幅超过80%,肿瘤缩小明显,且体能状态良好,提示其肿瘤生物学行为相对良好,可能从积极手术中获益。鉴于肿瘤仍侵犯周围组织,计划行“开腹根治性胰腺次全切除术+胃部分切除术+结肠部分切除术+左肾上腺切除术+左半肝切除术+腹膜后淋巴结清扫术”。
胰腺外科郭世伟副主任医师:该患者术前接受了长达近1年的系统性治疗。现有临床证据表明,对于晚期胰腺癌患者,延长新辅助治疗周期至6~8个月甚至更长时间,可有助于实现更深度的肿瘤降期及更有效地控制微转移灶。本例患者序贯接受了改良FOLFIRINOX、标准FOLFIRINOX及NALIRIFOX方案化疗,并入组PD⁃L1/CTLA⁃4双特异性抗体治疗临床试验,累计达11周期。治疗后评估显示,其肿瘤标志物水平显著下降,原发灶与肝转移灶体积明显缩小,尽管按照传统解剖学标准仍未完全达到可切除范畴,但综合其优异的治疗反应,提示其肿瘤生物学行为较为良好。当前,胰腺癌的治疗理念已从单纯解剖学可切除性评估,逐步演进为结合肿瘤生物学行为及治疗反应的综合评估体系。基于此理念,认为该患者具备尝试根治性手术切除的指征。
在精准医疗方面,患者来源的类器官药物敏感性测试是近年来的重要技术进展。该技术通过体外三维培养患者肿瘤组织,模拟体内微环境,从而直接评估不同化疗方案的杀伤效果。研究显示,类器官药敏模型预测临床疗效的准确性可达80%~90%,为个体化辅助化疗方案的选择提供了有力工具。然而,该技术目前仍存在一定局限,其培养成功率约60%,尚需在培养基优化与标准化方面进一步改进。此外,建议对该患者进行二代测序,以明确其基因变异谱。尽管胰腺癌靶向治疗机会相对有限,但如检出BRCA1/2等同源重组修复通路基因突变,可能提示其对铂类药物或PARP抑制剂敏感;而如存在错配修复蛋白缺陷或高度微卫星不稳定性,则可能预示其对免疫检查点抑制剂治疗有效。因此,建议在术后获取肿瘤组织标本,同步开展类器官药敏测试与基因检测,旨在为后续辅助治疗策略的制定提供双重依据,实现真正意义上的个体化治疗。
消化内科王云峰副主任医师:术前应优化患者营养状态,控制血糖。该患者在化疗期间出现了骨髓抑制症状,但经过积极对症治疗,目前各项指标包括肝功能、肾功能均恢复正常。由于考虑到术中要进行左半肝切除,所以建议在围术期继续进行保肝治疗,以防肝功能严重受损。
五、诊治经过
2024年5月17日,由金钢主任医师主刀,行预定手术。术中探查未见腹腔种植或其他远处转移灶。由于肿瘤与腹腔干动脉、胃及结肠粘连紧密,成功施行了动脉鞘剥脱、胃大部切除及结肠部分切除。完整切除胰腺原发灶、受侵的左肾上腺、部分胃与结肠,以及包含转移灶的左半肝。术后大体标本送检。病理报告确认所有切缘均为阴性。最终诊断:中至低分化胰腺导管腺癌,局灶为未分化癌,伴肝脏多发转移。经病理学评估,肿瘤细胞退变、坏死明显,肿瘤退缩比率约80%,肿瘤治疗反应分级为美国病理学家学会(College of American Pathologists, CAP)2级、安德森癌症中心(M.D. Anderson Cancer Center, MDA)2级。患者术后恢复顺利,无胰瘘、出血等严重并发症。
六、术后辅助治疗方案选择及随访
鉴于患者术后
第2次转化治疗病程
一、病例介绍
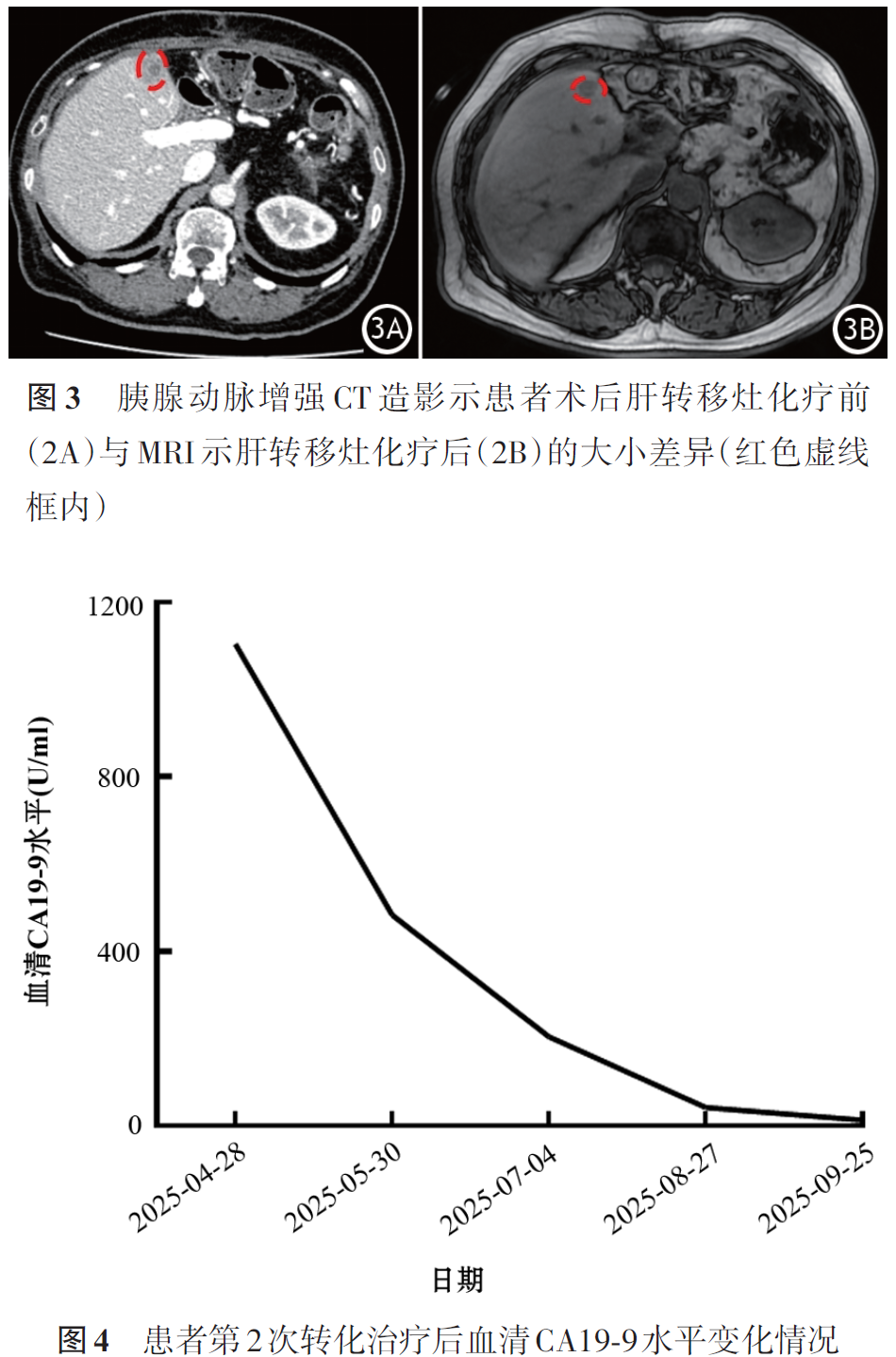
该患者于2025年4月15日复查,CTA提示胰腺术后改变,术区少许渗出,左半肝缺如,右肝前叶见一直径约20 mm低强化灶,考虑肝内转移瘤可能。血清肿瘤标志物CA19⁃9升高至1104.61 U/ml。2025年4月28日再次行EUS⁃FNA,肝脏转移灶组织病理学结果仍提示胰腺来源的低分化导管腺癌。重复类器官
二、初步诊断
胰腺癌术后肝转移(转化治疗后),2型糖尿病。
三、多学科协作诊疗计划
胰腺外科金钢主任医师:约80%的胰腺癌患者在术后5年内出现复发或转移,其中肝脏是最常见部位。根据NCCN指南,肝转移一般以全身系统治疗为主,手术切除不作为常规推荐。然而,近年部分研究表明,对于化疗反应良好、病灶控制稳定的部分患者,二次切除转移灶可能会带来生存获益。本例患者经过4周期的NALIRIFOX转化治疗后,肿瘤标志物降至正常,影像学评估为稳定疾病,因此行肝转移灶切除有望延长生存,建议施行
胰腺外科郭世伟副主任医师:该患者影像学显示肝转移灶数量、直径均较前相仿,未见新发病灶,根据RECIST 1.1,符合疾病稳定标准。同时病理组织免疫组织化学结果显示p40、CK5均为阴性,支持其分子分型仍倾向于经典样型胰腺癌,提示肿瘤生物学行为未发生显著恶化。鉴于未见肝外转移,同意行转移灶切除。
消化内科王云锋副主任医师:患者既往曾行左半肝切除并接受多轮化疗,但目前肝功能指标基本正常。建议在围术期加强保肝治疗,以降低手术对肝功能的影响。
四、诊治经过
患者于2025年9月12日行腹腔镜探查,术中超声探及肝右叶3枚转移灶,直径1~2 cm,未见腹腔种植或其他远处转移。遂施行腹腔镜下肝部分切除+肠粘连松解术。术后病理证实为胰腺癌肝转移,切缘阴性。患者术后恢复顺利,无并发症,按期出院。
五、术后辅助治疗方案选择及随访
鉴于患者术后病理检查和类器官药敏测试结果,选择卡培他滨+奥拉帕利方案进行辅助化疗。截至本报告撰写时,患者术后定期随访,生活质量尚可,未见新发转移征象。
小 结
本文介绍了1例经过两次转化治疗后达到无瘤状态并长期生存的胰腺癌伴发肝转移的多学科协作诊疗病例。患者在经过两轮独立的转化治疗后,分别接受了原发灶与转移灶的根治性切除,并最终实现无瘤状态。这一诊疗过程提示对于伴发肝转移的胰腺癌患者,单次的转化治疗及根治性手术可能不足以清除所有的微转移灶,这或许是导致术后早期复发的重要原因。因此“序贯性转化治疗”可为一种积极的治疗策略,即在首次根治性手术后,不应视治疗终结,而应为患者预备并实施再次的系统性转化治疗,彻底清除潜在的微转移灶,从而突破传统治疗模式的瓶颈,追求分子层面的疾病清除与更持久的无瘤生存。本例患者的诊疗过程集中体现了目前胰腺癌治疗中的几个关键进展与思考。(1)转化治疗在晚期胰腺癌中的价值:对于初始不可切除的局部晚期或转移性胰腺癌,化疗(如FOLFIRINOX、NALIRIFOX)为基础的转化治疗已显示出巨大潜力。本例通过长达14个月的持续治疗,实现了深度的肿瘤降期和肿瘤标志物下降,为后续根治性手术创造了条件。这提示对于选择性患者,治疗周期不应机械地局限于4~6个月,而应基于治疗反应和耐受性进行个体化调整。(2)多学科协作的核心作用:从诊断的确立、转化治疗方案的选择、手术时机的把握到复发后的管理,每一个环节都离不开多学科协作的综合研判。影像科提供了精确的解剖学评估,病理科确认了诊断并指导了潜在靶点探索,内科与外科共同制定了贯穿始终的治疗策略。多学科协作是成功实施此类复杂诊疗模式的基石。(3)手术角色的再定义:本例挑战了“胰腺癌肝转移是手术绝对禁忌”的传统观念。在对转化治疗反应极佳的寡转移患者中,积极的外科干预可能会给患者带来显著的生存获益。决策依据应从单纯的“解剖学可切除性”转向结合“肿瘤生物学行为(治疗反应、肿瘤标志物动态变化)”的综合评估。(4)精准医学与个体化治疗:类器官药敏测试在本例术后辅助治疗和复发后治疗选择中起到了关键的指导作用。尽管肿瘤最终复发,但药敏测试指导下的化疗有效地控制了疾病进展,为二次手术创造了机会。这展示了功能性精准医学在优化治疗序列、克服耐药方面的应用前景。(5)复发转移灶的积极处理:胰腺癌术后肝转移复发率高,治疗棘手。本例在系统治疗基础上,对再次局限的肝转移灶行二次切除,患者仍获得了生存获益,表明对于生物学行为相对惰性的复发灶,积极的局部治疗策略仍值得考虑。
综上所述,通过多学科协作模式,采用强效、持续的转化治疗方案,并对治疗反应良好的选择性胰腺癌肝转移患者实施积极的根治性手术,有望突破传统治疗瓶颈,为部分晚期患者带来长期生存的机会。未来需要更多前瞻性研究以明确最佳转化治疗方案、治疗持续时间以及筛选可能获益患者的生物标志物。