许多成人癌症是由于几十年累积的环境毒素和基因突变导致。但儿童癌症不同,它们通常发生在生命的最早期——甚至在胎儿发育阶段就开始了。一种被称为
近日,来自纽约西奈山伊坎医学院的 Wagenblast博士 领衔的研究团队在 Cancer Discovery 发表上题为 Ontogeny Dictates Oncogenic Potential, Lineage Hierarchy, and Therapy Response in Pediatric Leukemia 的文章,揭示了一个关键发现:白血病发生的“时机”与“突变”同样重要。 研究人员发现,即使是完全相同的基因突变,如果在胎儿发育早期发生,其恶性程度和对药物的反应将截然不同于在出生后发生的白血病。这项研究不仅解释了为什么某些

这项研究构建了一个精妙的实验,将致癌突变(NUP98::NSD1)分别引入到三个不同发育阶段的人类造血干细胞中:
胎儿肝脏(Fetal Liver, FL):代表生命最早期的造血环境。
脐带血(Cord Blood, CB):代表出生时的造血环境。
成人骨髓(Adult Bone Marrow, BM):代表成熟后的造血环境。
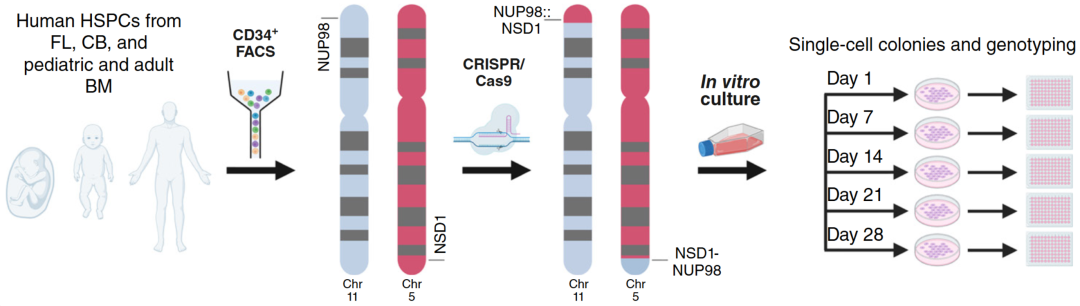
下面的柱状图直观地展示了结果——只有胎儿(FL)来源的细胞在基因编辑后迅速生长(蓝色/红色柱子很高),而成人骨髓(Adult BM)来源的细胞几乎没有反应。
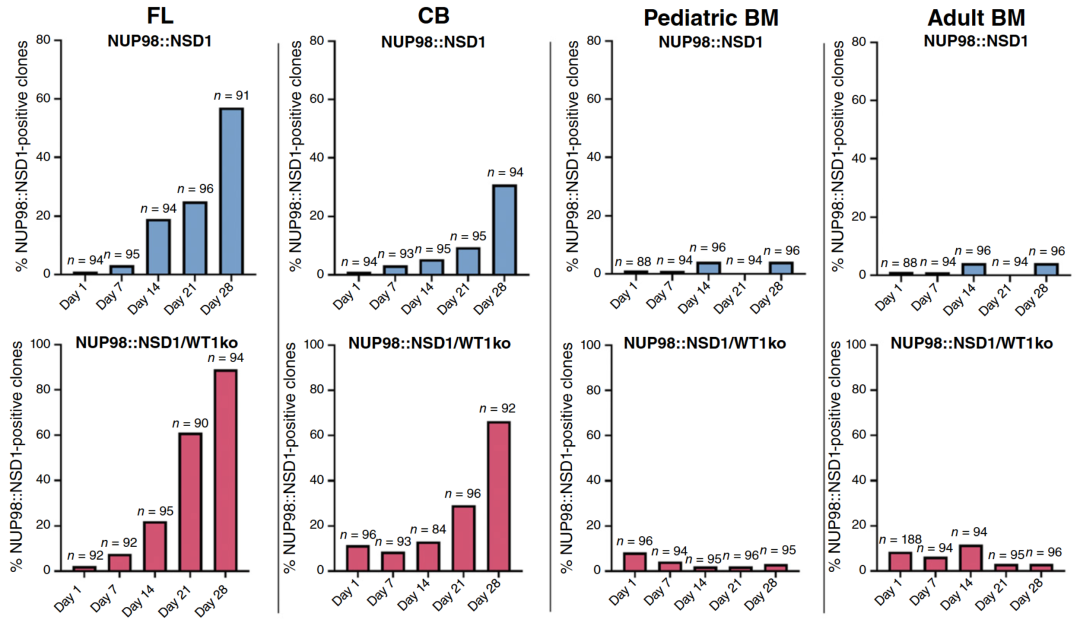
胎儿细胞最易癌变: NUP98::NSD1突变能迅速将胎儿肝脏细胞转化为白血病细胞,并具有极强的生长优势。
成人细胞具有“免疫力”: 同样的突变,如果发生在成人骨髓细胞中,几乎无法引发白血病。
结论: 细胞的“出身”(发育起源)决定了它是否会癌变。这种白血病是一种具有显著“发育特异性”的疾病,主要发生在胎儿和出生后早期窗口。
在临床上,NUP98::NSD1 白血病患者常常同时伴有 WT1基因的缺失或突变。研究证实,WT1 突变就像是一个“助燃剂”:
临床上,这类白血病不仅对传统化疗耐药,对目前热门的靶向药——Menin抑制剂(如Revumenib)也经常无效。研究揭示了背后的机制:
细胞在 “休眠”:来自胎儿起源的白血病干细胞处于一种深度 “静止” 或 “休眠” 状态(Quiescence)。化疗药物通常针对快速分裂的细胞,因此对这些 “沉睡” 的恶性细胞束手无策。
独特的代谢方式:这些细胞不依赖普通的能量来源,而是高度依赖脂肪酸氧化(Fatty Acid Oxidation)和氧化磷酸化(OXPHOS)来生存。
耐药机制:WT1的缺失会导致抗炎机制被激活,并改变了细胞对Menin抑制剂的反应路径,使其产生耐药性。
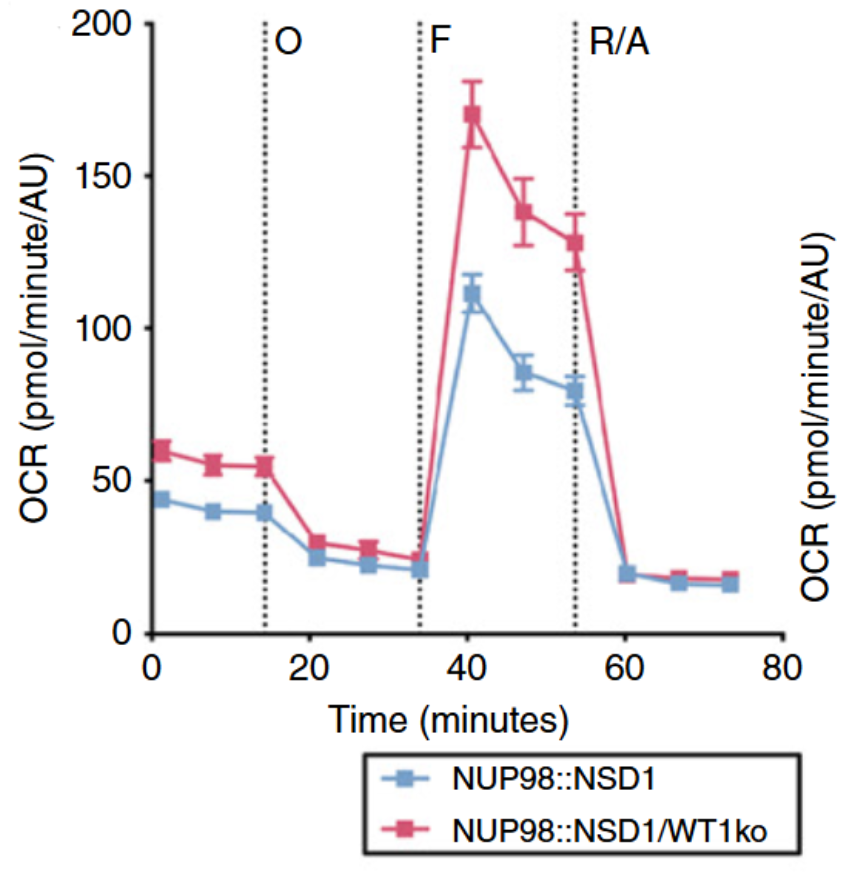
上图展示了线粒体耗氧率(OCR)的测定曲线。图中可以看到 NUP98::NSD1/WT1ko 细胞的曲线(红色)远高于对照组,非常形象地展示了这些癌细胞的“能量代谢”是多么旺盛。
“胎儿致癌特征”评分: 研究人员定义了一套由100个基因组成的“胎儿致癌特征”(Fetal-Oncogenic Signature)。在NUP98::NSD1白血病患者中,该特征评分越高,患者的生存率越低。这比单纯看年龄更能预测风险。
CD52作为替代指标: 基因测序可能比较复杂,但研究发现细胞表面标记物 CD52 可以作为一个简便的“代理指标”。CD52在那些源自胎儿、预后较差的白血病细胞表面高表达。这是一个现成的临床流式细胞术检测指标,医生可以直接利用它来识别高危患者。
研究团队在分子层面找到了控制这一切的“总开关”——一个名为PRDM16的基因。
这就暴露了一个巨大的治疗机会:这些恶性细胞为了生存,极度依赖BCL2蛋白。
基于上述发现,研究人员测试了维奈克拉(Venetoclax),这是一种BCL2抑制剂(即一种能阻断细胞抗死亡机制的药物)。主要机制是联合治疗迫使耐药细胞更加依赖氧化磷酸化代谢,从而使它们对维奈克拉更加敏感。
实验结果令人振奋:
精准打击:维奈克拉能有效杀灭那些由于胎儿起源和WT1突变而高度恶性的白血病干细胞,而对健康造血干细胞影响较小。
联合用药效果更佳:虽然单独使用化疗或Menin抑制剂效果不佳,但如果将维奈克拉与它们联合使用,可以近乎完全地清除体内的白血病细胞。
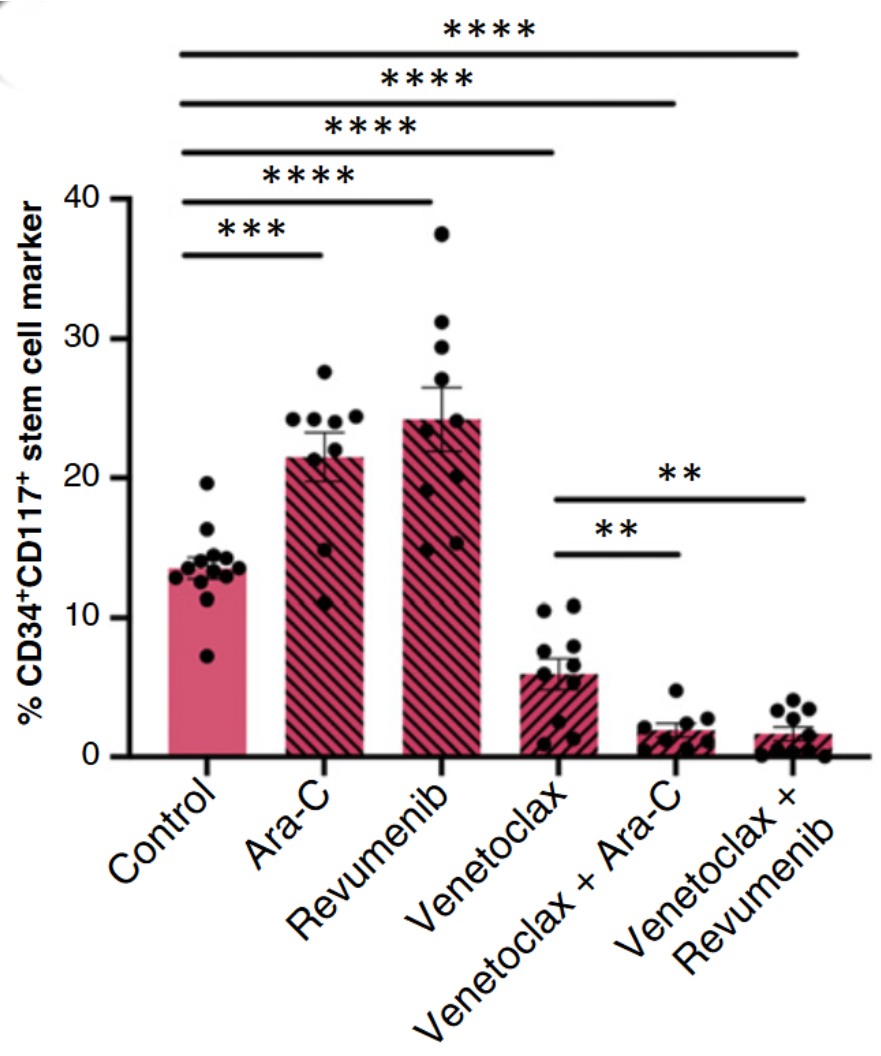
上图展示了在使用不同药物组合后,小鼠体内白血病干细胞(LSCs)的残留数量。可以看到单用化疗(Ara-C)或靶向药(Revumenib),柱子依然很高(代表癌细胞存活多);但一旦加入维奈克拉(Venetoclax)及其组合(最右侧的柱子),癌细胞数量几乎降到了零。虽然这只是小鼠的实验结果,但也显示了未来临床上应用的可能性。
起源决定预后:携带 “胎儿特征” 基因信号的患者,预后通常较差。这为医生进行风险分层提供了新依据。
PRDM16是潜在标志物:PRDM16高表达是这类高危白血病的重要特征。
治疗新策略:对于携带NUP98::NSD1和WT1突变的难治性儿童白血病,包含维奈克拉的联合疗法可能是一个极具潜力的治疗方案,能够克服传统化疗和Menin抑制剂的耐药性。
如果把白血病比作野草,传统的化疗像是在割草,虽然能暂时除掉地面的叶子,但除不掉深埋地下的“根”(静止期的白血病干细胞)。这项研究发现,这种特定类型的“根”非常特别,它们喜欢“吃脂肪”并由一个叫PRDM16的开关控制。好消息是,研究人员发现了一种除草剂(维奈克拉),它能专门针对这种根的弱点,配合其他药物,有望将这些顽固的根彻底拔除。
文章转自“儿童肿瘤前沿”公众号
声明:本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。