
既往原醛症被认为是一种“少见病”,但现有临床数据颠覆了这一认知。原醛症多见于中年人群,发病年龄多在40~64岁,是难治性
原醛症不仅会导致血压难以控制,更易诱发脑卒中、心力衰竭、肾脏损害及代谢紊乱等严重并发症,其远期危害极大却长期处于被低估状态。
原醛症的临床表现具有高度异质性和不典型性,增加了临床识别难度。
更具迷惑性的是,原醛症的肾上腺病变呈现多样化特征。除了影像学可见的腺瘤,还有散在细胞团样改变等不典型表现。在临床实践中,“影像学腺瘤+肾上腺静脉采血(AVS)分泌增高”的典型病例较易识别;而双侧等分泌型、“影像学正常但单侧分泌增高”等类型则极易被忽略。

《原发性醛固酮增多症诊断治疗的专家共识(2024版)》推荐对以下人群进行原醛症筛查:
①持续性高血压(>150/100 mmHg)者;使用3种常规降压药(包括利尿剂)无法控制血压(>140/90 mmHg)的患者;使用4种降压药才能控制血压(<140/90 mmHg)的患者及新诊断的高血压患者。
②高血压合并自发性或利尿剂所致的低钾血症患者。
③高血压合并肾上腺意外瘤的患者。
④早发性高血压家族史或早发(<40岁)脑血管意外家族史的高血压患者。
⑤原醛症患者中存在高血压的一级亲属。
⑥高血压合并阻塞性呼吸睡眠暂停的患者。
目前临床首选醛固酮/肾素比值(ARR)作为原醛症的筛查指标,该指标可有效发现血钾正常的隐匿性原醛症患者,显著提高检出率。
筛查前需做好充分准备:尽量将血钾纠正至正常范围,维持正常钠盐摄入;停用对ARR影响较大的药物至少4周,包括醛固酮受体拮抗剂、保钾及排钾利尿剂、甘草提炼物等;血管紧张素转换酶抑制剂(ACEI)、血管紧张素受体拮抗剂(ARB)、钙离子拮抗剂(CCB)等药物可能导致假阴性,需停用至少2周后再检测,若服药时
对于无法停用降压药物的患者,可遵循以下流程进行筛查,如应用ACEI/ARB±CCB时,ARR阳性需进一步确诊,阴性但接近临界值需调整药物后复查;应用β受体阻滞剂时,ARR阳性需停药调整后复查,阴性可排除原醛症。
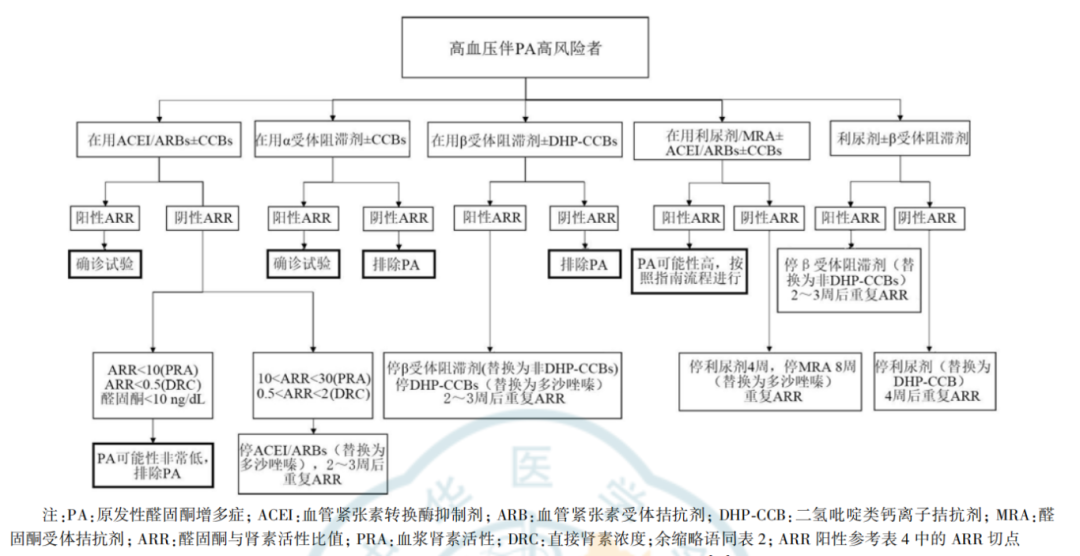
图1 服用降压药物患者接受原醛症筛查的建议流程
若ARR阳性,需进一步进行确诊试验(如
表1 原醛症确诊试验

值得一提的是,ARR结果易受多种因素影响,需警惕假阳性或假阴性。年龄>65岁者肾素下降更明显,可能导致ARR假阳性;女性经前期、排卵期及黄体期ARR可能升高,尤其检测DRC时需注意。低钠饮食可能导致假阴性,高钠饮食可能导致假阳性,筛查前需通过

手术治疗是单侧肾上腺腺瘤、单侧优势分泌型增生患者的首选方案,核心方式为病变肾上腺切除。但术后疗效不及预期,仍有较多患者术后血压偏高。尽管手术对生化指标的控制效果较好,但其术后并发症风险不容忽视,可能出现肾上腺皮质功能减退、肾上腺危象、肾功能减退等问题,极少数情况下还可能出现严重肾功能损伤。此外,部分患者术后会出现复发,多因术前未发现双侧微小病变,单侧切除后对侧病变组织开始异常分泌所致;对于双侧肾上腺病变患者,手术治疗效果更差,复发率相对更高。
药物治疗是原醛的基础干预手段,主要适用于双侧肾上腺增生、不适合手术或拒绝手术的患者等,核心药物为醛固酮受体拮抗剂(如
消融治疗是近年来兴起的一种微创治疗手段,可作为药物、手术治疗无效或不耐受患者的补充选择,核心原理是通过局部干预破坏异常分泌醛固酮的肾上腺组织,减少醛固酮分泌以实现血压控制和生化指标改善。
目前,在临床实践中,主要采用物理消融(如射频消融)和化学消融(如
在疗效方面,消融治疗对单侧肾上腺病变患者效果显著,可明显降低醛固酮水平,治疗初期降压效果优于药物治疗,长期随访中与药物治疗的血压控制效果趋于一致,整体血压与生化指标的完全控制率及部分改善率相对较高;对于双侧病变患者,双侧消融效果优于单侧,但长期疗效仍需更多多中心试验验证。此外,消融治疗对肾素抑制状态的解除效果优于药物治疗,能更有效降低远期心脑血管事件风险。
在安全性方面,消融治疗的副作用相对轻微,主要为胃肠道反应和局部疼痛,对症处理后可快速缓解;治疗后不会出现肾上腺皮质功能低下等严重并发症,肾功能减退风险也远低于手术治疗,整体安全性良好。目前,该治疗方式已获多国指南及专家共识推荐,成为原醛诊疗的重要补充。

尽管目前原醛症的治疗仍面临诸多挑战,但随着医学技术的不断发展和对原醛症认识的不断深入,新的治疗方法和药物有望不断涌现。例如,新型醛固酮受体拮抗剂和肾素-血管紧张素-醛固酮系统抑制剂的研究和应用,可能为原醛症的治疗带来新突破。消融治疗这一新兴微创手段的临床应用场景也将进一步拓展,为不适合手术或药物治疗效果不佳的患者提供全新治疗路径。
此外,原醛症作为内分泌源性疾病,其诊疗过程涉及内分泌科、心血管内科、泌尿外科、影像科等多个学科,多学科协作是提升诊疗质量的关键,通过多学科联合诊疗模式可充分整合各学科优势,为患者制定个体化诊疗方案,进而有效提高诊断率、优化治疗效果、改善长期预后。
参考文献:中华医学会内分泌学分会.原发性醛固酮增多症诊断治疗的专家共识(2024版).中华内分泌代谢杂志. 2025; 41(1):12-24.
