1. 核心诱因:衰老导致 CD8+T 细胞 NAD 水平显著下降
衰老个体的 CD8+T 细胞中,烟酰胺腺嘌呤二核苷酸(NAD)稳态严重失衡,这是 CAR-T 疗效差的根源。NAD 是维持线粒体健康、能量代谢及 T 细胞命运的关键代谢物 —— 作为氧化磷酸化辅酶保障能量供应,同时作为 SIRT 家族去乙酰化酶底物调控线粒体生物发生(如调控 PGC-1α)。
- 小鼠实验证实:衰老(>80 周)小鼠 CD8+T 细胞的 NAD 水平是年轻(8 周)小鼠的关键下调代谢物,液相色谱 - 串联质谱(LC-MS/MS)显示其在衰老细胞中丰度最低;
- 人类临床验证:对大 B 细胞淋巴瘤(LBCL)、黑色素瘤患者的外周血单个核细胞(PBMC)分析发现,衰老个体(>65 岁)CD8+T 细胞的 NAD 代谢异常,且无应答(NoR)患者的 NAD 相关通路活性显著低于应答(R)患者。
2. 关键机制:CD38 高表达与 PARP 激活导致 NAD “降解 - 消耗” 双重失衡
衰老 CD8+T 细胞的 NAD 下降并非单一因素所致,而是 “降解增加 + 消耗加剧” 的双重结果。
- CD38 高表达:NAD 及前体的 “降解器”CD38 是多功能酶,可直接降解 NAD 生成 cyclic ADP-ribose,还能降解 NMN、NR 等 NAD 前体,导致外源性补充前体无效。衰老 CD8+T 细胞(静息 / 激活态)的 CD38 表达显著高于年轻细胞,且所有 T 细胞亚群( naive Tn、中心记忆 Tcm、效应记忆 Tem)均存在该现象;仅 CD38 高表达(CD38hi)的衰老 CD8+T 细胞会出现线粒体活性降低,年轻细胞过表达 CD38 后还会重现衰老 CAR-T 的 “Tcm 比例减少、mtDNA 含量降低” 表型。
- PARP 激活:NAD 的 “消耗器”衰老 CD8+T 细胞存在 DNA 损伤积累(γH2AX 磷酸化水平升高),激活聚 ADP 核糖聚合酶(PARP)——PARP 是细胞内主要的 NAD 消耗酶,其激活进一步加剧 NAD 耗竭,与 CD38 形成 “双重打击”,导致 NAD 稳态难以逆转。
3. 功能后果:线粒体障碍与干细胞样特性丧失,致 CAR-T “无效且不持久”
NAD 下降直接引发下游连锁反应,最终导致 CAR-T 细胞功能失效:
- 线粒体功能全面障碍衰老 CD8+T 细胞的线粒体膜电位(TMRM 染色)、线粒体质量(MitoTracker Green 染色)显著降低,氧化磷酸化能力(耗氧率 OCR)下降,线粒体嵴数量减少(电镜证实),同时活性氧(ROS)积累 —— 这些缺陷导致 CAR-T 细胞能量供应不足,无法维持长期功能;
- 干细胞样特性彻底丧失CAR-T 疗效依赖 “干细胞样记忆 T 细胞(Tcm,CD44+CD62L+)” 的长期维持,而衰老 CAR-T 细胞在 IL-7/IL-15(诱导记忆表型的细胞因子)条件下,Tcm 比例仅 4.03%(年轻细胞为 95.7%),干细胞样标志物 TCF1 表达显著降低;体内实验中,衰老 CAR-T 细胞 30 天后在脾脏几乎检测不到,完全无法控制肿瘤生长(B16-HER2 模型中,仅年轻 CAR-T 可抑制肿瘤)。
破解策略
1. 核心方案:CD38 抑制剂(78c)+NAD 前体(NMN),双管齐下恢复 NAD
针对 “CD38 降解 NAD” 的核心机制,采用 “CD38 抑制剂阻断降解 + NAD 前体补充合成” 的联合策略,可有效逆转衰老 CAR-T 的功能缺陷:
- 作用机制CD38 特异性抑制剂 78c(200nM)可阻断 CD38 的 NAD 酶活性,解除其对 NAD 及前体的降解,使 NAD 前体 NMN(1mM)能有效转化为 NAD,恢复 NAD/NADH 比值至年轻水平;
- 干预效果
- 线粒体修复:衰老 CAR-T 细胞的线粒体备用呼吸能力(SRC)、线粒体质量显著提升,氧化磷酸化功能恢复;
- 表型改善:Tcm 细胞中 CD62L 表达升高,干细胞样特性增强;
- 体内疗效:在 B16-HER2(HER2 靶向 CAR)、EL4-mCD19(CD19 靶向 CAR)两种小鼠肿瘤模型中,联合处理的衰老 CAR-T 细胞控瘤能力与年轻细胞相当,30 天后脾脏中 CD45.1+CAR-T 细胞数量显著增加(P=0.0343);
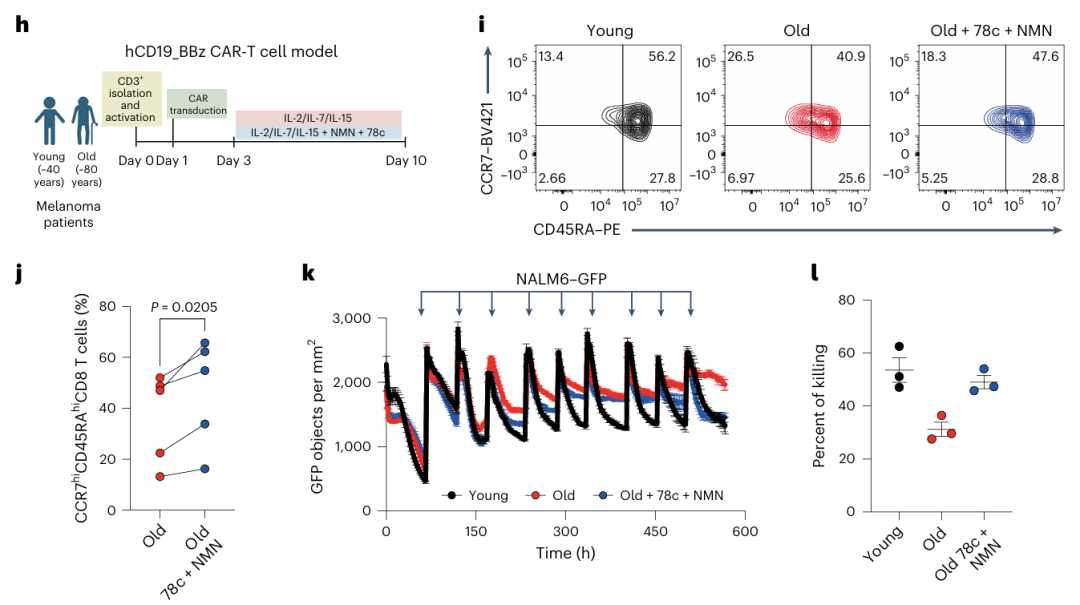
- 人类验证:对 > 65 岁健康人或黑色素瘤患者(76-84 岁)来源的 CD19 CAR-T 细胞,该方案可恢复线粒体 SRC(P=0.0177)、提升 CCR7hiCD45RAhi(干细胞样标志物)细胞比例(P=0.0205),且多次肿瘤再挑战后仍能维持杀伤能力。
2. 替代方案:PARP 抑制剂,针对性解决 NAD “消耗过量”
针对 “PARP 激活消耗 NAD” 的机制,使用 PARP 抑制剂(如奥拉帕尼,5μM)可减少 NAD 消耗,同样实现 NAD 水平与线粒体功能的恢复 —— 该方案在衰老 CD8+T 细胞中验证有效,为无法耐受 CD38 抑制剂的患者提供了备选策略。
3. 临床转化价值:从 “机制” 到 “临床应用” 的闭环验证
人类临床样本进一步证实该策略的可行性:
- 疗效预测:CD38 表达水平、NAD 代谢可作为 CAR-T 疗效的预测指标 ——LBCL 患者中,CD38 高表达的 NoR 患者占比更高;B-ALL 患者中,基线 CD38 高表达与 CAR-T 持久性差显著相关;
- 适用人群:覆盖临床 75% 的 > 65 岁癌症患者,填补老年患者 CAR-T 疗效差的空白,为个性化 CAR-T 制备提供 “代谢优化” 方案。
综上,衰老个体 CAR-T 疗效差的核心是NAD 下降驱动的代谢 - 功能连锁障碍,而 “靶向 CD38/PARP + 补充 NAD 前体” 的联合策略可从机制上破解该问题,为老年患者 CAR-T 治疗提供了明确的转化方向。
参考资料
Helen Carrasco Hope et al,Age-associated nicotinamide adenine dinucleotide decline drives CAR-T cell failure, Nature Cancer 2025, https://doi.org/10.1038/s43018-025-00982-7
Katsyuba, E., Romani, M., Hofer, D. & Auwerx, J. NAD+ homeostasis in health and disease. Nat Metab. 2, 9–31 (2020).
Covarrubias, A. J., Perrone, R., Grozio, A. & Verdin, E. NAD+ metabolism and its roles in cellular processes during ageing. Nat. Rev. Mol. Cell Biol. 22, 119–141 (2021).
Mann et al. NAD + metabolism and function in innate and adaptive immune cellsJournal of Inflammation (2025) 22:30 https://doi.org/10.1186/s12950-025-00457-7