来源:IBD Daily
研究团队使用成分明确的饮食 (CDD)、CDD+
给三组小鼠分别饲喂CDD、CDD+纤维素 (不可发酵纤维)、CDD+菊粉的饲料,小鼠的体重、肠道形态、炎症状态、结肠中固有免疫细胞的数量和炎症相关基因均无明显差异,但当使用DSS处理后CDD+菊粉组的小鼠对DSS诱导的结肠炎表现出更高的敏感性,体重和体脂、结肠长度和重量显著下降,结肠炎病理评分显著增加。(图1)
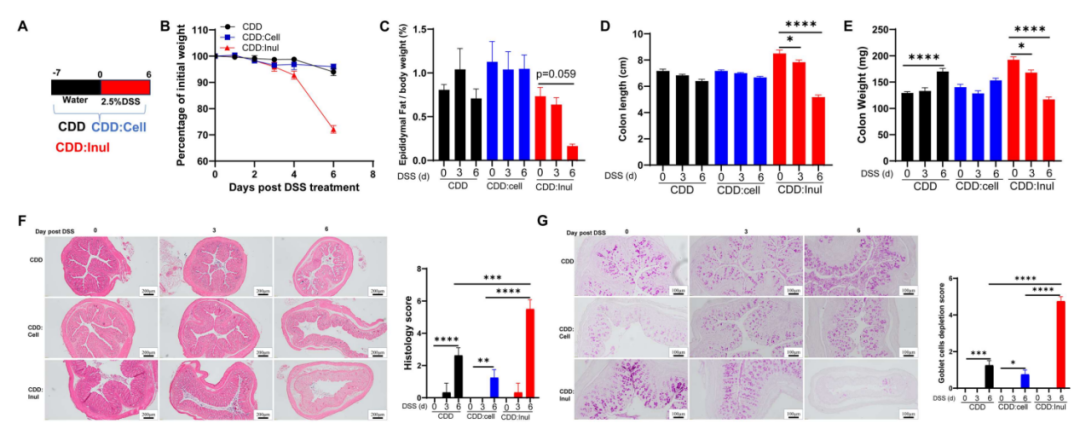
图1 菊粉不引发结肠炎,但加重DSS诱导的结肠炎
CDD:Cell CDD+纤维素;CDD:Inul CDD+菊粉
研究团队给两组小鼠饲喂谷物饲料 (GBC) 并用DSS处理5天,两组表现出类似的体重下降趋势,然后一组饲喂CDD,一组饲喂CDD+菊粉,饲料转换后CDD组小鼠体重开始恢复,但CDD+菊粉组小鼠体重持续下降,且实验结束时菊粉组的小鼠脂肪占比更低、结肠重量/长度比值升高、结肠内杯状细胞数减少、促炎细胞因子表达增加,这些结果表明菊粉会通过维持或加剧肠道炎症抑制小鼠结肠炎的恢复。(图2)
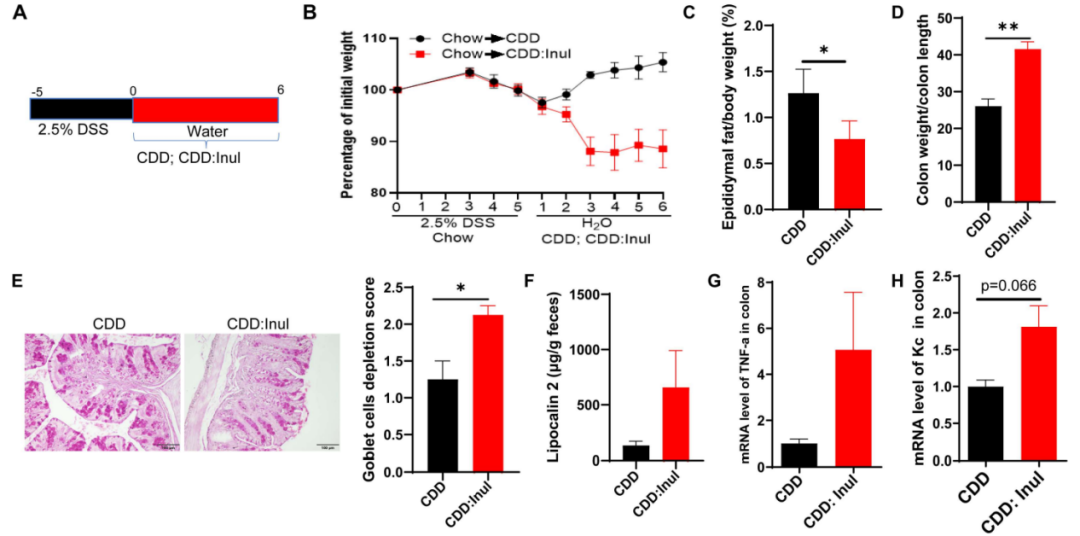
图2 菊粉抑制DSS诱导的结肠炎的恢复
研究团队对DSS处理6天后小鼠血液中的免疫细胞进行计数,结果显示与CDD和CDD+纤维素相比,CDD+菊粉组的小鼠总白细胞计数更高,其中中性粒细胞和单核细胞的百分比和绝对数量均显著升高,流式细胞术分析表明CDD+菊粉组小鼠结肠中的中性粒细胞和巨噬细胞浸润均增加,且伴随促炎细胞因子表达上调。使用抗Gr1抗体来选择性地清除中性粒细胞和炎症性单核细胞 (可被募集到结肠并可分化为巨噬细胞) 可显著减轻了菊粉引起的DSS诱导的结肠炎的加重,这表明中性粒细胞和炎症性单核细胞及其衍生的巨噬细胞会导致补充菊粉后炎症反应和结肠炎加剧。(图3)
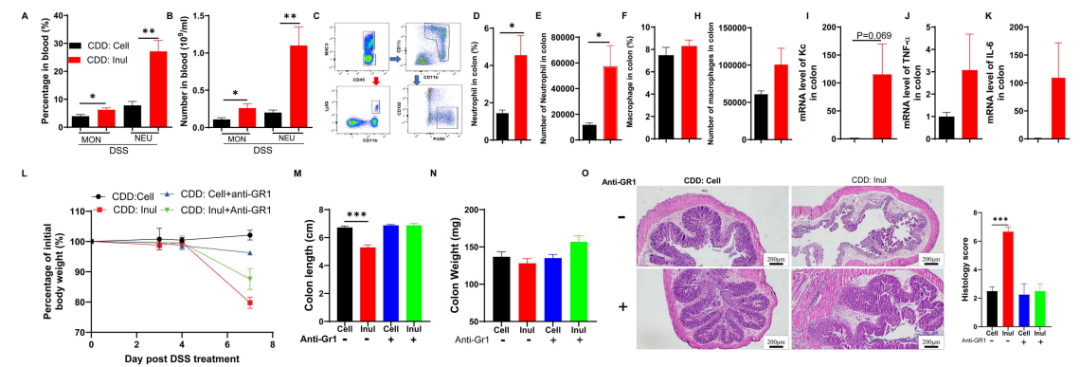
图3 菊粉增强Gr1细胞介导的炎症反应加剧DSS诱导的结肠炎
研究团队对各组小鼠的肠道菌群进行16S rRNA基因测序,发现菊粉显著改变了肠道菌群的整体组成,与CDD和CDD+纤维素相比,CDD+菊粉组的小鼠的肠道菌群在DSS处理前后均表现出微生物多样性显著降低且失衡程度增加 (Shannon 指数) 。在门水平上,饲喂菊粉的小鼠肠道菌群中放线菌门 (Actinomycetota) 和芽孢杆菌门 I (Bacillota_I) 的丰度增加,而疣微菌门 (Verrucomicrobiota) 、芽孢杆菌门 A (Bacillota_A) 和芽孢杆菌门 B (Bacillota_B) 的丰度则降低;在属水平上,饲喂菊粉的小鼠虽然有益菌群如
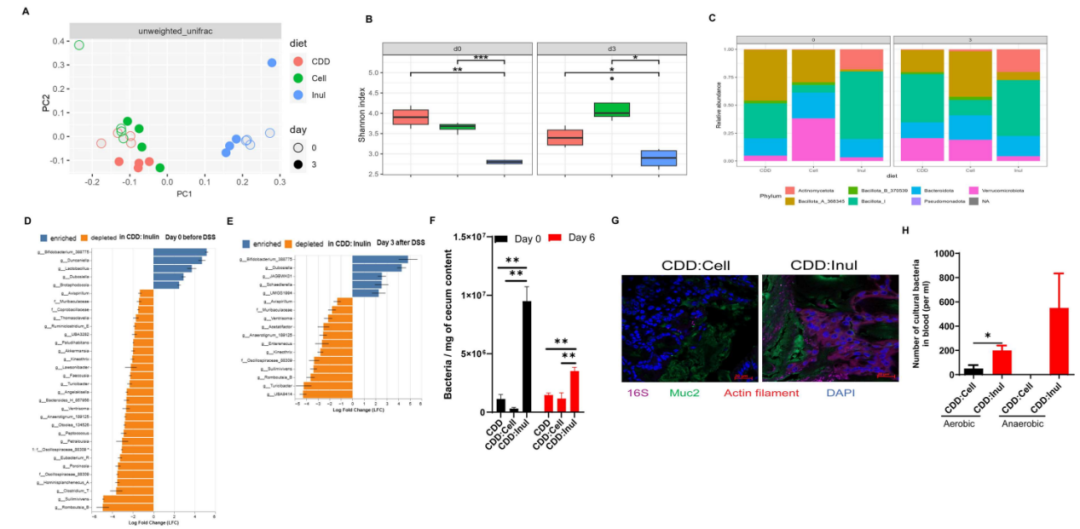
图4 菊粉对DSS诱导的结肠炎期间肠道菌群的影响
为了确定菊粉诱导的肠道菌群变化是否会导致DSS诱导的结肠炎加重,研究团队给CDD组和CDD+菊粉组的小鼠喂食广谱抗生素混合物以清除肠道菌群,然后使用DSS诱导抗小鼠产生结肠炎。结果显示抗生素治疗逆转了CDD组和CDD+菊粉组的小鼠之间结肠炎严重程度的差异,原本两组间存在差异显著的体重、脂肪、结肠长度、结肠重量、炎症因子等在经抗生素治疗后均不显著。这些结果表明菊粉促进结肠炎的作用依赖于肠道菌群的存在。
短链脂肪酸 (SCFAs) 是菊粉在肠道菌群发酵过程中产生的关键代谢产物之一,为了检验菊粉加重DSS诱导的结肠炎是否依赖于发酵产生的SCFA,研究团队使用能够显著抑制菊粉的发酵并降低SCFA的生成β-酸进行处理,结果显示β-酸对SCFA产生的抑制作用并不能影响DSS诱导CDD+菊粉组小鼠结肠炎的加重,表明菊粉的促结肠炎作用并非由其微生物发酵过程中产生的SCFA介导。(图5)
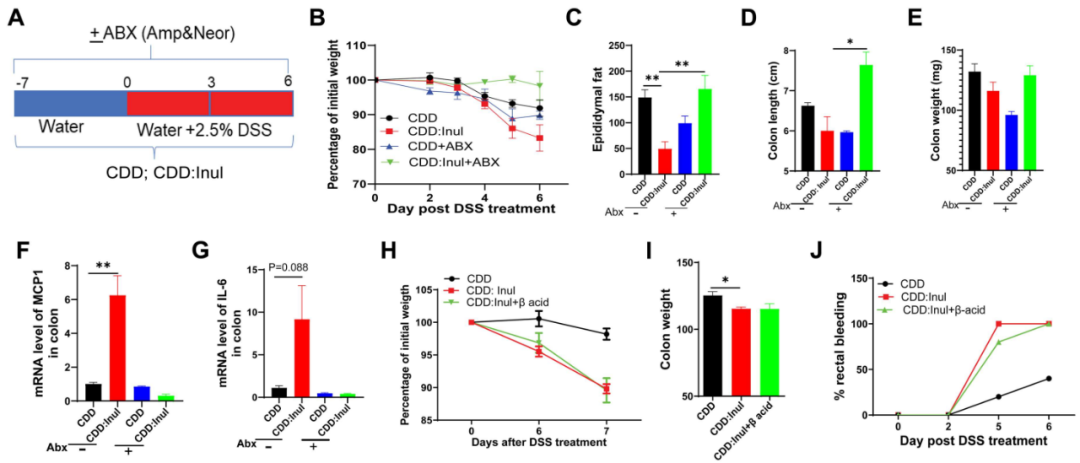
图5 菊粉引起的DSS诱导结肠炎加重依赖于肠道菌群
菊粉在增加肠道内的细菌负荷后,随着细菌总数的增加细菌的鞭毛蛋白显著升高,粪便中抗鞭毛蛋白 IgA的水平也显著升高。研究团队推测鞭毛蛋白可能会激活固有免疫信号通路,从而加剧DSS诱导的结肠炎。因此团队使用缺乏包括NLRC4和TLR5在内鞭毛蛋白受体的N4T5基因敲除小鼠进行实验,结果显示CDD+菊粉组的N4T5基因敲除小鼠结肠炎程度仍高于CDD+纤维素组,但其结肠炎严重程度的差距低于野生型小鼠中CDD+菊粉组和CDD+纤维素组中的差距,表明菊粉引起的细菌成分鞭毛蛋白增加可能在DSS诱导的结肠炎加重中发挥一部分作用。
MyD88在小鼠固有免疫中发挥关键作用,为了进一步研究固有免疫信号在菊粉加重结肠炎中的作用,研究团队使用MyD88敲除小鼠重新进行实验,结果表明无论在饲喂纤维素或菊粉,MyD88敲除小鼠在DSS处理后表现出相似的疾病严重程度,体重下降、结肠长度、结肠重量和组织病理学无显著差异。这些结果表明,菊粉加重结肠炎的效应依赖于MyD88介导的先天免疫信号通路。(图6)
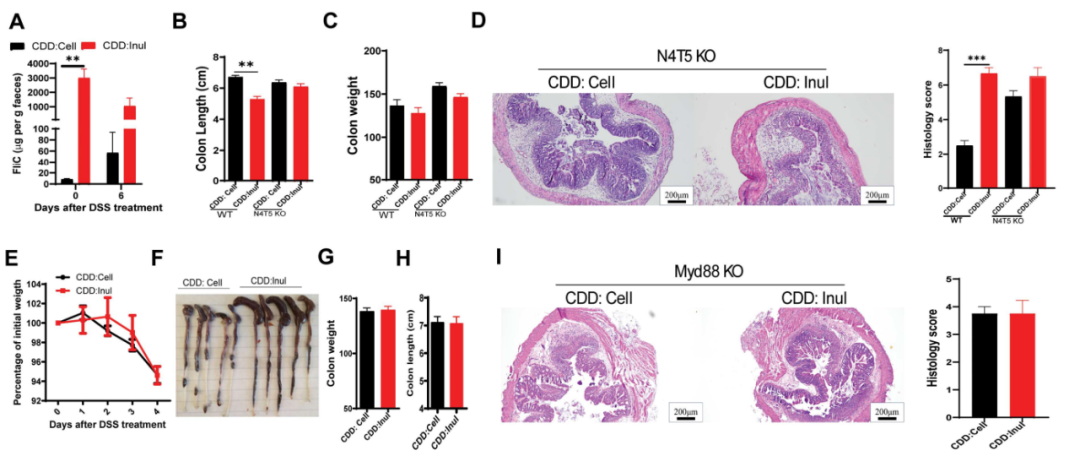
图6 MyD88信号通路驱动菊粉引起的DSS诱导结肠炎加重
MyD88调控多种下游通路并最终导致细胞因子产生,在众多细胞因子中IL-18被认为在结肠炎发病中起到关键作用。因此该团队下一步探究菊粉补充剂是否通过 IL-18 加剧DSS诱导的结肠炎。首先研究团队发现菊粉显著上调了肠道菌群正常的普通小鼠血清中IL-18的表达,而无菌小鼠中IL-18的表达不变,这表明菊粉诱导的IL-18表达增加依赖于肠道菌群的存在。此外菊粉诱导了野生型小鼠结肠中IL-18水平的升高,而在MyD88基因敲除鼠结肠中IL-18水平不会受菊粉的影响。研究团队使用IL-18基因敲除鼠进一步明确IL-18的功能作用,结果显示在IL-18基因敲除鼠中无论CDD+纤维素组还是CDD+菊粉组DSS诱导的结肠炎严重程度不变,这些发现表明IL-18在菊粉加重DSS诱导的结肠炎中发挥关键作用。(图7)
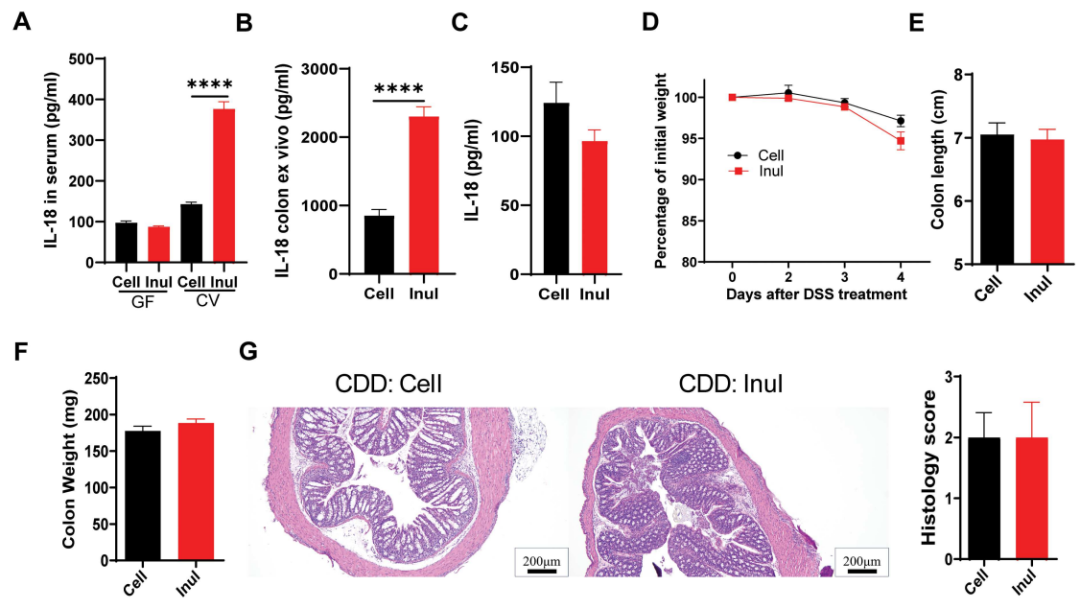
图7 IL-18是介导菊粉加重DSS诱导结肠炎的关键分子
研究团队先前的研究表明母体饮食不仅会影响母鼠自身的肠道微生物组,还会改变其后代的肠道菌群组成。基于这项研究的16S rRNA测序数据,团队发现与来自CDD组的母鼠成年后代相比,来自CDD+菊粉组的母鼠成年后代的微生物多样性显著降低,其菌群变化模式与在成年小鼠直接摄入菊粉时所观察到的变化相一致。
为了进一步证明这一点,研究团队在母鼠出生后不久就开始分别喂食CDD或CDD+菊粉,这些母鼠的子代在3周龄断奶,随后饲喂以谷物为主的饲料至6周龄,然后使用DSS诱导结肠炎,结果表明与CDD组相比,CDD+菊粉组母鼠的子代对DSS 诱导的结肠炎易感性更显著。这些结果表明,哺乳期母鼠摄入菊粉会降低后代肠道菌群多样性,并增加促结肠炎细菌的丰度,从而增加其成年后对 DSS 诱导的结肠炎的易感性。(图8)
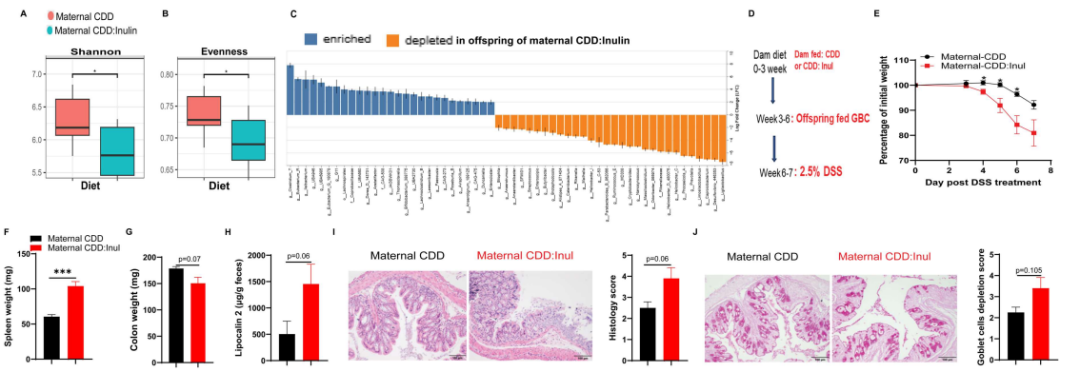
图8 母亲摄入菊粉会降低子代肠道菌群多样性,并增加其对DSS诱导结肠炎的易感性
这项研究表明菊粉摄入通过肠道菌群介导的炎症和MyD88/IL-18信号通路加剧DSS诱导的结肠炎,且这种影响会持续存在于子代中。这些结果强调了在疾病特异性饮食干预中考虑膳食纤维类型的重要性。
致谢
中南大学湘雅三医院 付云东
中南大学湘雅三医院 王思丹
中南大学湘雅三医院
中南大学湘雅三医院
对本篇文章解读做出的贡献
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)