
首都医科大学附属北京安贞医院
ACS是全球范围内导致死亡和残疾的主要原因。OSA在ACS患者中具有极高的患病率,且与不良预后密切相关。与此同时,营养不良作为一种可改变的危险因素,近年来在
既往研究表明,OSA导致的慢性间歇性缺氧和全身性炎症可能引起代谢紊乱和蛋白质消耗,进而可导致营养状态恶化;而营养不良引起的肌肉萎缩(特别是呼吸肌无力)、体液重分布等又可能加重OSA,两者形成恶性循环。然而,在ACS这一特定临床人群中,OSA是否会影响营养不良与心血管预后的关系,目前尚缺乏临床证据支持。
本研究为“OSA-ACS项目”的一项子分析,属于前瞻性、观察性、单中心队列研究。
研究对象:连续纳入了2015年6月至2020年1月期间在北京安贞医院住院的1756名ACS患者。
分组标准:所有患者入院后均进行了便携式睡眠监测。根据呼吸暂停低通气指数(AHI),患者被分为OSA组(AHI ≥15次/小时,931例)和非OSA组(825例)。
评估工具:采用三种客观营养评分工具对患者进行基线评估:控制营养状态评分(CONUT)、营养风险指数(NRI)和那不勒斯预后评分(NPS)。
终点事件:研究的主要终点为主要心血管和脑血管不良事件(MACCE),包括心源性死亡、
1.营养不良普遍存在且具有隐蔽性
研究发现,ACS患者中营养不良的检出率因评估工具而异(CONUT:47.4%,NRI:23.0%,NPS:87.8%)。值得注意的是,在BMI ≥25.0 kg/m²(超重及肥胖)的患者群体中,仍有相当比例存在营养不良(如CONUT评分检出率为44.7%),提示高BMI一定程度上掩盖了潜在的营养受损状态。
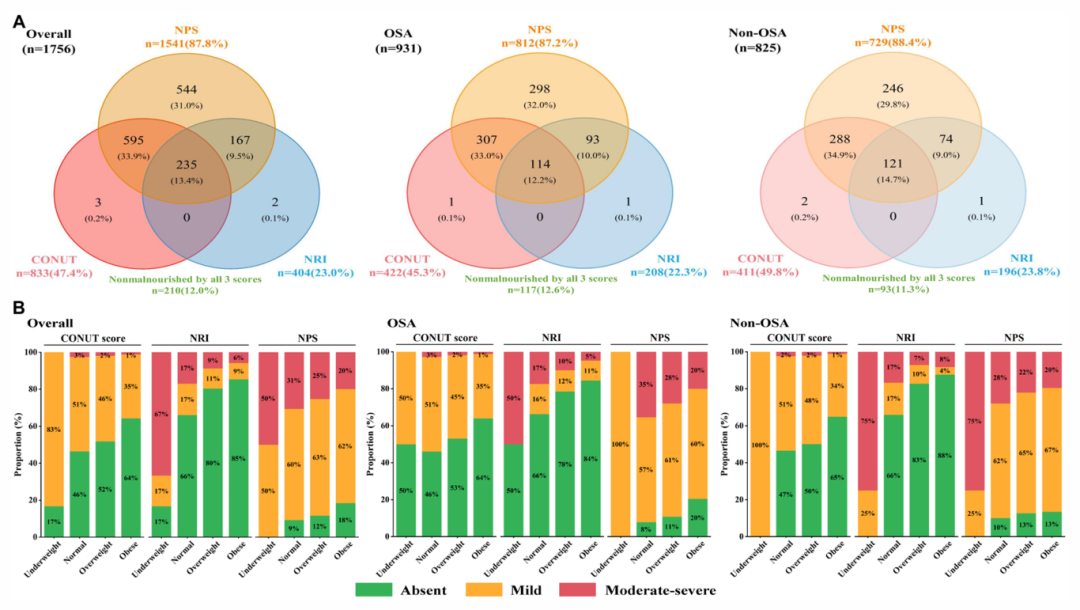
2. 预后关联存在显著的人群特异性
多因素Cox回归分析显示,营养不良对预后的影响在是否合并OSA的患者中存在显著差异:
•在OSA组中:营养不良是MACCE的独立预测因子。中重度营养不良患者发生不良事件的风险显著增加(CONUT评分调整后风险比[aHR]为2.707;NRI为1.647;NPS为1.962)。且随着营养不良程度加重,风险呈线性趋势。
•在非OSA组中:除CONUT评分提示的轻度营养不良外,未观察到营养不良与MACCE之间存在显著的独立关联。
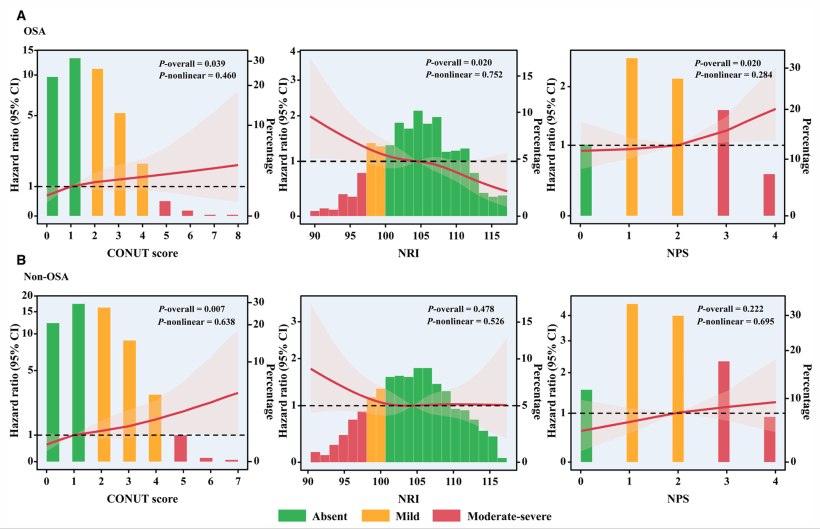
3.评估工具效能比较
在三种工具中,CONUT评分在预测MACCE方面表现出更佳的准确性(AUC值最高)和区分度(C统计量最高)。
本研究得出的核心结论是:营养不良与OSA在ACS患者中存在显著的交互作用,二者共存一定程度上放大了心血管复发风险。
•识别高危亚组:临床医生应意识到,“ACS合并OSA且伴有营养不良”的患者属于极高危人群。OSA引发的炎症风暴与营养不良导致的代谢储备下降可能产生协同打击,导致预后恶化。
•纠正BMI评估的局限性:临床不能仅凭体型判断营养状态。研究探讨了“肥胖悖论”背后的营养异质性,即肥胖患者可能因肌少症或炎症消耗而处于“隐性营养不良”状态,这在OSA患者中并不少见。
•优化筛查流程:鉴于CONUT评分计算简便(仅需白蛋白、总胆固醇、淋巴细胞计数)且预测效能较高,建议将其纳入ACS合并OSA患者的常规入院评估体系,以实现早期风险分层。
本研究为临床提供了重要证据,同时指出了未来的研究方向:
•因果关系验证:本研究为观察性研究,未来需要进一步的基础研究来阐明OSA导致营养不良的具体病理生理机制(如缺氧对肠道吸收或蛋白质代谢的具体影响)。
•动态评估:本研究仅进行了基线评估。考虑到ACS后患者的饮食和代谢可能发生变化,未来研究应关注出院后营养状态的动态变化对预后的影响。
•干预研究:最重要的是,需要开展干预性临床试验,以明确针对这一高危人群(OSA+营养不良)进行营养支持治疗(如抗炎饮食、蛋白质补充)是否能切实改善其长期心血管预后。
北京安贞医院冠心病中心为国内首批专注于冠心病系统化诊疗的专科中心,是国家心血管病临床医学研究中心核心单元、国家卫健委冠心病介入诊疗培训基地及中国胸痛中心示范单位。年冠脉介入手术量近4万例,关注冠心病的临床与基础研究,致力于推动冠心病的规范化培训与诊疗。

刘逸翔 医生
公威 教授
聂绍平 教授
