哮喘是一种以呼吸道症状、炎症和气道高反应性为特征的慢性呼吸系统疾病,影响全球约4亿人。其标志性事件——急性加重(或称“急性发作”),是构成该疾病负担的主要因素。
哮喘急性发作不仅难以预测,还会形成“发作-风险增加-再发作”的恶性循环,导致肺功能持续下降与生活质量恶化。当前,口服皮质类固醇(OCS)是治疗急性发作的核心药物,但其使用会带来
近期发表在CHEST期刊上的一篇综述,深入探讨了哮喘急性发作在定义、分型、诱因及内在生物学机制上的异质性,并评述现有管理策略的局限性与精准医疗等新兴疗法的发展。
哮喘急性发作在临床上被定义为呼吸系统症状进行性加重,通常伴随肺功能下降,并需要调整治疗的急性事件。根据GINA指南,当患者峰值
➤严重程度分类模糊:“中度”与“严重”发作的指标(如肺功能下降、症状、药物使用)存在显著重叠,表明急性发作严重程度是一个连续谱,而非界限分明的类别;
➤依赖主观报告:定义在很大程度上依赖患者主观报告的症状,其准确性和感知的个体差异可能导致判断不一致;
➤忽略炎症维度:传统定义缺乏对血嗜酸性粒细胞(BEC)、呼出气
哮喘急性发作的临床表现具有高度异质性,反映了触发因素、炎症机制与患者个体因素之间复杂的相互作用。根据起病速度与临床特征,可主要划分为两种表型,见表1。
表1. 哮喘发作的两大临床表型
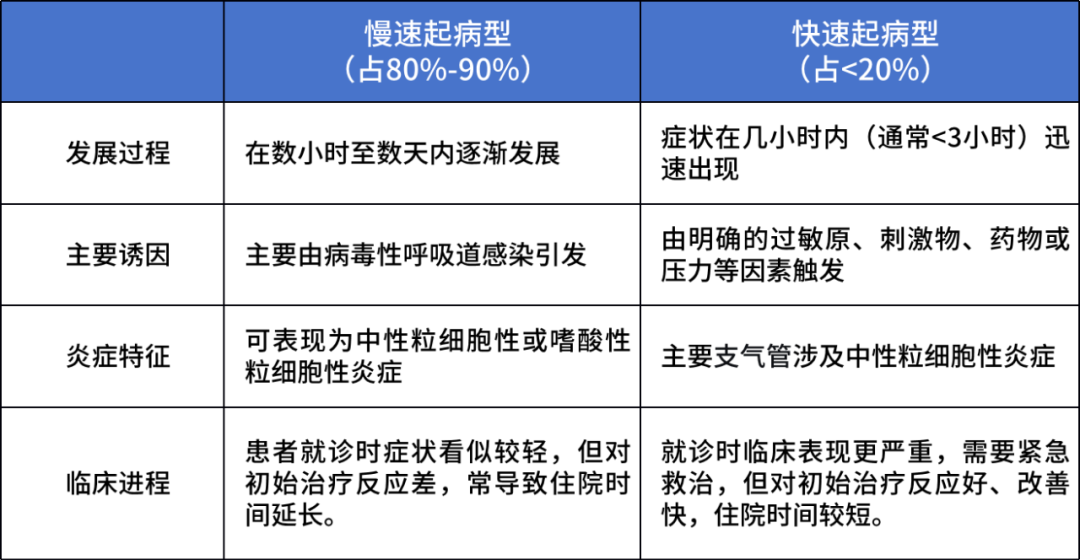
这种基于临床表现的表型分类,虽然描述了不同的疾病轨迹,但未能揭示其背后的病理生物学机制,因此无法实现针对性的精准治疗。未来的管理策略需要结合生物标志物,以深入理解生物学驱动因素,从而制定真正的个体化治疗方案。
哮喘急性发作的病理生理机制具有显著异质性,由不同的触发因素驱动,并对应着不同的炎症类型。这种机制上的差异,是临床表现相似的背后根源。
1. 主要触发因素与机制
哮喘急性发作由多种因素触发,每种因素关联着独特的炎症通路,详见表2。
表2.哮喘发作的主要触发因素与机制
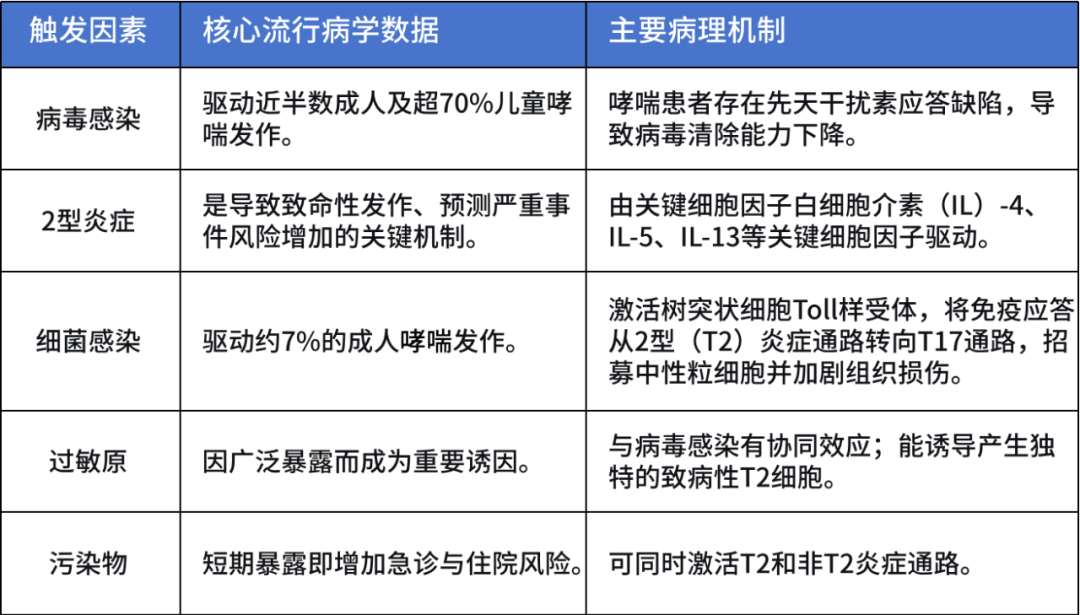
2. 炎症内型的实证研究
哮喘急性发作的本质具有显著的炎症异质性,这一特征在未使用生物制剂与已使用生物制剂的患者中呈现出不同特点。
➤未使用生物制剂的患者:研究表明其急性发作可分为T2-高、T2-中和T2-低等炎症表型。值得注意的是,这些表型与临床症状、肺功能损害程度等常规指标并无关联,且患者稳定期的炎症表型与急性发作期表型无显著相关性。这揭示了临床症状与生物学机制之间的脱节,凸显了在急性发作期通过生物标志物识别内在驱动机制的重要性。
➤接受生物制剂治疗的患者:研究表明近半数急性发作仍表现为嗜酸性粒细胞性炎症(伴有FeNO和BEC升高);而另外近半数急性发作则表现为非嗜酸性粒细胞性特征(伴有的C反应蛋白浓度升高、痰中性粒细胞比例增加以及更频繁的抗生素使用)。此外,上皮应激、先天免疫反应和黏液分泌也是驱动急性发作的重要机制。FeNO在识别不同驱动类型中具有重要价值。
总之,无论患者是否使用生物制剂,其哮喘发作的炎症驱动都存在明显异质性,且无法通过临床表现准确判断。这强调了在急性发作期进行生物标志物检测的核心价值,是实现精准治疗的关键所在。
1. 当前策略(图1)
➤传统药物治疗模式面临挑战
哮喘急性发作管理很大程度上依赖于OCS,虽能降低入院风险,但长期使用可能增加全因死亡率;22%-44%的患者在接受OCS同时接受不必要的抗生素治疗,研究证实抗生素使用对改善症状、肺功能或住院率方面无显著获益。
➤治疗理念革新:抗炎缓解治疗(AIR)
短效β2受体激动剂(SABA)虽能快速缓解症状,但无法控制潜在的气道炎症,且过度使用可能增加发作的严重程度和频率。
研究发现急性发作前两周存在"干预窗口期",此时气道炎症加剧但肺功能尚未明显下降。GINA指南推荐采用AIR疗法,即按需使用低剂量吸入性
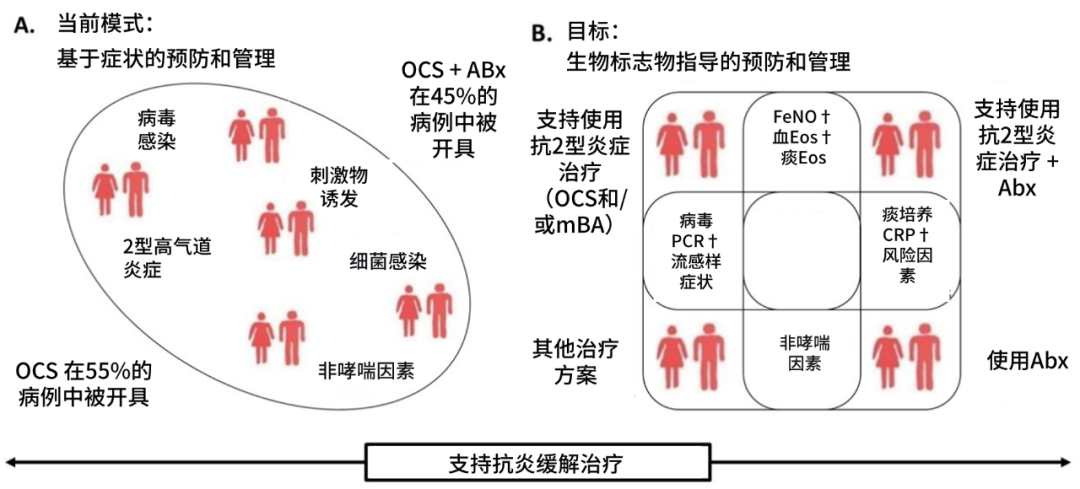
图1. 哮喘急性发作的两种不同管理方法。A:在当前基于症状的哮喘管理模式下,我们对所有急性发作均采取相同或随机的预防和治疗措施,至少会使用口服糖皮质激素(OCS),并且常常联用抗生素(Abx)。B:目标是利用可及的生物标志物——其中许多可作为床旁检测(†)——所提供的客观生物学证据,更好地为我们的预防和治疗决策提供信息。这可能有助于更精准或创新地应用针对2型炎症的抗炎治疗,包括OCS和/或单克隆抗体(mAb)。所有急性发作都应从AIR中获益。
缩写:CRP=C反应蛋白,Eos=嗜酸性粒细胞,FeNO=呼出气一氧化氮分数,PCR=聚合酶链式反应。
2. 新兴策略(图2)
➤生物标志物指导的分层治疗
研究表明,通过BEC计数和FeNO水平可更好地了解患者急性发作治疗反应中的异质性。数据显示,T2-高表型患者(BEC≥300 cells/μL且FeNO≥35ppb)接受OCS后肺功能改善显著(FEV₁提升0.39L),而T2-低表型患者改善有限。有研究进一步证实,FeNO≥25ppb的患者对治疗的反应更佳。同时,分子检测技术有助于识别病毒感染,为合理使用抗生素提供依据,有效避免过度治疗。
➤生物制剂在急性发作期的突破性应用
临床试验证实,针对嗜酸性粒细胞性发作(BEC≥300 cells/μL),使用贝那利珠单抗可显著延长治疗有效时间,改善症状评分,成为半个世纪来首个急性发作新疗法。虽然该方法在重症患者中的应用仍需更多证据,但为摆脱传统“一刀切”策略奠定了基础。
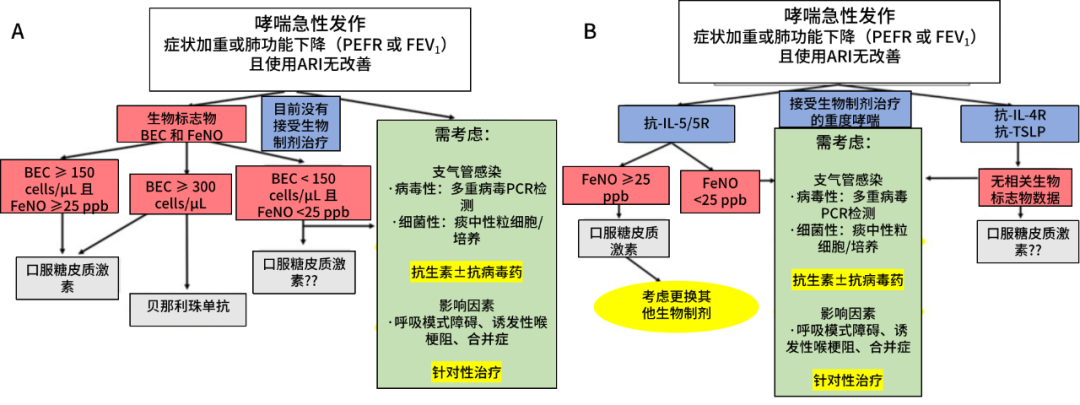
图2. 哮喘急性发作的生物标志物指导管理方法。哮喘急性发作是指症状增加或肺功能下降,且在使用抗炎缓解药物后仍无改善。本图根据近期证据,提出了一种基于血嗜酸性粒细胞计数和呼出气一氧化氮分数来管理哮喘急性发作的临床算法建议。A:展示了未接受生物制剂治疗患者的分层策略。B:概述了已接受生物制剂治疗的重度哮喘患者的处理方法。
缩写:AIR=抗炎缓解治疗;BEC=血嗜酸性粒细胞计数;BPD=呼吸模式障碍;FEV1=第一秒用力呼气容积;FeNO=呼出气一氧化氮分数;ILO=诱发性喉梗阻;PEF=峰呼气流量;OCS=口服糖皮质激素;PCR=聚合酶链式反应
哮喘急性发作不仅严重影响患者生活质量、占用大量医疗资源,更是导致死亡事件发生的关键因素。作为重要的哨兵事件,急性发作既是病情恶化的警示,也为调整和优化个体化治疗方案提供了宝贵契机。尽管研究表明驱动哮喘急性发作的机制具有高度异质性,但70年来临床治疗仍停留在OCS和抗生素的"一刀切"模式。
基于现有研究证据,未来发展方向应聚焦于推动精准医疗策略在急性发作管理中的应用:通过免疫学和临床研究的进步,完善哮喘急性发作的定义标准;加强生物标志物在识别发作机制中的作用;开发个体化治疗策略。这种基于精准医学的新型诊疗模式亟待进一步研究验证,以实现从传统标准化治疗向个体化管理的根本转变。
参考文献:Celis-Preciado CA, Hamou Kuijpers EB, Ramakrishnan S, et al. Applying precision medicine to the heterogeneity of asthma attacks. Chest. Published online November 13, 2025. doi:10.1016/j.chest.2025.11.013
声明:本文内容基于学术文献综述,旨在科普最新医学进展,不能替代专业医疗建议。具体诊疗方案请遵从您的主治医生指导。
