编者按
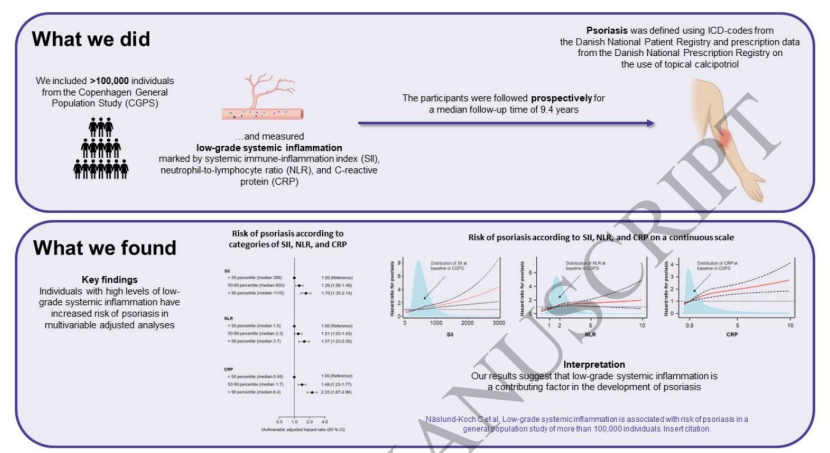
图1 研究的设计逻辑与核心结论


本研究数据来源于哥本哈根一般人群研究(CGPS),这是一项前瞻性队列研究,于2003-2015年间纳入了105,418名20-100岁的丹麦居民,中位年龄58岁,其中55%为女性。研究通过以下方法开展分析:
中位随访9.4年(四分位数范围6.7-11.9年),采用Cox比例风险回归模型计算hazard ratios(HR),评估炎症标志物与银屑病发病风险的关联,并调整潜在混杂因素。


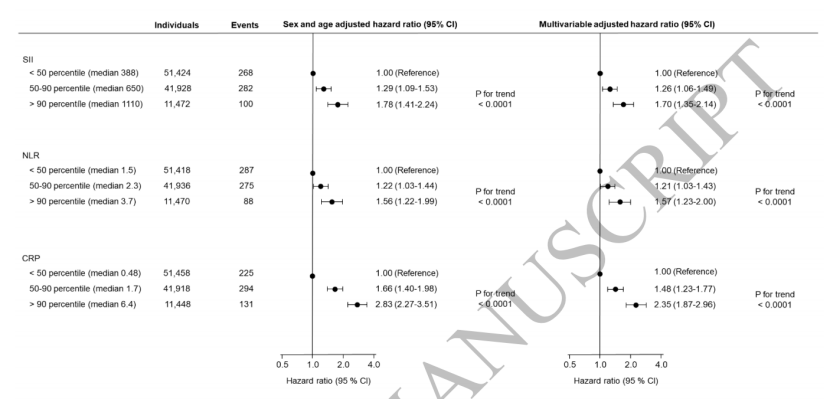
图2 不同分档的SII、NLR、CRP与银屑病发病风险关联
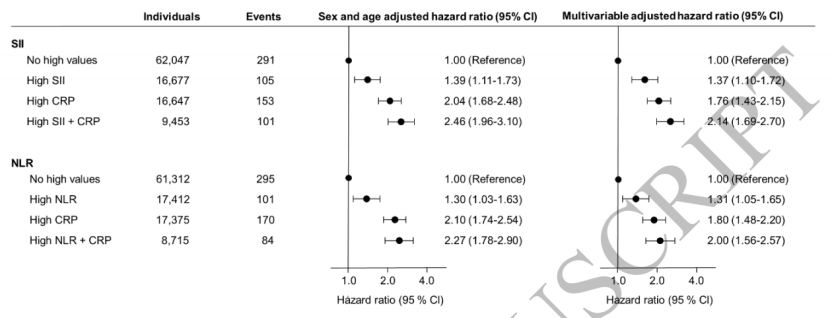
图3 SII或NLR与CRP联合升高时的银屑病发病风险
机制解析:全身炎症如何驱动银屑病发病?


中性粒细胞、淋巴细胞等免疫细胞比例失调(如NLR升高),会打破皮肤局部免疫平衡。例如,中性粒细胞过度活化可释放大量促炎细胞因子(如IL-17、TNF-α),激活皮肤角质形成细胞和树突状细胞,启动银屑病特征性的Th17免疫应答。
CRP作为经典炎症标志物,其水平升高反映体内慢性炎症状态。持续的低度炎症会诱导血管内皮生长因子(VEGF)、趋化因子等表达,促进皮肤血管新生和免疫细胞浸润,为银屑病发生提供“炎症土壤”。
SII综合血小板、中性粒细胞、淋巴细胞的动态变化,更全面反映全身炎症网络。血小板激活后释放的血小板源性生长因子(PDGF),可直接刺激角质形成细胞增殖;同时,血小板与中性粒细胞的相互作用(如形成中性粒细胞胞外诱捕网,NETs),会加剧皮肤局部免疫损伤,最终触发银屑病




➤因果关系确认
队列研究虽显示炎症标志物先于银屑病发生,但无法完全排除残余混杂(如未测量的遗传因素、肠道菌群紊乱)。未来需通过孟德尔随机化、干预性试验(如抗炎治疗后观察银屑病发病率变化)进一步确认因果关系。
➤种族与地域差异
研究人群为丹麦白人,结果能否推广至亚洲、非洲等其他种族?不同地域的环境因素(如紫外线暴露、感染流行率)如何影响全身炎症与银屑病的关联?这些需多中心、跨种族队列研究补充。
➤精准阈值界定
目前仅基于百分位数划分标志物水平,缺乏临床实践中“高危/低危”的精准阈值(如CRP具体多少mg/L时银屑病风险显著升高)。后续需结合机器学习,构建个性化风险预测模型,优化临床决策。


参考文献:
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
