1979年,Weiden等人在《The New England Journal of Medicine》上发表的论文描述了异基因骨髓移植后的移植物抗白血病(GvL)效应,首次清晰且系统地证明了人免疫系统清除癌细胞的能力。具体而言,西雅图研究团队发现接受异基因骨髓移植并发生
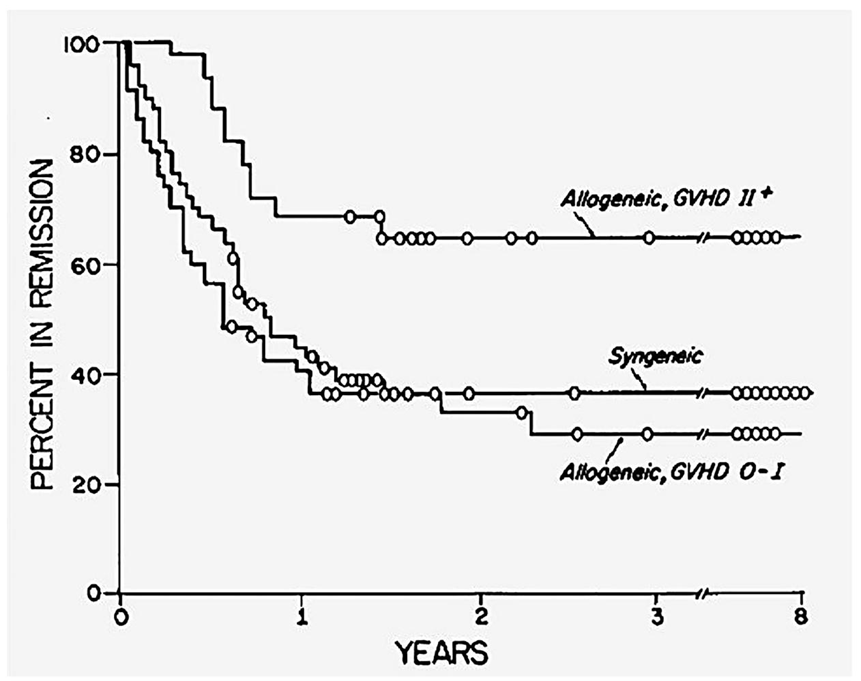
图1 根据Kaplan-Meier方法预估的
GvL效应的发现推动了大量关于如何进一步利用“免疫力量”的研究,最终产生了如今多种免疫疗法,其中包括骨髓移植最直接的衍生技术——过继性T细胞疗法。随着对GvL效应的认识,临床医生开始通过输注活性供体淋巴细胞的方法来治疗移植后复发的患者,少数患者获得持续缓解,但多数患者的GvHD恶化。因此我们需要提升治疗的效力与特异性。
到20世纪80年代,小鼠模型研究已证实能够通过识别、分离和扩增肿瘤反应性T细胞,清除小鼠体内的已成型肿瘤。随之而来的问题是如何应用于人体。Phil Greenberg和Stan Riddell以巨细胞病毒(CMV)为模型,开创性地建立了从骨髓供体中识别分离CMV反应性T细胞的方法:通过CD3/CD28刺激进行体外扩增,再将这类细胞回输注至移植后患者体内。令人振奋的是,这些过继性输注的T细胞成功重建了抗CMV免疫,有效保护了患者免受CMV疾病的侵袭。这成为人类历史上首次实现抗原特异性细胞免疫在个体间成功转移的范例。
随后,研究方向转向开发识别人肿瘤特异性或
尽管现有疗法仍存在不足且价格昂贵,但研发进展速度令人瞩目,可以预见未来可将拥有在体内进行T细胞基因修饰的方法。这一切都始于对GvL效应的发现。
参考文献:
Appelbaum FR. Graft-<i>versus</i>-leukemia. Haematologica 2025; 110(6):1243-1244; https://doi.org/10.3324/haematol.2025.287401

戳“阅读原文”,查看更多内容
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)