慢性淋巴细胞白血病(CLL)是一类在中老年群体中较为常见的B细胞恶性肿瘤。近年来其治疗格局已从传统化疗转向靶向治疗1-2。布鲁顿酪氨酸激酶抑制剂(BTKi)的广泛应用显著延长了患者生存期,但长期治疗所引发的获得性耐药,限制了疗效的持续性3。匹妥布替尼作为非共价BTKi,以独特的结合方式克服部分耐药机制,为复发/难治性(R/R)患者提供了新的治疗手段。
近期,血液学顶级期刊《Blood》(IF=23.1)在线发表了题为“Genomic Determinants of Response and Resistance to Pirtobrutinib in Relapsed/Refractory Chronic Lymphocytic Leukemia”的重要研究,系统解析了R/R CLL患者中基因组特征与匹妥布替尼疗效及耐药之间的关联4。为深入理解该研究的学术价值与临床意义,医脉通特邀周继豪教授与李回军教授共同解读这一研究成果,并就其在CLL精准治疗领域的潜在影响进行前瞻性探讨。
入组245例经cBTKi治疗(伊布替尼89%、阿可替尼16%、泽布替尼3%)的R/R CLL患者(图1),既往中位治疗线数为4(范围:1-11)。数据截止时,245例患者的总缓解率(ORR)为82%,中位治疗持续时间为20.7个月(95%CI:18.4-24.0个月),33%的患者仍在接受治疗。
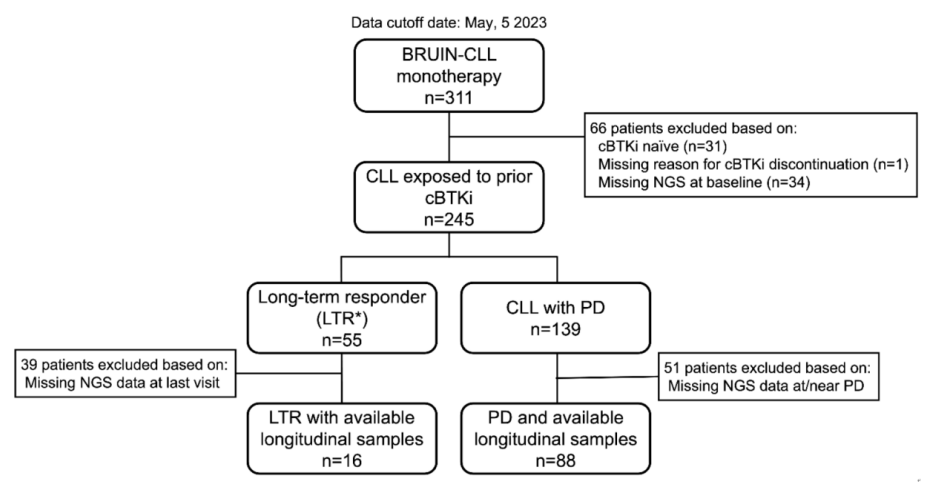
图1 纳入本研究的患者流程图
基线常见突变包括:BTK(43%)、TP53(38%)、SF3B1(25%)、NOTCH1(23%)、ATM(19%)、XPO1(11%)、PLCG2(9%)和BCL2(8%)。其中最常见的BTK突变包括C481S(85%)、C481R(10%)、C481F(6%)和C481Y(4%),C481S突变的中位变异等位基因频率(VAF)最高(25%)。非C481位点的BTK突变主要包括L528W(3%)和T474I(5%);其他BTK突变(T474F/M/S、A428D、D149G和E7A)较为罕见。染色体异常包括:13q缺失(43%)、17p缺失(28%)、11q缺失(23%)和12号染色体三体(17%)(图2)。
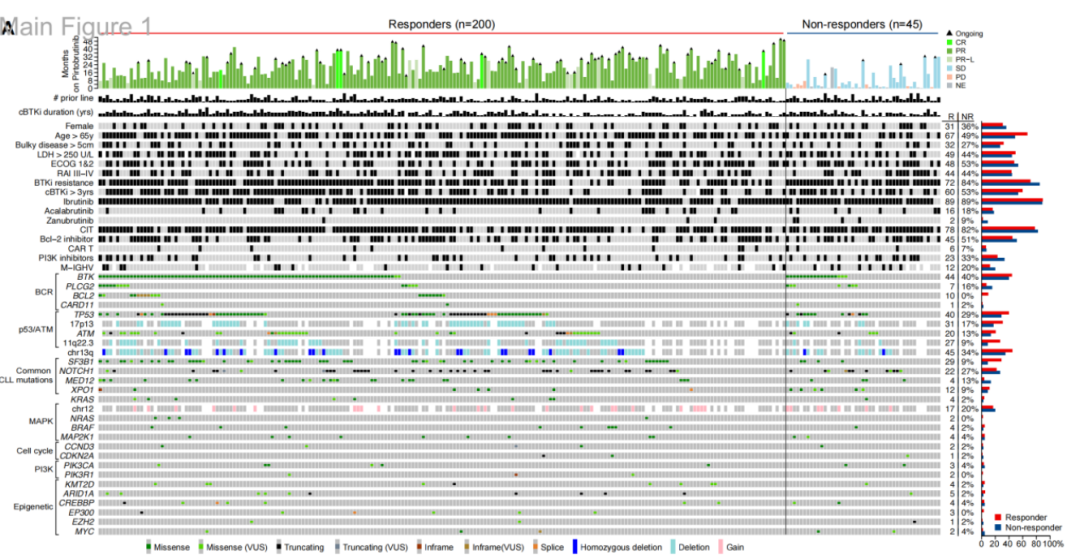
图2 对匹妥布替尼有应答和无应答的CLL患者基线时的瀑布图
既往cBTKi治疗情况与基线BTK突变的关系:基线伴BTK突变的患者既往接受cBTKi治疗的持续时间显著长于基线无BTK突变的患者(4.1年 vs 2.6年,p<0.0001)。但基线存在单个BTK突变与多个BTK突变的患者的治疗持续时间无显著差异(4.0年 vs 4.2年,p=0.97)。既往cBTKi治疗持续时间与基线时BTK突变的平均VAF呈正相关(ρ=0.25,p=0.009)(图3)。
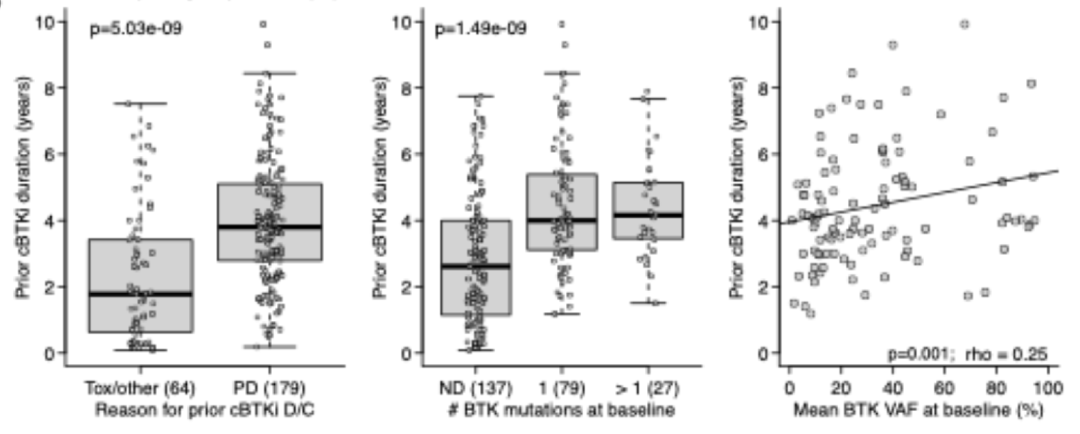
图3 既往cBTKi治疗持续时间与停药原因、基线BTK突变状态以及基线平均BTK VAF的相关性
既往因PD停用cBTKi的患者BTK突变频率(52% vs 17%,p<0.01,q<0.01)和IGHV未突变频率(26% vs 9%,p<0.01,q<0.01)显著高于因毒性反应或其他原因停药的患者(图4)。
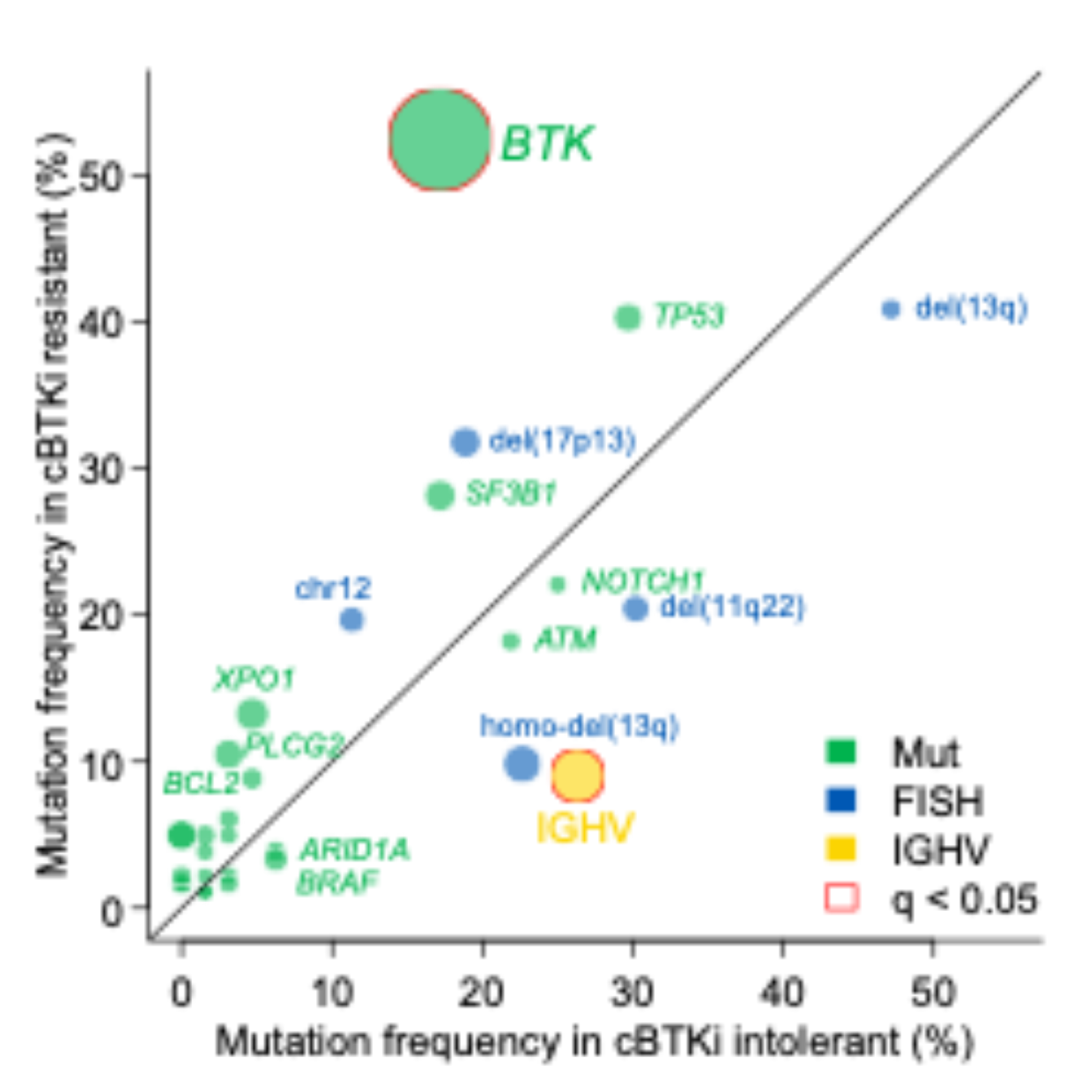
图4 因PD停药的患者与因毒性/其他原因而停药的患者的基线突变频率比较
匹妥布替尼应答者(n=200)与无应答者(n=45)在大多数基线临床和基因组特征的频率上无统计学差异(图2)。应答者与无应答者的BTK突变频率(44% vs 40%,p=0.74,q=0.93)、TP53突变频率(40% vs 29%,p=0.23,q=0.75)及IGHV突变频率(12.2% vs 20%,p=0.21,q=0.75)相似。无应答者的MED12突变频率(4% vs 13%,p=0.017,q=0.22)和PLCG2突变频率(7% vs 16%,p=0.07,q=0.50)高于应答者(图5)。
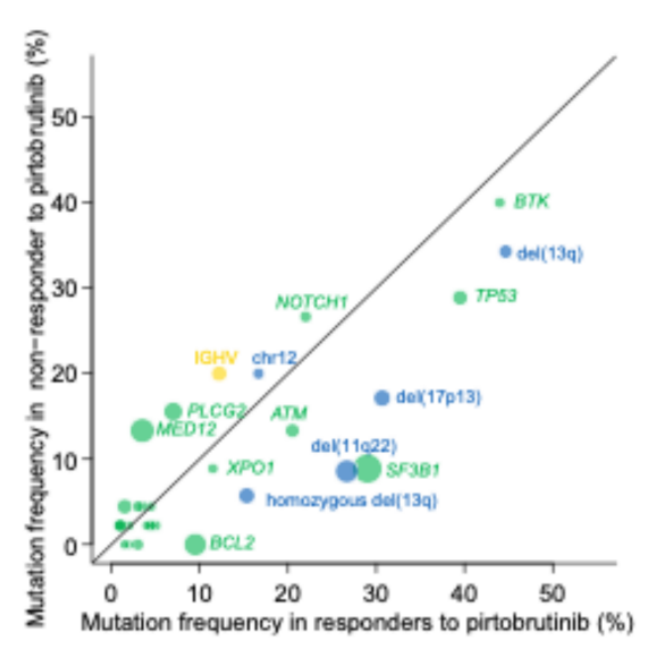
图5 应答者与无应答者的基线突变频率比较
既往cBTKi耐药、乳酸脱氢酶(LDH)升高、美国东部肿瘤协作组(ECOG)体力状态评分、既往接受BCL-2抑制剂、磷脂酰肌醇3-激酶(PI3K)抑制剂或化学免疫治疗(CIT)治疗史,以及PLCG2或EZH2基因突变(q<0.05)与患者疾病进展风险增加相关(图6)。
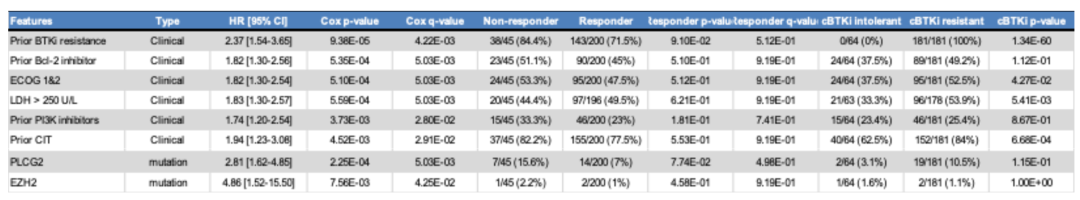
图6 匹妥布替尼疗效的影响因素及其与cBTKi停药的相关性
中位随访29个月,139例(57%)患者接受匹妥布替尼治疗后出现PD。其中88例患者拥有基线和疾病进展时的配对PBMC样本,可进行测序分析。采用5%的检测限时,54例(61%)患者基线时存在的119种突变在疾病进展时未被检出(即突变清除)(图7)。匹妥布替尼治疗使24例患者的36种BTK突变得到清除。无BTK突变清除的患者与有BTK突变清除的患者,其ORR无显著差异(81% vs 88%,p=0.75)。被清除的突变多为C481x替换突变。总体而言,43例基线存在BTK C481x突变的患者中,36例(84%)在疾病进展时出现C481x突变减少或清除。
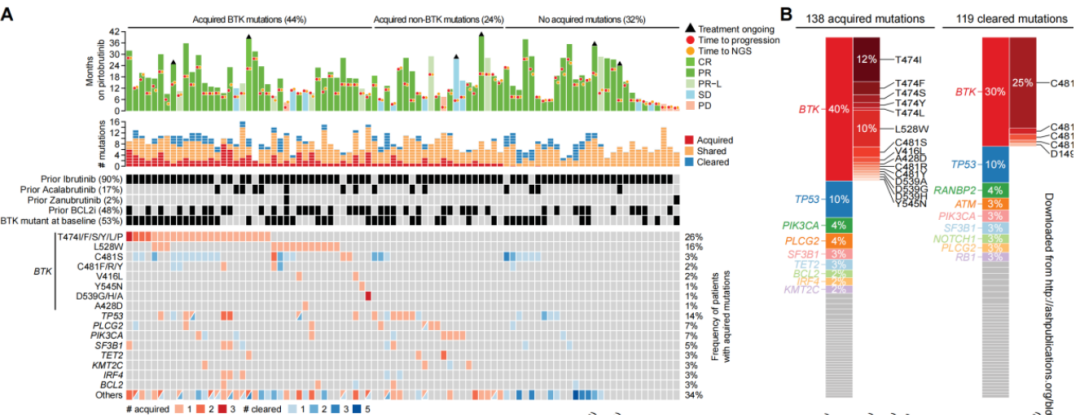
图7 匹妥布替尼治疗下的克隆进化。A:清除突变与获得性突变的瀑布图;B:按基因和BTK残基展示获得性突变与清除突变分布的柱状图,每种颜色代表一个基因
疾病进展时,88例患者中有60例(68%)检测到138种获得性突变:其中44%出现获得性BTK突变,24%出现其他基因获得性突变,32%未检测到任何获得性突变(图7)。有获得性突变与无获得性突变的患者治疗持续时间无显著差异(16.5个月 vs 16.1个月,p=0.91)。最常见的获得性突变发生在BTK(39例患者中55种)、TP53(12例患者中14种)、PLCG2(6例患者中6种)和PIK3CA(6例患者中6种)(图7)。获得性BTK突变中最常见的位点包括:T474X看门基因突变(T474I/F/S/Y/L/P)、激酶功能受损的L528W突变、C481S/R/Y突变,以及其他位于ATP结合口袋附近的突变(D539A/G/H、V416L、Y545N、A428D)(图8)。采用更灵敏的检测方法发现,49种获得性BTK突变中有18种(37%)在基线时已以低等位基因频率存在。共有31例患者在疾病进展时提供了足够的DNA样本,并使用更高灵敏度的测序方法进行了重新测序,所有31例患者疾病进展时均能检测到获得性突变(获得性BTK突变39%,其他突变61%)。
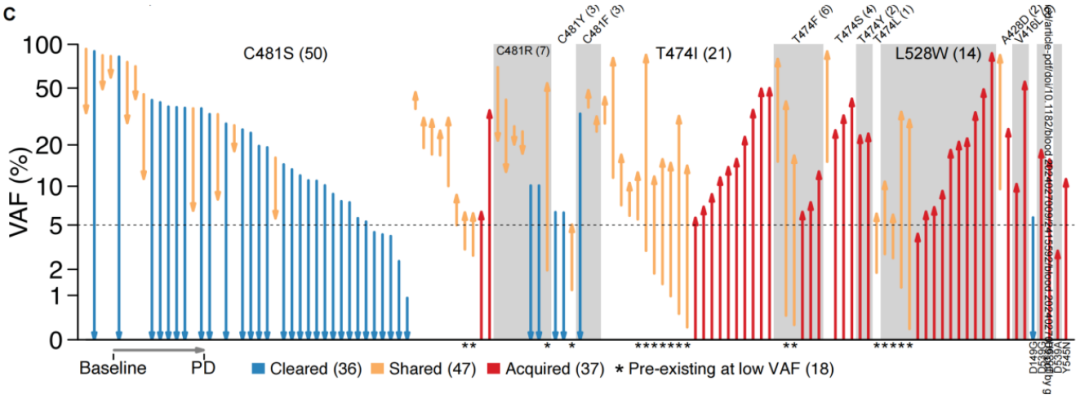
图8 基线和/或PD时检测到的120种BTK突变在基线与进展时的VAF
为进一步分析匹妥布替尼耐药的纵向模式,研究对疾病进展前的多个时间点样本进行测序。67例患者有基线、治疗期间及进展时的匹配PMBC可供检测,有30例在疾病进展时出现获得性BTK突变;其中13例(43%)在疾病进展前(最早提前7.6个月)就检测到获得性BTK突变(图9)。
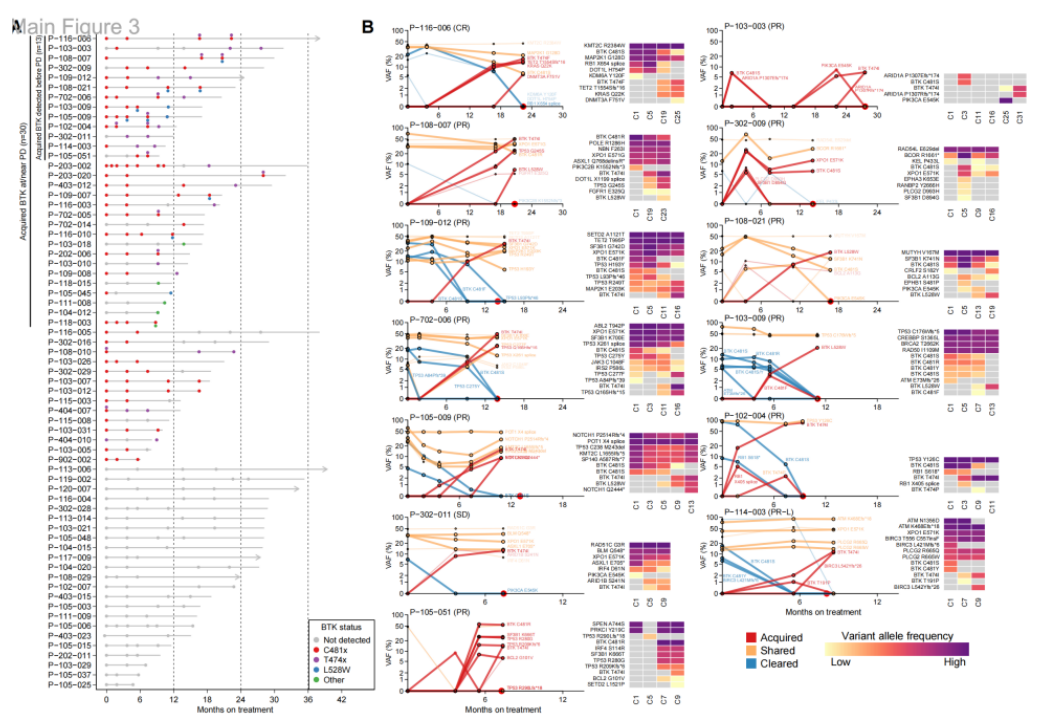
图9 匹妥布替尼耐药的纵向模式。A:67例PD患者中检测到BTK突变的时间线;B:13例在PD前检测到BTK突变的患者在多个时间点的VAF
值得注意的是,对于出现多种BTK突变的患者,不同突变的VAF存在差异,且在可评估的情况下显示位于不同等位基因上,提示这些突变可能存在于不同的亚克隆中(图10)。

图10 BTK的克隆性与基因定相。A:基线时检测到多个BTK突变的患者的BTK VAF;B:成对BTK突变的定位分析结果,以确定它们是否同源;C:一个具有两个同源BTK突变的代表性患者的IGV截图
研究还分析了接受匹妥布替尼治疗后获得长期缓解(LTR)的CLL患者的克隆进化情况。54例缓解患者接受匹妥布替尼治疗超过24个月,且在数据截止时仍存活且无明确PD;其中16例LTR患者拥有最近一次随访时采集的样本,可进行纵向测序分析。
对比患者基线和最近一次随访时的样本发现,16例LTR患者中有14例(88%)检测到25种获得性突变(图11),其中8例(57%)存在多种获得性突变,最多可检测到3种。然而纵向样本分析显示,与43%的PD患者中观察到的情况相反,中间时间点(第5周期)未检测到获得性BTK突变(图11B)。此外,长期接受匹妥布替尼治疗使12例LTR患者的35种突变得到清除,其中6例患者的8种BTK突变(6种C481S、2种C481Y)被清除。LTR患者中突变的清除可能与循环CLL细胞的清除有关。
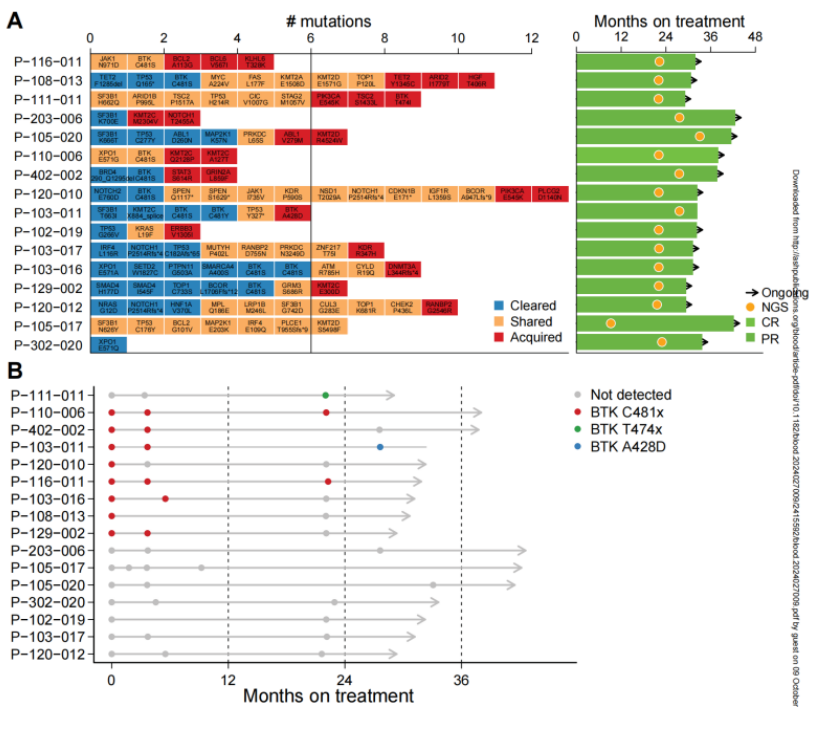
图11 LTR患者的获得性耐药。A:16例LTR患者的获得性、共享及清除的突变;B:16例LTR患者在不同时间点检测BTK突变的时间线
周继豪教授
CLL的治疗在进入靶向时代后,疾病管理的核心挑战已从“如何实现初始缓解”转变为“如何克服耐药与延长疗效”。既往研究多聚焦于cBTKi的耐药机制,而对后续治疗方案(尤其是非共价BTKi)所引发的克隆演变规律认知尚浅。本研究在大样本中系统解析了匹妥布替尼疗效与耐药的影响因素,结果具有临床指导意义。首先,研究发现在既往接受cBTKi的R/R CLL患者中,BTK为最常见的突变,从而导致了cBTKi的耐药。而非共价BTKi匹妥布替尼,由于其与BTK蛋白ATP口袋的位点非共价结合,重建对BTK的抑制,实现对CLL细胞的杀伤。其次,该研究还显示了在治疗压力的选择作用下,患者出现了新的耐药突变,其中BTK T474X与L528W为主要突变类型,且基线存在L528W的患者PFS更短。但由于该研究是从已经进展的患者中进行回顾性检测,这部分患者的PFS要短于总体人群,且基线L528W突变的人数过少,因此仍需要未来进行前瞻性的研究进一步回答对于匹妥布替尼疗效的影响。因此,该研究不仅填补了非共价BTKi治疗R/R CLL克隆演变机制的认知空白,更为临床制定“cBTKi-非共价BTKi”序贯治疗策略、优化个体化耐药监测方案提供了关键循证依据。
李回军教授
匹妥布替尼作为新一代非共价、高选择性的BTKi,其核心优势在于不依赖BTK C481残基结合,可同时抑制野生型与C481突变型BTK。BRUIN研究的亚组分析显示,无论R/R CLL患者是否存在C481突变,其接受匹妥布替尼治疗的ORR和PFS相似5,6。而对于本研究中发现的最常见的获得性BTK突变T474X和L528W,当基线存在突变时,其ORR分别为93%(13/14)和75%(3/4),与总人群的ORR(82%,200/245)相似。因此,临床实践中,仍无法使用单个基因的突变情况来预测匹妥布替尼的疗效及耐药。研究还显示,在治疗超24个月且无进展的长期响应(long-term response)患者中,12例实现了35种突变的清除,包括6例患者的8种BTK突变(6种C481S、2种C481Y),印证了匹妥布替尼对耐药克隆的持续清除能力与长期获益的关联。同时,研究中还观察到TP53克隆的清除,说明匹妥布替尼对R/R CLL的杀伤作用不受TP53突变的影响。这些结论不仅指导我们如何用好匹妥布替尼,更深远的意义在于,它为如何序贯后续疗法以及设计联合治疗策略,以避免或延迟这些特定耐药突变的出现,提供了重要的科学依据。

周继豪 教授
深圳市人民医院血液内科行政负责人,深圳市血液内科专业质量控制中心主任
主任医师,博士/博士后,硕导
广东省医学会内科学分会常委、血液学分会常委、血液学分会青委会副主委
深圳市医师协会血液科医师分会会长
深圳市医学会血液学分会副主委
深圳市健康管理协会血液病分会副主委

李回军 教授
深圳市人民医院血液内科 副主任医师
学术任职:
深圳市抗癌协会罕见血液肿瘤专业委员会 副主任委员
广东省抗癌协会血液肿瘤专业委员会 委员
广东省医学教育协会血液免疫诊断与治疗专业委员会 委员
广东省老年保健协会血液病专业委员会 委员
广东省预防医学会血液肿瘤防治专业委员会 委员
广东省精准医学应用学会淋巴瘤分会 委员
深圳市医师协会血液科医师分会理事会 常务理事
广州抗癌协会罕见肿瘤专业委员会 委员
深圳市医师协会淋巴瘤专业委员会 常务理事
深圳市健康管理协会血液病专业委员会 常务委员
深圳市抗癌协会血液肿瘤专业委员会 常务委员