

前言

一年一度的肿瘤领域盛会——2025年欧洲肿瘤内科学会年会(ESMO 2025)将于10月17日至21日在德国柏林隆重举行,届时将揭示众多前沿临床科研成果,并吸引全球知名专家教授进行研讨,共同促进临床肿瘤学的发展与进步。

2234P |
研究背景
胰腺癌具有高度侵袭性且预后极差,尽管目前的一线治疗方案如AG方案(
研究方法
mPC患者接受以下治疗方案:恩沃利单抗(400 mg,皮下注射,第1天)、Rh-endostatin(210 mg,静脉持续输注72小时)、吉西他滨(1000 mg/㎡,静脉输注,第1天和第8天),以及白蛋白结合型紫杉醇(125 mg/㎡,静脉输注,第1天和第8天),每3周为一个周期,直至疾病进展、不可接受的毒性或患者拒绝继续治疗。主要终点为安全性和客观反应率(ORR),次要终点包括无进展生存期(PFS)、总生存期(OS)、疾病控制率(DCR)和生活质量(QoL)。
研究结果
共16例mPC患者可进行疗效评估。中位年龄为64.5岁(范围:28-77岁),其中男性10人,女性6人。中位随访时间为9.97个月。结果显示,ORR为37.5%,DCR为93.75%。
表 疗效分析

中位无进展生存期(mPFS)为6.5个月,mOS为10.5个月。
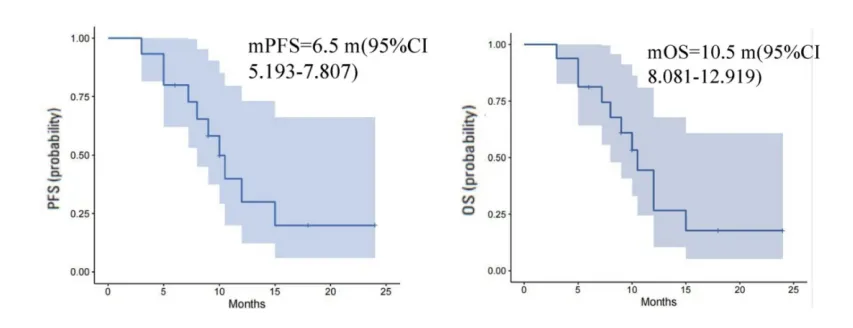
图 PFS和OS分析
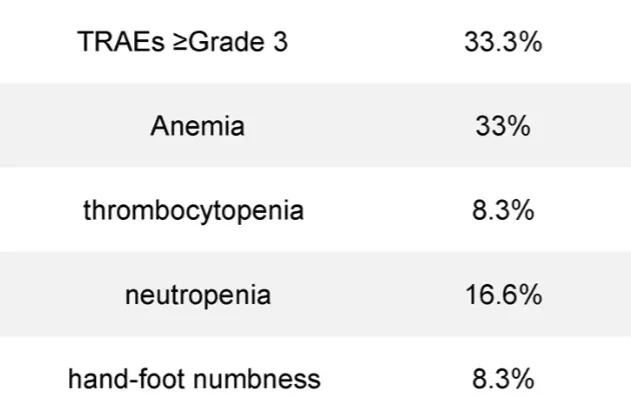
3级及以上治疗相关不良事件(TRAEs)发生率为33.3%,其中最常见的为
表 安全性分析
研究结论
初步数据显示,恩沃利单抗+Rh-endostatin+AG方案作为mPC一线治疗,显示出良好的疗效和较好的耐受性。

2260eP | AG/mFOLFIRINOX+
研究背景
本项回顾性、单臂、II期临床研究旨在分析mFOLFIRINOX方案或AG方案联合替雷利珠单抗作为一线治疗,用于局部晚期/转移性胰腺导管腺癌(mPDAC)的疗效和安全性。
研究方法
入组患者接受替雷利珠单抗(200 mg,Q3W)联合mFOLFIRINOX方案(Q4W)或AG方案(Q3W)治疗。主要研究终点是根据RECIST v1.1标准评估的ORR,次要研究终点包括mPFS和中位总生存期(mOS)。
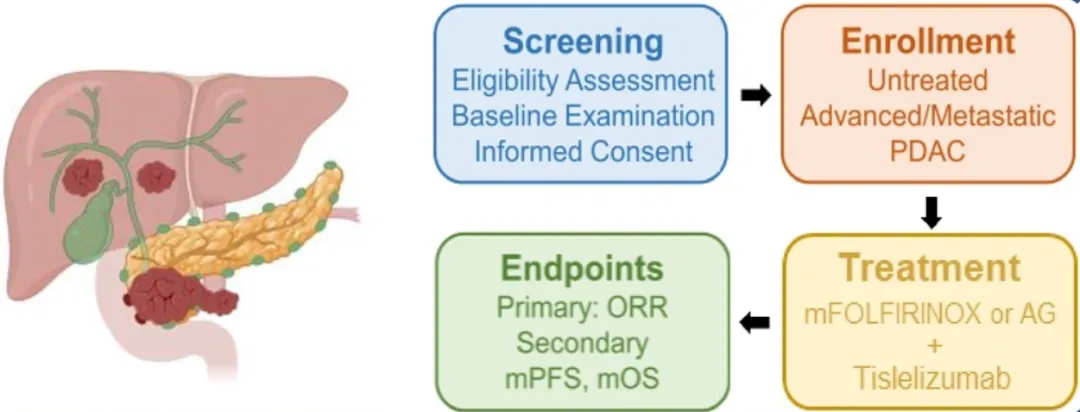
图 研究设计
研究结果
2021年6月至2024年5月,共纳入15例患者。截至2025年3月,15例患者(mFOLFIRINOX+替雷利珠单抗组6例,AG+替雷利珠单抗组9例)可进行疗效评估。在mFOLFIRINOX +替雷利珠单抗组中,ORR为16.7%(1/6),其中3例患者通过转化化疗成功实现肿瘤降期并接受了根治性手术切除。在AG+替雷利珠单抗组中,ORR为55.6%(5/9),其中2例患者成功转化并接受了根治性手术切除。
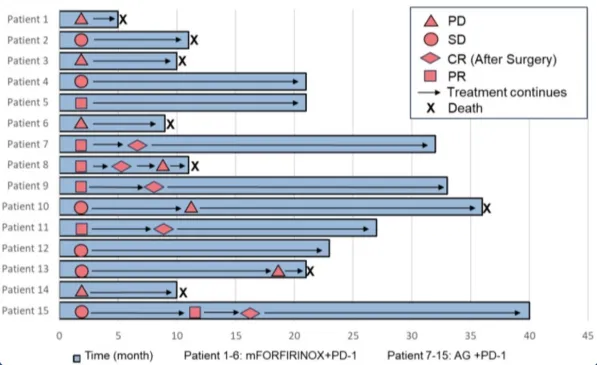
图 疗效结果
mFOLFIRINOX + 替雷利珠单抗组的mPFS和mOS分别为15.0个月和36.0个月。AG+替雷利珠单抗组的mPFS和mOS分别为6.0个月和11.0个月。
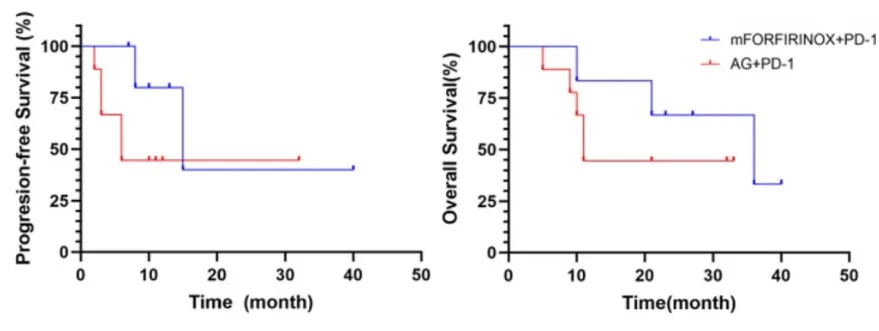
图 PFS和OS分析
最常见的不良事件(AEs)为肝毒性,发生率为26.7%(4/15),其中1例患者出现3级或以上不良反应。
研究结论
与标准的AG/mFOLFIRINOX治疗相比,AG/mFOLFIRINOX联合替雷利珠单抗方案在mPDAC患者中显示出更高的临床活性和可控的安全性,尤其是在不可切除的胰腺癌患者中。
参考文献:
Zhengxiang Han, et al. Envafolimab Combined with Recombinant Human Endostatin and Chemotherapy as First-line treatment in metastatic pancreatic cancer: A single-arm,exploratory, phase II trial. 2025 ESMO 1482P
Kang Chen, et al. AG/mFOLFIRINOX Plus Tislelizumab as First-Line Therapy for Locally Advanced/Metastatic Pancreatic Ductal Adenocarcinoma: A Phase 2 Clinical Study. 2025 ESMO 1484P
撰写:Aurora
审核:Aurora
排版:Aurora
执行:Babel
