在一年前的美国临床肿瘤学会(ASCO)年会上, III期临床研究KEYNOTE-177的分析结果以LBA(Late-breaking Abstract)的形式首次发布,并引起轰动1。此后不到一个月(2020年6月29日),美国食品药品监督管理局(FDA)基于该研究中无进展生存期(PFS)的阳性结果,批准PD-1免疫检查点抑制剂
当前,K药单药已成为不可切除或转移性MSI-H/dMMR结直肠癌的一线治疗新标准。KEYNOTE-177不仅改写了美国国立综合癌症网络(NCCN)结直肠癌诊疗指南,在国内,也获得刚发布的2021年中国临床肿瘤学会(CSCO)结直肠癌诊疗指南的I级专家推荐。
尽管如此,KEYNOTE-177的另外一个研究主要终点 – OS是否也能获得阳性结果仍引人关注,而且关注焦点不仅是中位OS有无改善,还有K药单药一线治疗的3年或4年的OS率是否足够“惊艳”。
KEYNOTE-177是一项旨在评估K药单药对比标准治疗 (FOLFOX或FOLFIRI化疗±靶向
根据今天ASCO正式公布的KEYNOTE-177 最终OS数据分析结果2,在中位随访逾44个月(K药治疗组44.5[36.0-60.3]个月, 对照组44.4[36.2-58.6]个月时),
有60%的对照组患者在出现疾病进展后接受了PD-1/PD-L1免疫检查点抑制剂治疗;
K药组的中位OS尚未达到,对照组中位OS为36.7个月, 死亡风险降低26%(HR 0.74; 95% CI, 0.53-1.03; P=0.0359);K药治疗组显示了OS获益趋势, 36个月的OS率为61%,对照组为50%。
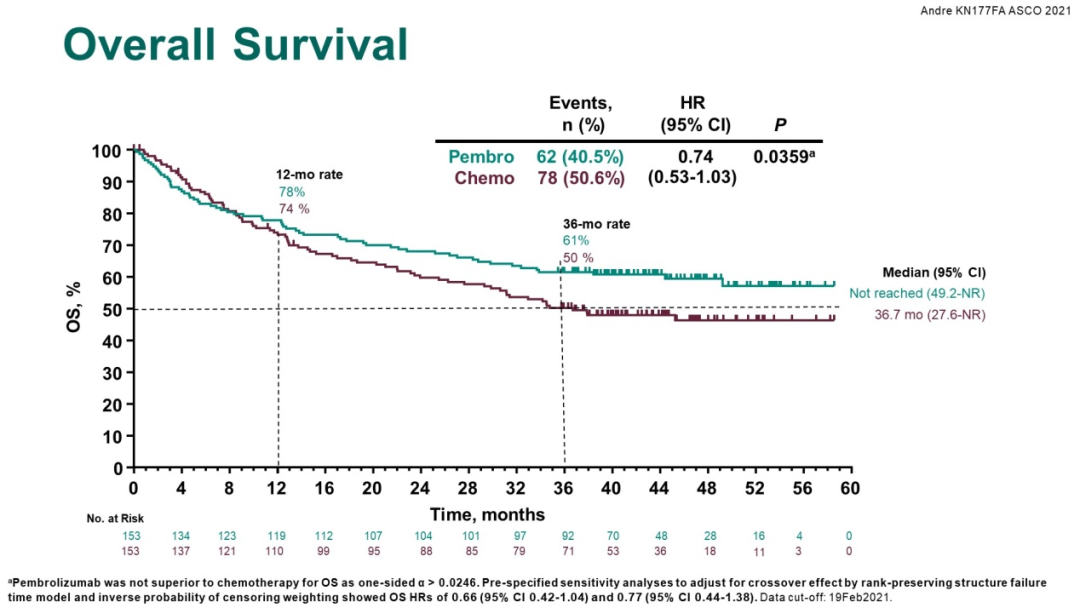
KEYNOTE-177 最终OS分析结果2
既往研究结果显示,FOLFOX或FOLFIRI化疗±靶向贝伐珠单抗或西妥昔单抗治疗晚期结直肠癌的OS为21.5个月3。KEYNOTE-177对照组的中位OS达到36.7个月,远高于既往研究的OS结果,提示二线免疫治疗为对照组患者带来的OS获益很大程度上“掩盖”了K药一线治疗带来的OS优势。
此次发布摘要也更新了PFS,以及ORR和安全性等次要终点的数据分析结果2:
K药组的中位PFS为16.5个月, 是对照化疗组(8.2个月)的两倍(HR=0.59;95%CI:0.45~0.79;P=0.0002);
K药组最终确定的ORR为45.1%(20 CR, 49 PR),对照组为33.1%(6 CR, 45 PR);
K药组的中位缓解持续时间(DOR)未达到 (2.3+ ~ 53.5+),对照组为10.6 个月 (2.8 ~ 48.3+);
K药组3级以上治疗相关不良事件(TRAE)发生率为21.6% ,对照组为66.4%。
虽然由于对照组二线接受免疫治疗的比例高而导致K药组仅显示OS获益趋势,而未能达到统计学意义,但是在36个月时仍然有61%的患者存活,而且仍比对照组高出11个百分点,这为K药单药作为MSI-H/dMMR晚期结直肠癌标准一线治疗方案带来了坚实的循证医学证据。
虽然当前有多个PD-(L)1免疫检查点抑制剂在全球以及国内获批,但免疫单药或联合一线治疗晚期实体瘤患者的长期OS随访数据却很少,而且多数数据来自KEYNOTE系列研究。
在2020 ASCO大会上,K药单药一线治疗晚期恶性黑色素瘤中位随访66.8个月的随访结果显示5年OS 率为43%4;在2020年ESMO大会上,K药单药一线治疗PD-L1高表达(PD-L1≥50%)的晚期非小细胞肺癌中位随访59.9个月的KEYNOTE-024随访结果显示5年OS率为 31.9% 5。
K药单药一线治疗MSI-H/dMMR型mCRC适应证的上市申请已于2020年11月12日被国家药品监督管理局(NMPA)正式受理,并且有望在近日获批!该适应证一旦获批,K药将成为国内首个依据MSI-H/dMMR状态指导临床实践的PD-1免疫检查点抑制剂,是国内精准免疫治疗的一个里程碑。期待该适应证的获批在为中国MSI-H/dMMR的转移性结直肠癌患者带来“去化疗”、高质量长期生存的同时,也推动精准肿瘤免疫治疗在国内的临床实践更上一层楼。