
聚前沿文献之声,解泌尿学术之惑
聚前沿文献之声,解泌尿学术之惑,这里是聚焦
本期与我们用声音见面的是浙江大学医学院附属邵逸夫医院成晟教授,他将与大家一同分享近期发表于《The Lancet Oncology》杂志(影响因子:35.9)的一项基于STAMPEDE平台的随机III期试验,研究评估了在转移性前列腺癌患者中,

联合疗法改善了转移性激素敏感性前列腺癌(metastatic hormone-sensitive prostate cancer,mHSPC)的预后。目前,ADT联合雄激素受体通路抑制剂(androgen receptor pathway inhibitor,ARPI),联合或不联合多西他赛已成为mHSPC的标准系统治疗方案,但ADT单药仍是老年和衰弱患者的常用治疗方案。ADT和ADT联合治疗无疑是有效的,但可能引起代谢不良反应,最明显的是体重增加、肌肉或骨质流失、严重心血管事件的增加等。前列腺癌患者中,老年患者和具有合并症的患者比例较高,这些患者本就深受基础疾病的困扰。此外,ARPIs价格较高,在中低收入国家可及性较低。而预计未来这些国家的确诊前列腺癌患者的数量将大幅增长。因此,亟需价格更低且同样安全有效的治疗策略。
二甲双胍是一种广泛用于治疗2型
已有临床试验探索了二甲双胍在前列腺癌中的治疗作用,但这些试验规模较小,且设计既包含单药治疗也包含各种联合方案。此外,有些研究仅关注代谢效应,而有些研究只评估其对癌症进展的影响。目前,现有研究均不具备足够的统计效力来证实二甲双胍治疗对前列腺癌患者生存的影响。STAMPEDE试验针对局部晚期或mHSPC患者进行了多种联合方案的评估,其中二甲双胍组评估了二甲双胍联合标准治疗的疗效,以确定二甲双胍对患者生存是否有增效作用以及其对ADT所致的代谢不良效应是否有缓解作用。本研究报告了转移性前列腺癌患者的结果[1]。
STAMPEDE是一项多臂、多阶段、随机化III期试验,纳入了经传统同位素骨扫描和计算机断层扫描(computed tomography,CT)分期的高危局部晚期或转移性前列腺腺癌患者。本文报告了STAMPEDE最新研究问题的结果,该部分旨在非糖尿病(
该试验从英国和瑞士112家医院招募符合STAMPEDE方案的患者。患者按1:1随机分入标准治疗组或标准治疗+二甲双胍(850 mg,每日2次)治疗组。研究采用最小随机化法进行分组,分层因素包括:随机化医院、年龄(>70岁 vs ≤70岁)、WHO体能状态评分(0 vs 1或2)、ADT类型、长期规律服用
患者基线情况
2016年9月5日至2023年3月31日期间,共1874例转移性前列腺癌患者被随机分入标准治疗组(n=938)和标准治疗+二甲双胍组(n=936)。本研究报告了截至2024年7月3日随访期间,二甲双胍治疗组最终的主要分析结果。不同治疗组患者间的基线特征基本均衡,详见表1。患者的中位年龄为69岁(四分位距[interquartile range,IQR] 63-73),中位
表1 患者基线数据

在标准治疗+二甲双胍组936例患者中,897例(96%)确认已开始二甲双胍治疗,其中28例在治疗开始前30天内停用二甲双胍。患者从随机分组至开始二甲双胍治疗的中位时间为7天(IQR 3-14),至停止二甲双胍治疗的中位时间为39个月(IQR 13-未达到)。截至2024年7月3日数据锁定时,仍有287例患者在接受二甲双胍治疗。在510例停用二甲双胍的患者中,134例停药原因为过量的毒性。至末次病例报告表随访的中位时间为60个月(IQR 49-72);末次存活确认时间的中位数为69个月(IQR 60-79;使用死亡民事登记[Civil Registrations of Death,CRD]数据)。
肿瘤学结果
合并CRD数据之后,标准治疗组和标准治疗+二甲双胍组分别报告了473例和453例死亡事件,中位OS分别为61.8个月和67.4个月(风险比[hazard ratio,HR] 0.91,95%置信区间[confidence interval, CI] 0.80-1.03,p=0.15,详见图1)。研究未发现非比例风险的证据(p=0.14)。预先指定的亚组分析结果显示,在所有亚组中均未发现显著的疗效异质性。在高瘤负荷和低瘤负荷亚组中,标准治疗组 vs 标准治疗+二甲双胍组OS的HR值分别为0.79(95%CI 0.67-0.94,p=0.0072)和0.98(95%CI 0.78-1.23,p=0.87,图1),交互作用p值为0.12。
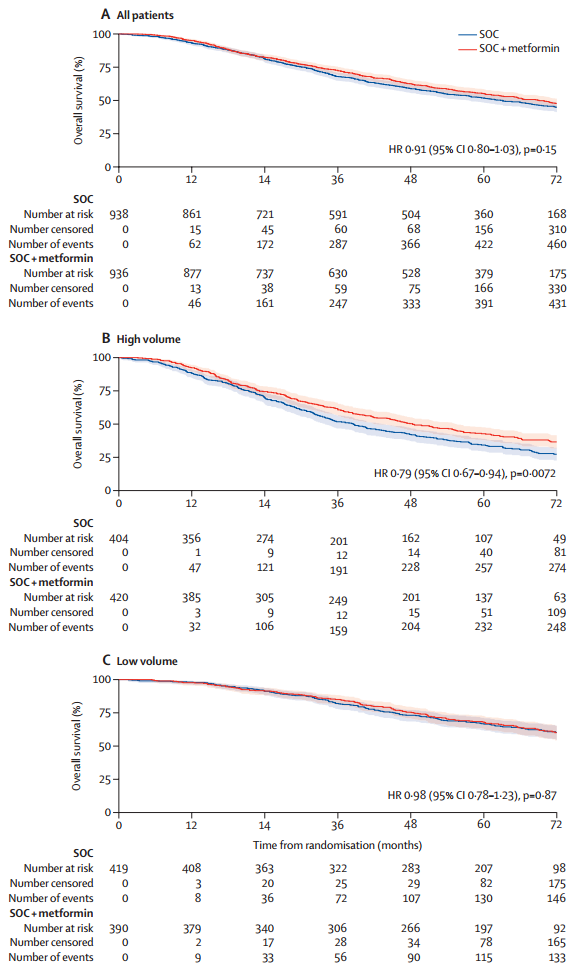
图1 不同治疗组和不同肿瘤负荷患者的OS
标准治疗组和标准治疗+二甲双胍组分别有400例和396例前列腺癌相关死亡。在总体人群中,研究未发现二甲双胍影响前列腺癌特异性生存的证据(HR 0.97,95%CI 0.85-1.12,p=0.70,见图2),各预设亚组间同样无显著的疗效异质性。在高瘤负荷和低瘤负荷亚组中,标准治疗组 vs 标准治疗+二甲双胍组前列腺癌特异性生存的HR值分别为0.85(95%CI 0.71-1.02,p=0.090)和1.06(95%CI 0.82-1.38,p=0.64,图2),交互作用p值为0.11。
标准治疗组和标准治疗+二甲双胍组分别有400例和396例无进展生存事件。在总体人群中,研究未发现二甲双胍影响无进展生存期的证据(HR 0.92,95%CI 0.81-1.04,p=0.16,见图2)。但是,研究发现与低瘤负荷患者相比(HR 1.06,95%CI 0.86-1.32,p=0.57),高瘤负荷患者(HR 0.76,95%CI 0.64-0.90,p=0.0011)的肿瘤负荷与治疗之间存在交互作用,p值为0.012。
在无转移性进展方面也观察到相似的趋势,标准治疗组和标准治疗+二甲双胍组分别有486例和461例事件,整体人群的HR为0.90(95%CI 0.79-1.02,p=0.93)。在高瘤负荷和低瘤负荷亚组中,标准治疗组 vs 标准治疗+二甲双胍组无转移性进展生存的HR值分别为0.74(95%CI 0.63-0.88,p=0.00054)和1.04(95%CI 0.83-1.31,p=0.72,图2),交互作用p值为0.013。
研究未发现二甲双胍对无失败生存期存在显著获益(HR 0.94,95%CI 0.84-1.05,p=0.30[标准治疗组和标准治疗+二甲双胍组分别有625例和618例事件,71%为PSA失败])。在高瘤负荷和低瘤负荷亚组中,标准治疗组 vs 标准治疗+二甲双胍组无失败生存的HR值分别为0.84(95%CI 0.72-0.98,p=0.03)和1.00(95%CI 0.83-1.21,p=0.99,图2),交互作用p值为0.15。
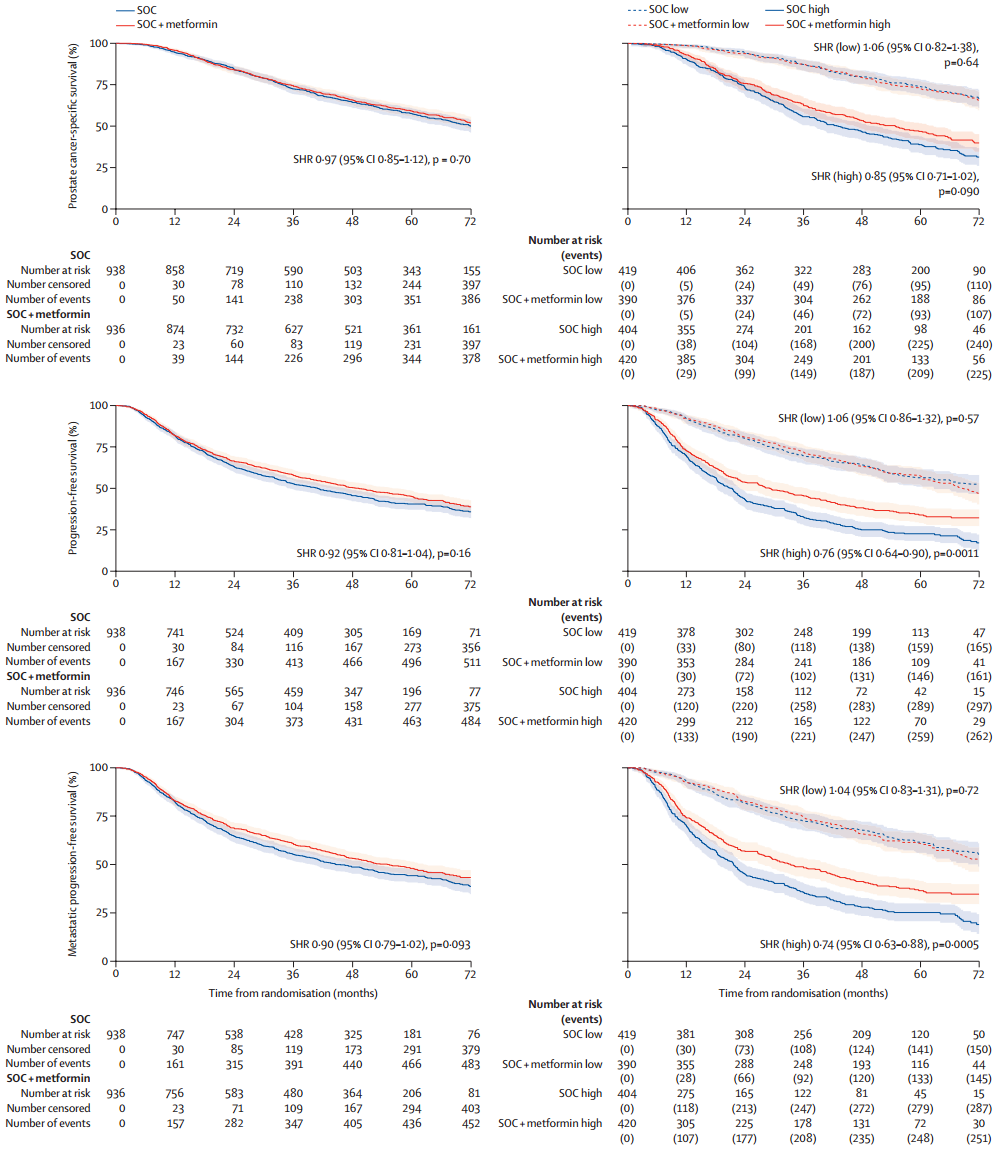
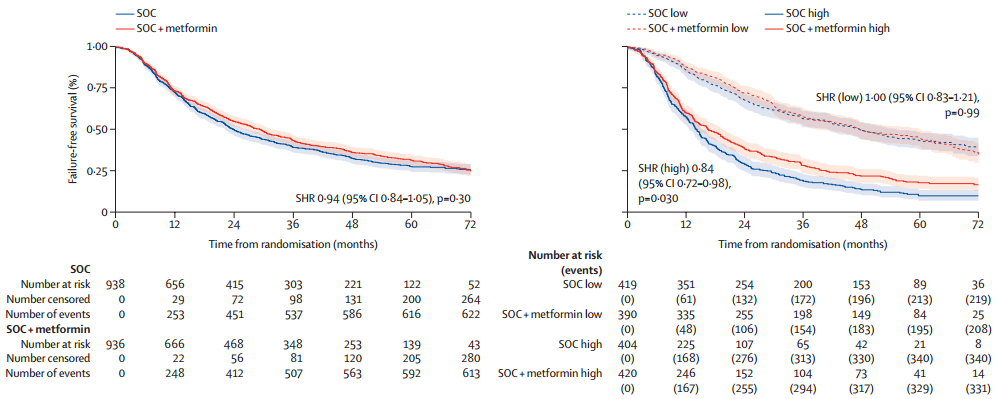
图2 不同治疗组和不同肿瘤负荷患者的前列腺癌特异性、无进展、无转移性进展和无失败生存期
代谢结果
研究发现,在第24周、48周和104周时,不同治疗组患者的体重增长差异显著(p均<0.0001)。在基线和104周体重数据可获得的583例患者中,标准治疗组患者104周时体重平均增加4.40 kg,而标准治疗+二甲双胍组患者104周时体重平均增加2.00 kg。此外,104周时,二甲双胍在以下代谢指标的改善方面均具有统计学优势:空腹血糖(p=0.0044)、总胆固醇(p=0.013)、低密度脂蛋白(p=0.0043)、HbA1c(p<0.0001)和腰围(p=0.038)。24周和48周的数据趋势与104周基本一致(除了腰围数据在前两个时间点无显著差异,见图3)。研究未发现两组在空腹甘油三酯和高密度脂蛋白方面存在显著差异。基线时肿瘤负荷与患者形态学和代谢相关参数无显著相关性。
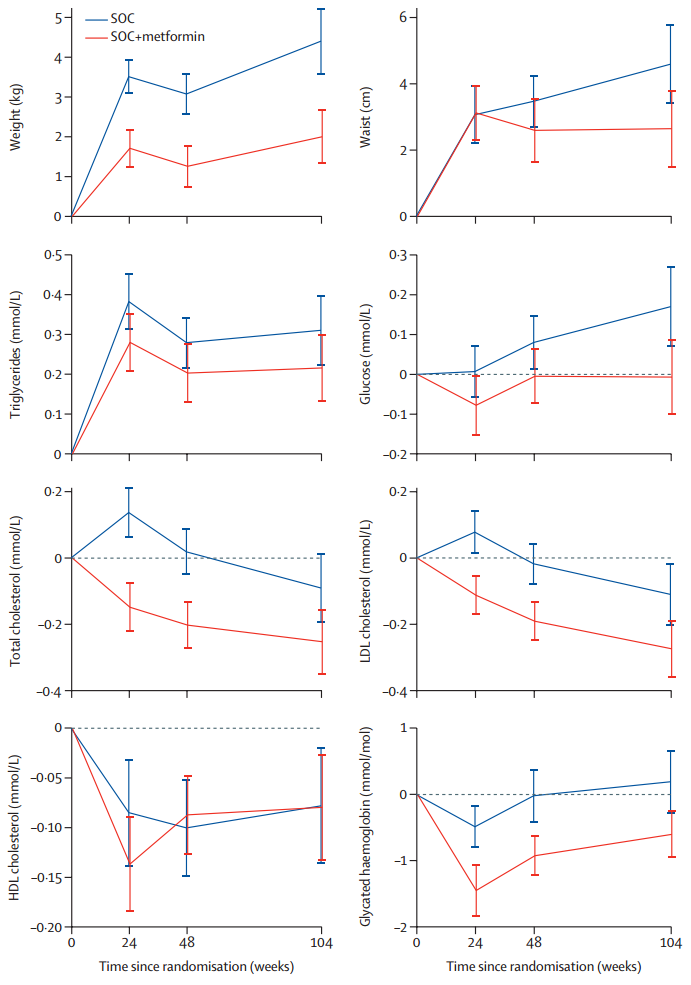
图3 与基线时相比,治疗后的形态学和代谢学改变
安全性
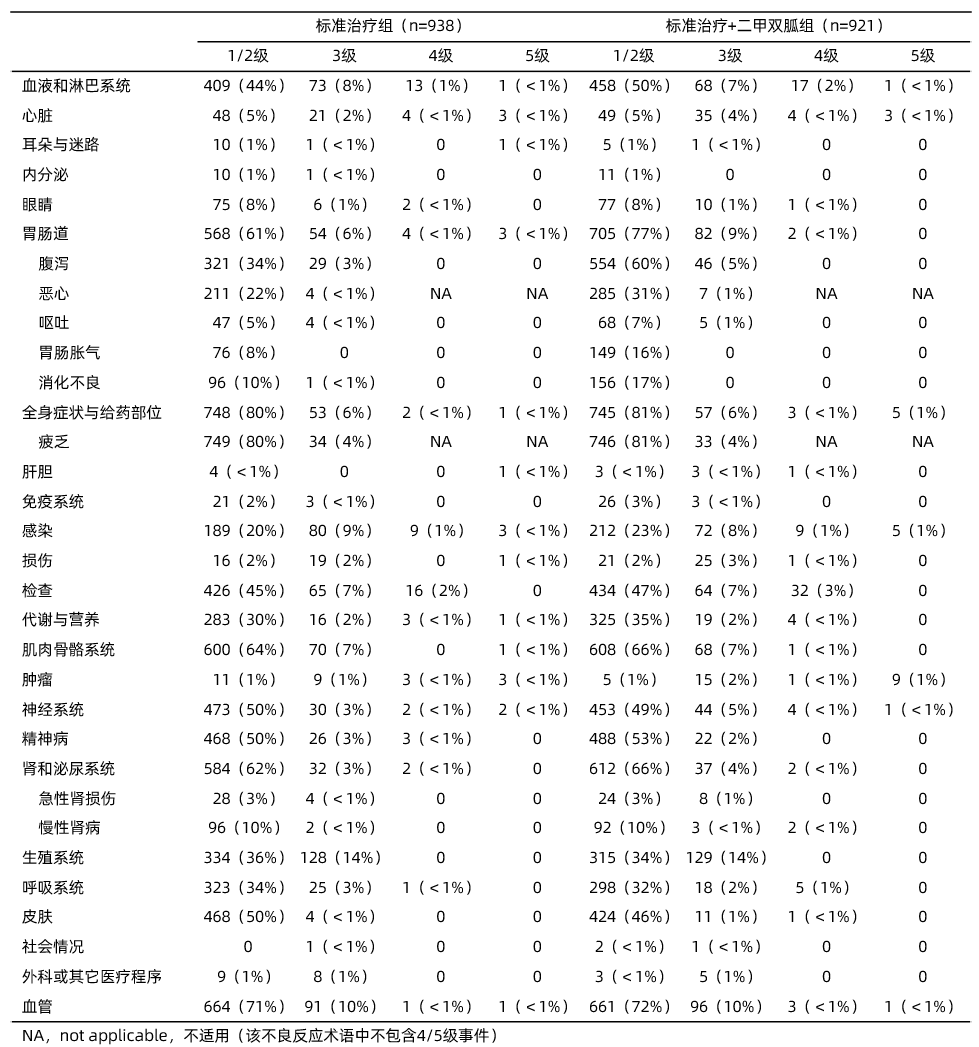
随访期间,两组患者不良事件通用术语评价标准(Common Terminology Criteria for Adverse Event,CTCAE)1-5级不良事件发生率总体相似。标准治疗组938例患者中的487例(52%)和标准治疗+二甲双胍组921例患者中的523例(57%)发生了≥3级不良事件。两组患者胃肠道及肾脏/泌尿系统不良事件发生率存在差异(详见表2)。与标准治疗组相比,标准治疗+二甲双胍组胃肠道不良事件发生率更高,分别为86%和67%;主要表现为
共发生286例严重不良事件,主要与标准治疗中的多西他赛相关。二甲双胍的14例严重不良事件中9例累及胃肠道系统。两组各1例激素治疗相关死亡(
表2 安全性分析人群的不良事件发生情况
总体而言,本研究未能证实在mHSPC总体人群中,二甲双胍联合标准治疗方案可以带来具有统计学意义的生存获益。二甲双胍的安全性特征符合预期,主要表现为腹泻。与标准治疗相比,联合二甲双胍可以显著降低ADT治疗所致的代谢不良反应。
本项研究虽然未显示二甲双胍联合应用其他已知药物在前列腺癌治疗中能够显著改善生存获益,但为临床治疗策略提供了新的思考方向。它提示我们,在晚期前列腺癌的治疗探索中,除了不断研发的新型药物(包括靶向治疗、免疫治疗及核素治疗等),对于一些在其他疾病领域已被广泛应用的成熟药物,将其与前列腺癌现有治疗方案联合使用,亦可能发挥一定作用。此类联合治疗的价值可能并非主要体现在延长患者生存,而更多在于改善患者生活质量、降低不良反应发生率及优化代谢水平等方面,从而拓展现有治疗策略的临床价值。
在前列腺癌的标准治疗体系中,ADT仍然是最基础且最关键的治疗模式,临床最常应用的药物为促性腺激素释放激素激动剂(gonadotropin-releasing hormone agonist,GnRH-a)。随着药物制剂技术的不断发展,GnRH-a已由传统剂型逐步发展至缓释及长效制剂。其中,以
与此同时,来自欧洲的一项对GnRH-a注射频率、满意度、医疗资源利用率和治疗决策参与度的偏好调查研究也表明,在414例接受GnRH-a治疗的前列腺癌患者中,53.9%倾向于选择6个月注射方案,其中77.0%的患者对该方案表示满意。该研究进一步指出,给药的便利性与规律性是推动患者偏好6个月注射频率的关键因素[3]。
GnRH-a 6月长效剂型不仅契合前列腺癌长期管理的临床需求,也为患者带来了依从性与生活质量的双重改善,在ADT治疗体系中具有重要的临床应用与推广价值。随着GnRH-a 6月长效剂型在前列腺癌临床实践中的应用愈发广泛,它的治疗潜力将得到进一步释放。
成晟 教授
浙江大学医学院附属邵逸夫医院
浙江大学医学院附属邵逸夫医院 泌尿外科 主任医师 硕士生导师
德国莱比锡大学医学博士
亚洲男科协会前列腺健康与咨询委员会委员
中国医促会泌尿健康分会加速康复学部委员
浙江省医师协会泌尿外科医师分会委员
浙江省数理医学学会泌尿肿瘤专委会委员
浙江省医学会泌尿外科分会微创学组委员
浙江省中西医结合男科分会前列腺学组委员兼秘书
浙江省医师协会泌尿生殖肿瘤加速康复学组委员
欧洲泌尿外科学会海外会员
德国莱比锡大学医学中心泌尿外科Fellow医生
美国辛辛那提大学医学中心高级访问学者
达芬奇机器人手术主刀医生
邵逸夫医院泌尿外科加速康复外科(ERAS)负责人
参考文献
1. Gillessen S, et al. Lancet Oncol. 2025 Jul 7:S1470-2045(25)00231-1.
2. Klotz L, et al. BJUI Compass. 2024 Jan 10;5(3)392-402
3. Kaltenbach E, et al. Adv Ther. 2025 May;42(5):2314-2334.
编辑:Vily
审校:Rudolf
执行:Lya
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
DIP_PC-CN-000402
DIP_PC-CN-000403

扫码进入“菲长视野”专区
查看更多前列腺癌前沿资讯

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)