作者:
作者单位:南京大学医学院附属金陵医院呼吸与危重症医学科
引用本文: 施毅. 侵袭性
摘要
侵袭性真菌病(invasive fungal disease,IFD)在免疫功能受损人群中更为常见,但近年来高发的
一、IFD危险因素的定义
宿主因素是指宿主自身所具有的、能够影响真菌感染易感性、感染进程以及预后的内在生理、病理或免疫相关特征,是宿主自身的“内在条件”,它们决定了宿主对真菌的“抵抗力
危险因素是指能够增加个体或群体发生真菌感染的概率或导致感染后病情加重、影响预后的各种因素,它们既可以来自宿主自身(内在因素),也可以来自外部环境或医疗干预(外在因素),其核心作用是降低宿主对真菌的抵抗力,增加真菌感染的机会。高危因素是指危险因素中对真菌感染发生具有“显著影响”的因素,可导致感染的概率大幅升高,更易发展为重症感染,增加病死率,是危险因素中的“重点”,也是临床判断感染风险等级(如高危人群)的核心依据。
宿主因素与危险因素之间有一定程度的交叉和重叠,在临床上也常常被混用,其主要区别在于宿主因素是危险因素的重要组成部分,而危险因素的范围更广泛。例如,
高危人群是指因存在一种或多种真菌感染高危因素,导致其发生真菌感染的概率显著高于普通人群,更易出现侵袭性、重症或难治性真菌感染的群体。其核心是“因高危因素导致感染风险和不良结局风险显著升高的群体”,识别这一群体是临床预防和控制真菌感染的关键环节。厘清这些概念将有助于及时正确地发现及诊断IFD,尤其在临床表现和实验室检查不典型的非粒缺患者。
二、IFD的危险因素与变迁
2. 危险因素的变迁:随着社会老龄化、免疫抑制人群增多,越来越多的循证医学证据表明,多样化非粒缺的基础疾病与日益进展的新型诊治技术应用同样是IPA的重要危险因素,特别是慢阻肺病[5]、重症病毒性肺炎(流感和新冠)[6, 7, 8]、糖尿病[9]等本身就是罹患IPA的独立危险因素。而不同真菌导致IFD的危险因素亦存在明显差异,如
慢阻肺病伴IPA的危险因素可分为两类[11]:(1)疾病本身相关因素:肺功能差、过去3个月内发生重度急性加重;(2)治疗相关因素:
对于IC,危险因素包括应用广谱抗菌药物、糖皮质激素和其他免疫调节药物,
3. 危险因素的分级:随着日益增多的IFD人群,人们逐渐认识到,根据对宿主免疫功能和真菌易感性的影响程度,危险因素可以分为高、中、低3个风险等级[12,15, 16]。血液系统疾病患者罹患IFD的危险因素多为高风险(高危因素,或为高危人群),它们易于判定,诊断提示价值高。非粒缺患者中虽然也可以见到IFD的高危因素(如艾滋病患者CD4⁺T淋巴细胞计数<200/μl,长期使用大剂量糖皮质激素,未控制的严重糖尿病,严重大面积
以慢阻肺病合并IPA为例,单纯慢阻肺病(GOLD分级Ⅱ~Ⅳ级)患者伴发IA的发病率是1.3%~3.9%,但入住 ICU 的重症慢阻肺病合并IPA的几率高达23.6%;如果伴有气道曲霉定植GLOD分级为Ⅳ级的慢阻肺病患者,罹患IPA的发病率升至33.0%,伴有曲霉定植并接受
近年来,新的指南对不同真菌感染分别给出了相应的危险因素判定。2025年“侵袭性肺真菌病诊断路径中国专家共识”分别对不同的肺真菌病(IPA、肺隐球菌病、
三、危险因素差异的可能机制
粒缺与非粒缺患者罹患IFD危险因素之间的差异与两者间免疫功能状态被影响的程度密切相关。粒缺属于典型的急性重度免疫缺陷,容易罹患IFD且病情危重,通常易于识别;但非粒缺患者的基础疾病多样,免疫受损程度差异极大,可以从基本正常(见于单纯肺隐球菌病患者)到严重缺陷(类似于严重粒缺),尤其轻到中度免疫受损的范围极广、变异度大,从而导致它们在危险因素、临床特征和实验室检查、罹患IFD的病种之间存在明显差异[15,21](图1),就需要更为细致、综合评估的思维方式。
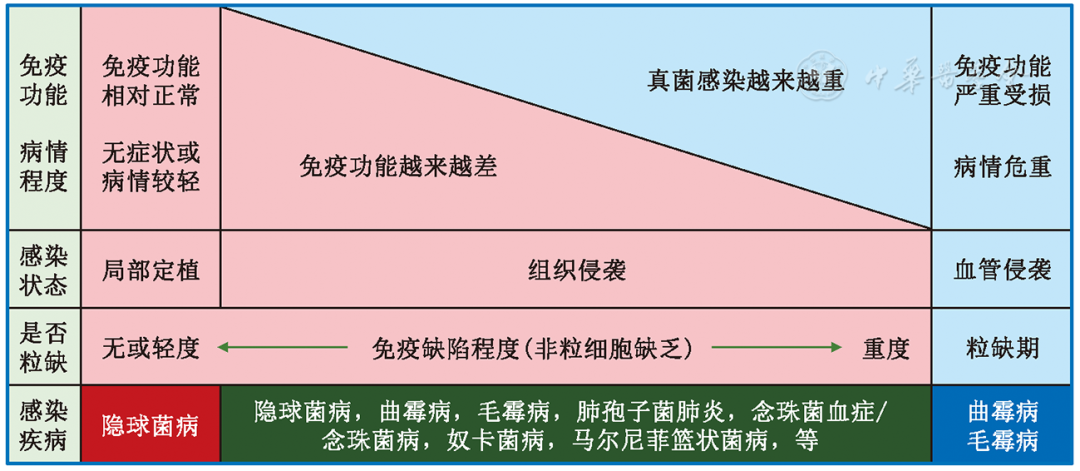
图1 免疫功能状态(粒缺与非粒缺)对侵袭性真菌病(IFD)病种、病情严重程度、感染状态的影响
最典型的是曲霉病,根据免疫受损的程度不同,可以表现为:(1)急性IA:包括IPA、肺外曲霉病,见于重度免疫抑制患者(尤其是粒缺患者);(2)
四、危险因素变迁对诊断标准的影响
2002年,Carcia-Vidal等[22]提出了IFD的诊断框架,将诊断分为3级:确诊(Proven,危险因素+临床特征+微生物学+组织病理学)、临床诊断(Probable,危险因素+临床特征+微生物学)和拟诊(Possible,危险因素+临床特征)。2008年欧洲癌症研究和治疗组织/侵袭性真菌感染协作组(EORTC/MSG)建立了侵袭性真菌感染疾病定义[23],诊断标准中都包含有危险因素这一要素。
近年来,血液病IFD诊治指南对粒缺高危患者不满足于“拟诊”,担心遗漏,提出了“未确定”的诊断标准,意在早期发现早期治疗;而重症学会IFD诊治指南对非粒缺患者则建议取消“拟诊”,因为难以区别定植与感染,以防止过度经验性治疗(主要是IC)。此外,对非粒缺患者罹患IFD开始提出不同的基础疾病(如慢阻肺病,ICU重症患者等)合并IFD应有各自的诊断标准;同样,不同的真菌感染(如曲霉,肺孢子菌等)也应有自己相应的诊断标准。新发布的指南与专家共识,既有以疾病为基础合并IFD的指南,也有以致病真菌为基础的指南,给临床提供了极大地帮助与指导。在涉及危险因素时,给出的范围更广泛,并呈现出明显的差异化。例如,符合确诊标准的IFD(活检组织真菌病理学阳性,或无菌部位标本真菌培养阳性),则不论其免疫功能状态如何、有无宿主危险因素[24]。符合临床诊断标准的IPA,只要BALF曲霉培养阳性,结合显微镜检发现分叉的菌丝,也不需要具备宿主危险因素[1,25]。综合而论,对IFD危险因素的评估,特别在非粒缺患者,尤其是只存在中低危险因素时,应该结合临床进行综合判定和评估。
总之,面对IFD,尤其是非粒缺患者,临床医师应提高警惕,既要关注罹患IFD的共有危险因素,更要熟悉不同基础疾病罹患IFD的危险因素和不同真菌感染的特殊危险因素。只有综合分析、系统评价才能做出正确的判断,从而提高对IFD的诊断水平[15]。
参考文献(略)
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)