
Toll 样受体(TLRs)作为先天免疫系统中的关键模式识别受体,在神经病理性疼痛的发生与发展中发挥关键作用。近年研究发现微小RNA(miRNAs)作为重要的基因表达调控分子,可通过多重机制调控TLR信号通路:既可作为内源性配体直接激活TLR7/8等受体,也可通过靶向 TLRs 及其下游信号分子进行负向调控,形成复杂的miRNA-TLR调控网络。本文系统综述了不同TLR亚型在神经损伤中的特异性作用,重点探讨了miR-21-TLR8、miR-146a-TLR4等关键调控轴在介导神经炎症和疼痛敏化的分子机制。尽管研究已证实靶向特定 miRNA-TLR 轴可有效缓解神经病理性疼痛,但其细胞特异性调控机制、胞外 miRNA 的递送路径及疾病亚型特异性网络等关键问题仍需深入解析。未来研究应整合多组学技术与精准递送策略,推动该调控网络从机制研究向临床治疗的转化,为神经病理性疼痛的精准干预提供新思路。
关键词:微小RNA;Toll样受体;神经病理性疼痛
神经病理性疼痛(NP)是一种由躯体感觉神经系统损伤或疾病所引起的慢性疼痛综合征,临床主要表现为自发性疼痛、痛觉过敏和触诱发痛。流行病学调查显示,全球7%~10%的人口受 NP的困扰,其病程迁延、治疗反应差,严重影响病人生活质量并带来沉重社会经济负担。目前临床常用的治疗手段包括阿片类药物和抗抑郁药物等,但仍面临疗效有限、药物依赖风险高及不良反应显著等诸多问题,迫切需要开发新治疗策略。
近年来的研究发现神经炎症反应在NP发病机制中扮演核心角色。在生理条件下,中枢神经系统稳态免疫调控主要由小胶质细胞和星形胶质细胞承担,它们参与维持神经内环境的稳定。病理状态下,这两种胶质细胞异常激活,活化的胶质细胞释放大量促炎细胞因子,包括白细胞介素-1β(IL-1β)、肿瘤坏死因子-α(TNF-α)、白细胞介素-6 (IL-6) 等,持续放大疼痛信号传递。在此过程中,Toll 样受体(TLRs) 作为先天免疫系统中的关键模式识别受体,在启动并放大神经炎症反应中扮演重要角色,已成为疼痛调控研究的热点靶标。
miRNAs 是一类长度约22个核苷酸的非编码RNA分子,可通过特异性结合靶基因3'非翻译区(3'-UTR),在转录后对基因表达进行调控。越来越多的证据表明,在NP研究领域miRNAs可通过靶向离子通道、神经递质受体及炎症信号分子,动态调控疼痛进程。例如,miR-155 可通过增强TLR4信号通路活性,加剧坐骨神经结扎模型中的痛觉超敏;而miR-146a则通过抑制白细胞介素-1受体相关激酶(IRAK1)和肿瘤坏死因子受体相关因子6 (TRAF6)的表达,对TLR4通路起到负向调控作用。这些发现不仅揭示了miRNA-TLRs交互网络在NP中的关键调控功能,也为开发新型镇痛策略提供了潜在分子靶点。
尽管已有不少研究进展,但miRNA如何调控TLR信号通路从而影响特定类型的NP,其具体机制仍缺乏系统性的梳理与阐释。目前,不同 TLR 亚型在各类NP模型中的作用尚未得到充分的横向比较与整合;miRNA-TLR调控轴在不同细胞中的功能特异性及其相互协作的机制仍不清晰;此外,胞外miRNA作为TLR配体,其递送途径、识别机制以及在疼痛慢性化过程中的动态变化,也有待更深入的解析。
基于此,本文系统梳理了不同TLR亚型在NP中的角色,重点探讨miRNA通过充当内源性配体直接激活TLR,或通过靶向TLR及其下游信号分子实施负向调节,进而精细调控TLR信号通路的多种机制。同时本文归纳了(如miR-21-TLR8、miR-146a-TLR4等)关键调控轴在疼痛发生与发展中的作用。期望通过对现有证据的整合与分析,揭示miRNA-TLR网络在NP中的多层次调控规律,为后续机制探索及靶向治疗策略的研发提供理论参考与思路启示。
TLRs家族是先天免疫系统中一类高度保守的模式识别受体,在哺乳动物中目前已鉴定出13种亚型。这些亚型在不同物种间存在表达差异,人类表达 TLR1至TLR10共10种亚型,小鼠则表达TLR1至TLR9以及TLR11至TLR13共12种亚型。这类受体不仅广泛分布于小胶质细胞、巨噬细胞和树突状细胞等经典免疫细胞中,也在神经元中表达,构成了免疫系统与神经系统之间重要的沟通桥梁。
从分子结构特征分析,TLRs属于一类跨膜蛋白,其胞外结构域由多个富含亮氨酸的重复序列构成独特的马蹄形空间构象,这种结构使其能够高效识别多种病原体相关分子模式。胞内结构域则包含高度保守的Toll白细胞介素-1受体结构域(TIR结构域),该结构域负责启动下游信号转导过程。根据亚细胞定位与功能特点,TLRs 可分为两大类:位于细胞质膜的TLR1、TLR2、TLR4、TLR5、TLR6和TLR10主要识别细胞外病原体成分,如脂多糖、脂蛋白和鞭毛蛋白等,是宿主抵御外界感染的第一道防线;而定位于内体、溶酶体等细胞内膜结构的TLR3、TLR7、TLR8和TLR9则主要识别病毒核酸等胞内病原体成分。
在信号转导机制方面,TLRs主要通过两条经典通路发挥作用。除TLR3外,绝大多数TLR,包括TLR1/2、TLR4、TLR5、TLR6、TLR7、TLR8、TLR9均可激活髓样分化因子88 (MyD88),通过核因子κB (NF-κB)和丝裂原活化蛋白激酶(MAPK) 促进促炎细胞因子的产生;TLR3和 TLR4激活TIR结构域衔接蛋白诱导干扰素β(TRIF),通过干扰素调节因子3 (IRF3)诱导I型干扰素的产生。这些信号通路在神经炎症与痛觉敏化过程中扮演双重角色,一方面参与正常的免疫防御,另一方面在病理状态下可能导致过度炎症及神经元超兴奋。
在 NP 的发生与慢性化进程中,TLRs 家族作为先天免疫系统的关键模式识别受体,通过识别内源性损伤相关分子模式,在介导神经炎症与中枢敏化中发挥核心作用。不同 TLR 亚型在疼痛调控中具有独特的表达、机制与功能,其作用已在多种经典疼痛模型中得到验证。
TLR2在坐骨神经慢性压迫损伤和痛性糖尿病周围神经病变模型中扮演重要角色。它在脊髓小胶质细胞、星形胶质细胞、背根神经节(DRG)神经元及施万细胞中广泛表达,能够识别高迁移率族蛋白B1(HMGB1)、热休克蛋白等内源性信号。TLR2 的激活主要通过MyD88/NF-κB信号通路,驱动TNF-α、IL-1β等促炎细胞因子的释放,从而放大局部神经炎症并加剧疼痛行为。
TLR3主要参与由神经损伤或慢性疼痛状态触发的病理过程,并与疼痛相关的认知功能障碍密切相关。在脊髓小胶质细胞及海马等脑区神经元中,内源性双链RNA (dsRNA)可激活TLR3,通过其特有的TRIF依赖性信号通路,不仅诱导促炎细胞因子的产生,还能激活半胱天冬酶介导的细胞凋亡通路,从而同时参与神经炎症的维持与神经元损伤。研究证实,通过鞘内注射TLR3抑制剂,既可以单独产生镇痛作用,也能与吗啡协同,显著增强其镇痛效能。
TLR4 是疼痛研究中最为深入的TLR亚型,在坐骨神经结扎等模型及复杂性区域疼痛综合征病人中均被证实具有关键作用。其在脊髓背角小胶质细胞中表达显著上调。HMGB1是其主要配体之一,TLR4被激活后通过经典的MyD88/NF-κB通路,促进IL-1β、环氧化酶-2等炎症介质的表达,直接增强神经元兴奋性,是疼痛信号传递的重要放大器。
TLR7的活化在周围神经损伤诱发的疼痛中至关重要。其表达主要富集于DRG中瞬时受体电位香草酸亚型1(TRPV1)阳性的伤害性感受神经元,并受转录因子CCAAT增强子结合蛋白β的调控。胞外miRNA(如let-7b)作为内源性配体被TLR7识别,通过MyD88通路激活NF-κB与IRF7,诱导炎症因子与I型干扰素表达,并与神经元上的瞬时受体电位锚蛋白亚型1(TRPA1)离子通道协同,直接介导快速的伤害性反应。
TLR8同样在脊神经结扎等NP模型中发挥重要作用,在DRG神经元和脊髓小胶质细胞中表达上调。它能够特异性识别dsRNA 及miR-21等miRNA。激活后的TLR8通过触发细胞外信号调节激酶(ERK)等信号通路,促进促炎细胞因子的释放,并直接增强DRG神经元的兴奋性,从而维持机械性异常性疼痛。
TLR9在化疗药物(如紫杉醇)诱导的周围神经病变模型中具有特殊地位。该受体主要表达于脊髓胶质细胞,能够识别由受损细胞释放的线粒体DNA等内源性核酸。TLR9的激活可驱动脊髓胶质细胞向促炎表型转化,维持慢性炎症状态,从而促进疼痛的持续与慢性化。
通常情况下,miRNA在转录后水平调控基因表达,其在细胞核内经德罗沙核糖核酸酶III初步剪切形成前体,再经胞质中核糖核酸酶III最终加工为成熟miRNA。成熟的miRNA随后被装载至RNA诱导沉默复合体中,通过其“种子序列”与靶基因mRNA的 3'-UTR 特异性结合,从而在转录后水平诱导mRNA降解或翻译抑制,实现对基因表达的精细调控。在免疫调控领域,miRNA因其能够同时调控多个靶基因,成为TLRs信号通路的重要调节因子。研究表明,单个miRNA(如miR-155 或miR-146a)可靶向TLR信号通路中的多个组分,包括TLR4、NF-κB 和热蛋白结构域相关蛋白3,形成精细的调控网络。miRNA的这种多靶点特性,使其能够对TLR介导的炎症反应实现精细调控,从而在维持免疫稳态与调控神经炎症性疼痛中发挥核心作用(见图1)。
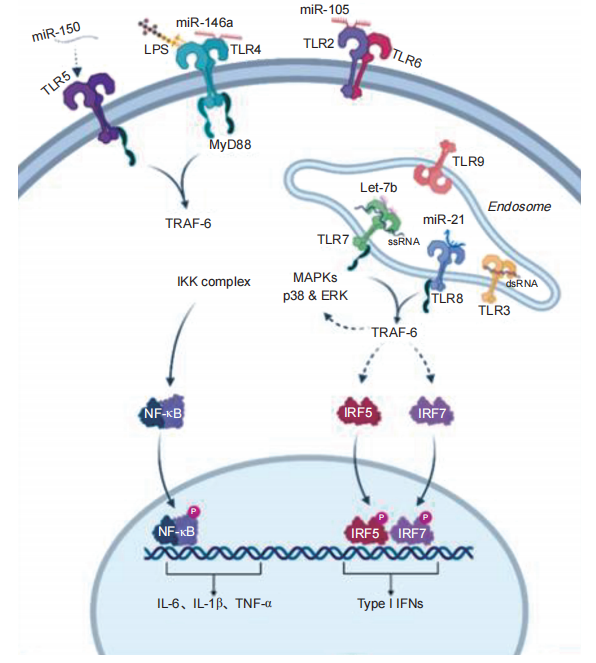
图 1 Toll 样受体信号通路及其 miRNA 调控示意图
不同细胞定位的 TLRs 在识别相应配体后的信号转导过程,包括 MyD88 依赖与 TRIF 依赖通路如何激活 NF-κB、IRF 等转录因子,进而诱导促炎细胞因子与 I 型干扰素表达。miR-21、let-7b、miR-146a 等代表性 miRNA通过直接作为配体激活 TLR7、TLR8,或通过靶向 TLRs、衔接蛋白、激酶及转录因子等关键节点,实现对 TLR 信号的正向或负向调控,从而参与神经免疫调节与疼痛敏化过程。
IL-6:白细胞介素-6;IL-1β:白细胞介素-1β;TNF-α:肿瘤坏死因子-α; MAPK:丝裂原活化蛋白激酶;Type I IFN:I 型干扰素;TRAF-6:TNF受体相关因子 6;IKK complex:调控 NF-κB 信号通路的激酶复合体;Endosome:内体
1. 细胞外miRNA作为内源性配体激活TLR信号通路
当细胞发生坏死、凋亡或主动分泌时,其内部的miRNA可被释放到细胞外间隙或循环系统中。这些胞外 miRNA 随后能够被邻近或远端的免疫细胞摄取,主要包括树突状细胞、巨噬细胞和浆细胞样树突状细胞等。经内吞作用进入细胞后,miRNA被转运至酸性内体区室,并可被定位于此的特定TLR识别与结合,从而启动下游炎症信号传导。
在这一机制中,miRNA主要作为激动型配体发挥作用。TLR7与TLR8是识别单链RNA的关键受体。胞外miRNA被免疫细胞内吞后,富含鸟苷与尿苷的特定序列及二级结构在酸性内体中可直接与TLR7或TLR8结合。此类结合引发受体活化,通过其胞内TIR结构域募集衔接蛋白MyD88,启动下游信号级联,最终激活转录因子NF-κB与IRF7,促进TNF-α、IL-6、IL-12以及I型干扰素等促炎细胞因子的大量产生。这一机制在自身免疫性疾病中具有关键作用,来自死亡细胞的特定miRNA分子,如miR-21和miR-29可作为自身抗原被TLR7、TLR8识别,持续驱动病理性I型干扰素的产生。在神经系统中,miR-155、miR-21 等高表达的 miRNA,也通过此途径激活小胶质细胞与星形胶质细胞,加剧神经炎症与中枢痛觉敏化。
除了TLR7、TLR8通路,同样定位于内体膜的TLR3专门识别dsRNA。某些miRNA能够形成发夹样结构,或者通过与互补分子暂时配对形成双链复合体,被TLR3识别。TLR3激活后,通过衔接蛋白TRIF传递信号,主要诱导转录因子IRF3的活化及IFN-β的产生,同时也激活NF-κB通路。研究表明,在肿瘤微环境或神经系统中,细胞释放的miRNA可被免疫细胞摄取,并通过激活TLR3信号通路参与调控相关的炎症与免疫进程。
部分miRNA也扮演着拮抗型配体的角色。这类miRNA虽能与TLR结合,却无法诱发有效的下游信号传导,而是通过竞争性占据配体结合域,阻止外源性或内源性危险信号对受体的激活。神经组织特异性表达的miR-124,能够作为TLR7的内源性竞争性拮抗剂,有效抑制其他miRNA介导的小胶质细胞活化,形成一种关键的负反馈调节通路,在限制炎症过度扩散和维持神经稳态中发挥重要作用。
2. miRNA直接调控TLRs表达
TLR信号通路的精密有序激活是先天免疫应答的核心,其一旦失调将成为驱动神经炎症与疼痛的关键机制。在这一过程中,miRNA作为关键的转录后调节因子,能够对TLR通路的几乎所有核心节点进行精准抑制,从而实现对炎症反应的精细调控。TLR信号传导主要依赖MyD88依赖通路和TRIF依赖通路两大分支,二者在中枢神经系统中均有广泛表达。TLR信号通路的各个环节均受到miRNA的严密调控。从信号起始、中游转导直至下游转录与效应输出,miRNA通过靶向不同节点实施多层次、网络化的调控。
在信号起始阶段,TLR信号通路中连接受体与下游激酶的接头蛋白,成为miRNA频繁作用的靶点。miR-146a、miR-21等可直接靶向抑制MyD88的表达,从而在源头阻断MyD88依赖通路的信号传递;类似地,miR-125b通过靶向含Toll白细胞介素1受体域衔接蛋白(TIRAP),部分miRNA则调控TRIF,实现对不同TLR信号分支的特异性干预。
信号传导进入中游阶段,涉及一系列激酶与泛素化分子的活化与信号放大。其中,IRAK1家族成员以及TRAF6是此环节的核心枢纽。miR-146a作为该通路的经典负反馈调节因子,能够同时靶向IRAK1和TRAF6,有效遏制信号的级联放大。此外,miR-181c等miRNA可通过靶向TGF-β活化激酶1等位于TRAF6下游的关键信号激酶 , 抑制NF-κB等转录因子的活化,从而在信号传导的中游层面实施调控。
信号通路最终的调控落点在于转录因子,其活性直接决定促炎基因的转录水平,这一环节同样处于miRNA的调控网络中。在中枢炎症中,NF-κB是关键调控靶点,miR-21、miR-146a等可通过直接或间接途径抑制其活化及向细胞核内转移。同时,MAPK家族成员以及IRF3 等转录因子也受到miR-124、miR-181a等多种miRNA的调控,从而影响痛觉敏化及干扰素应答等相关基因的表达。
在TLR通路的最终效应输出层面,炎症介质的释放也直接受到miRNA的调控。多种 miRNA能够直接靶向促炎细胞因子、趋化因子及相关酶的mRNA,在翻译水平上实施最后一道调控。例如,miR-146a可抑制TNF-α和IL-1β,miR-29靶向诱导型一氧化氮合酶(iNOS),而miR-181b则能调控趋化因子CXCL10的表达,从而在多层面影响神经炎症的进程与结局。除了广泛调控下游信号分子外,miRNA还在TLR通路源头发挥关键作用,即直接调控TLR受体本身的表达。在先天性免疫应答中,TLR的表达受到转录后水平的精细调控,其中 miRNA 扮演核心角色。miRNA 通过其5'端2~8个核苷酸构成的“种子序列”与靶基因mRNA的3'-UTR特异性结合,进而通过翻译抑制或促进mRNA降解来实现调控。
在众多TLR中,TLR4作为识别脂多糖(LPS)的关键受体,其表达受到多种miRNA的严格调控。let-7家族成员let-7i可通过特异性结合TLR4 mRNA的3'-UTR,显著抑制其翻译过程。此外,M2型巨噬细胞标志基因编码的miR-511也能直接抑制TLR4翻译,形成细胞表型自我限制的调控回路;miR-143同样也可直接靶向TLR4,其下调与某些感染模型中炎症反应的增强相关。TLR2的表达同样受到特定miRNA的直接调控。miR-105能特异性抑制TLR2表达,在维持肠道黏膜免疫耐受中发挥重要作用;miR-19a/b在血管内皮细胞中可被炎症因子下调,使其对TLR2的抑制作用减弱,进而参与血管炎症的发生发展;此外,miR-221和miR-222可协同抑制TLR2和TLR4的表达,构成一个整合性的调控枢纽。然而,它们在NP模型中的表达、功能及特异性作用部位仍有待未来研究阐明。
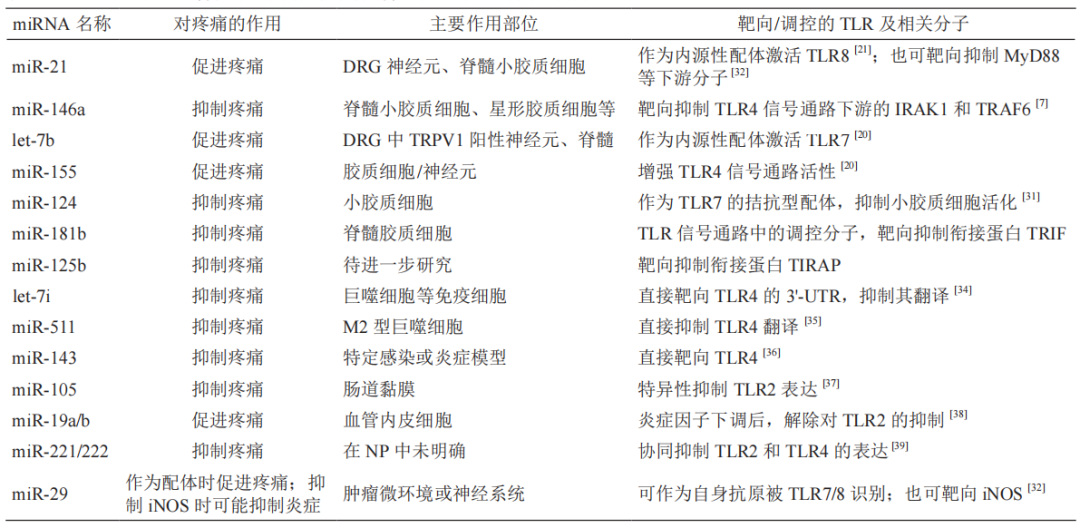
综上所述,多种miRNA通过靶向或直接充当内源性配体等方式,对TLR信号通路进行多层次调控,在NP的发生与维持中发挥关键的促进或抑制作用。为清晰呈现主要miRNA的调控关系、疼痛效应及作用部位,其具体信息归纳见表1。
表1 miRNA对Toll样受体的调控及其在神经病理性疼痛中的作用
本文系统综述了miRNA通过调控TLRs信号通路在NP中的核心作用。大量证据表明,特定的miRNA或作为TLRs(特别是TLR7、TLR8)的内源性配体直接激活免疫信号,或通过靶向TLRs及其下游信号分子进行精细的负向调控,构成了一个复杂的调控网络。这一网络在神经损伤后被显著扰动,通过驱动持续的神经炎症和神经元兴奋性,主导了NP的发生与慢性化进程。靶向特定的miRNA-TLR调控轴,为开发新型、精准的镇痛策略提供了重要的分子基础与干预方向。
尽管该领域已取得显著进展,仍存在若干需要解决的问题。首先,目前研究普遍关注miRNA对TLRs的整体调控作用,但对其在不同细胞类型中的功能特异性认识尚不充分。miR-146a虽可抑制TLR4信号,但其在神经元与星形胶质细胞中的调控效率及靶向偏好可能存在差异,这种差异是否由细胞特异的转录调控或RNA结合蛋白所介导,仍需深入探索。其次,miRNA作为TLRs内源性配体的作用,依赖于其完整的胞外递送与细胞内激活通路,而目前对这一过程的机制理解仍不完善。例如,损伤神经元释放的let-7b如何被小胶质细胞选择性摄取?是否存在特异性受体介导此过程?miRNA从胞质向内体的转运机制亦不明确。这些关键环节的缺失,限制了对miRNA-TLR激活机制的深入理解。
基于现有研究成果与存在的问题,未来应致力于系统解析miRNA对TLRs信号通路的调控网络,例如:①通过单细胞转录组测序、miRNA高通量测序等技术,筛选在慢性疼痛不同阶段和不同细胞类型中差异表达的miRNA及其调控的TLRs家族成员。在神经损伤、痛性糖尿病周围神经病变等疼痛模型中,鉴定可能参与TLRs信号调控的新miRNA分子,并在相应动物模型上进行功能验证,从而拓展对miRNA-TLR调控网络的认识,挖掘潜在的疼痛治疗新靶点。②利用细胞特异性基因操作技术,结合代谢组学、分子生物学等技术方法,明确特定miRNA-TLR轴在不同细胞类型中的调控差异及其下游信号通路。比较同一 miRNA对不同TLR亚型或同一TLR受不同miRNA调控的特异性机制,揭示细胞类型特异性的调控网络及其在疼痛维持中的功能异质性。
在深入探索其基础机制的同时,将相关研究成果向临床转化也是关键方向。未来研究应重点评估靶向该调控网络的精准治疗潜力与策略:一方面,可探索基于寡核苷酸,如miRNA模拟物、抑制剂或反义寡核苷酸或新型纳米载体的靶向递送体系,以实现特定miRNA在病变细胞或局部区域的特异性调控;另一方面,可结合病人临床分型与生物标志物,发展个体化干预方案,从而推动该基础研究向临床镇痛新策略的实质转化,最终为NP病人提供更安全、有效的治疗选择。
综上所述,深入解析miRNA对TLRs信号通路的精细调控网络,不仅能够揭示其在神经免疫稳态维持与失衡中的核心作用,还将为阐明NP的分子机制及开发靶向干预策略提供全新视角,也为个体化镇痛治疗开辟新的途径。
信源:黄梦璇,卢焕俊,高永静. miRNA调控Toll样受体信号通路在神经病理性疼痛中的作用[J].中国疼痛医学杂志,2026,32(4):254~260
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。