

1
肝豆状核变性又称威尔逊病(WD),是一种可治疗的常
在WD患者及多种动物模型的研究中发现,铜代谢障碍会引发系统性的脂代谢异常,其脂代谢紊乱被认为是WD临床症状出现前的早期特征。动物模型研究为此提供了较为清晰的证据。例如,ATP7B基因敲除(Atp7b⁻/⁻)小鼠的血清脂质谱呈现显著异常,主要表现为总胆固醇(TC)和
相较于动物模型的低脂质水平,临床观察到WD患者的血清脂质水平呈现出一定的复杂性。Seessle等对251例WD患者进行横断面研究,结果显示未经治疗的患者血清TC和TG的中位数通常处于正常范围,仅在有肝脏症状的患者中TC水平显著降低。一项针对WD儿童的回顾性研究也发现类似结果,
临床观察显示,WD患者经过有效的驱铜治疗后,随着肝功能改善,其异常的脂质水平可趋于正常。因此,有观点认为WD的低胆固醇血症可能归因于
在WD患者中,肝脂肪变性是常见的病理学改变,但其发生机制更为复杂。Liggi等研究显示,在98例WD患者中,53.1%存在组织学证实的肝脂肪变,其中近30%达到中度至重度,且在儿童患者中更为普遍和严重。值得注意的是,该研究发现肝脏铜含量与脂肪变的严重程度并无显著统计学相关,提示肝铜蓄积本身可能不足以解释WD中的脂肪变性。
然而,也有研究主张肝铜蓄积是WD肝脂肪变性的核心驱动因素。Liggi等通过对比WD与非酒精性脂肪性肝炎患者发现,尽管WD患者的整体代谢指标(如体重指数、
综合来看,WD中的肝脂肪变性可能是一个多因素、异质性的病理过程,肝细胞内铜离子蓄积与传统代谢危险因素(如肥胖、胰岛素抵抗)存在密切联系。例如,在LEC大鼠模型中发现,模型动物同时表现出肝内脂质堆积和外周血清低脂血症,深入研究发现肝铜蓄积导致胆固醇代谢通路全面抑制,包括合成、酯化及向胆汁酸转化等关键步骤活性显著下降,进而引起脂代谢的差异性变化。基于此,在临床实践中,仅凭血清脂质水平或影像学发现的脂肪肝无法对其病因进行诊断或鉴别,WD和MAFLD的肝脂肪变性在组织学上可能难以区分。但Stättermayer等研究提示,MAFLD患者肝脏铜含量较低,且铜含量与脂肪变性程度呈负相关。因此,面对脂肪肝患者,尤其是在肥胖流行背景下,将肝脏铜含量与24 h

2WD脂代谢紊乱的分子机制
WD脂代谢紊乱的机制错综复杂,其本质是铜离子异常蓄积损伤关键代谢相关细胞器或信号通路等,进而导致细胞功能障碍。
铜毒性诱导的氧化应激直接损伤了负责脂质代谢的关键细胞器。首先,铜过载可能会通过以下机制损伤线粒体:(1)铜诱导的氧化应激会引起线粒体结构和功能异常;(2)铜的直接毒性以及对线粒体自噬的抑制可能进一步加重线粒体损伤;(3)氧化应激可能通过增加核呼吸因子核内含量、过氧化物酶体增殖物激活受体( PPAR)γ共激活因子-1α启动子区域高甲基化等方式,影响脂代谢基因表达。研究发现,WD动物模型中,在出现明显肝脂肪变性前,肝细胞线粒体已经发生结构异常(如嵴尖端囊性扩张),其氧化磷酸化能力,尤其是复合物Ⅳ活性显著下降,导致脂肪酸β氧化这一主要供能途径受阻,为脂质积累创造了条件。另一方面,Oe等研究证实,铜过载会诱发显著且持续的内质网应激,内质网作为胆固醇合成、TG组装及磷脂代谢的核心场所,持续的应激状态很可能严重扰乱肝细胞的脂质合成、修饰与转运流程等,从而参与异常脂代谢的形成。例如,Song等在水生动物中发现,铜通过诱导未折叠蛋白反应进而引起肝脂肪变性。此外,由内质网应激和未折叠蛋白反应诱导的肝脏胰岛素诱导基因耗竭,也在一定程度上促进了铜引起的肝脏固醇调节元件结合蛋白-1c激活,这为深入了解铜与内质网应激的相互作用提供了新视角。
铜蓄积系统性地抑制了维持肝脏脂质稳态的核受体信号调控网络,尤其是肝X受体(LXR)/类视黄醇X受体(RXR)的功能抑制尤为关键。研究发现,在WD模型中,RXR蛋白水平在胞质和核内均显著降低,导致LXR/RXR异源二聚体功能受损,加之内源性配体氧化甾醇水平下降,共同抑制了核受体活性,进而抑制下游脂代谢基因的转录,并削弱脂肪酸氧化。此外PPAR也属于核受体家族,包括PPARα、PPARβ和PPARγ 3种亚型。与RXR形成异二聚体,调控参与能量稳态、胰岛素敏感性、脂质代谢和维持代谢稳态的基因。Nagasaka等研究表明,在WD患者中,肝脏PPARγ的表达随肝损伤加重而升高,且与脂肪变性程度呈显著正相关,提示PPARγ可能在铜诱导的肝脂肪变性中起促进作用。与此同时,作为细胞能量感受器的腺苷一磷酸活化的蛋白质激酶(AMPK)被持续激活,这可能是由铜诱导的氧化应激所驱动。也有研究认为,肝脏铜含量增加可通过促进SCO1-LKB1-AMPK复合物的组装来激活AMPK。在Atp7b⁻/⁻小鼠模型中,AMPK的激活一方面抑制了肝脏脂质合成基因(如固醇调节元件结合蛋白-1c、乙酰辅酶A羧化酶1)的表达,另一方面也下调了糖异生基因(如磷酸烯醇式丙酮酸羧激酶1、
面对铜毒性与代谢压力,肝细胞启动相应的代偿性反应。Polishchuk等研究证实,ATP7B缺陷的肝细胞通过激活自噬(包括显著的线粒体自噬)来清除铜毒性损伤的细胞器,从而维持细胞存活。自噬在维持细胞内环境稳定的同时,也可能深度参与了脂质的周转与重编程。此外,表观遗传调控构成了另一层复杂的适应机制。研究表明,成人和青少年外周血DNA甲基化状态的改变与肝脂肪变性密切相关,提示其可能作为肝脏脂肪积累的潜在生物标志物。铜蓄积可能通过干扰
WD的代谢紊乱不局限于肝脏,近期研究表明,在肠道细胞层面,ATP7B功能失活通过多重机制加剧WD的全身性脂代谢紊乱。Fontes等研究表明,在WD中,ATP7B缺失导致肠上皮细胞内的铜分布异常,引发线粒体功能障碍与紧密连接破坏,可能通过影响肠道脂质处理与吸收参与全身脂代谢紊乱。Guttmann等利用基因编辑技术在人肠道Caco-2细胞中敲除ATP7B后引起细胞内铜蓄积,引发载脂蛋白表达谱重编程(如载脂蛋白A1/C3/E上调和载脂蛋白B48下调),直接损害
综上所述,肝脏铜积累时,可通过增加氧化应激或直接铜毒性,损伤脂质合成相关细胞器,包括引起线粒体功能障碍和内质网应激,影响脂肪酸氧化和脂质合成等。铜也可能进入细胞核,引起DNA甲基化改变、抑制LXR/RXR、调控PPAR家族及AMPK等,从而影响脂代谢基因表达。肝铜还可以激活自噬间接改变肝脏脂质状态。此外,肠道上皮铜离子的蓄积可能通过干扰乳糜微粒的组装进一步影响全身脂质代谢,最终引起
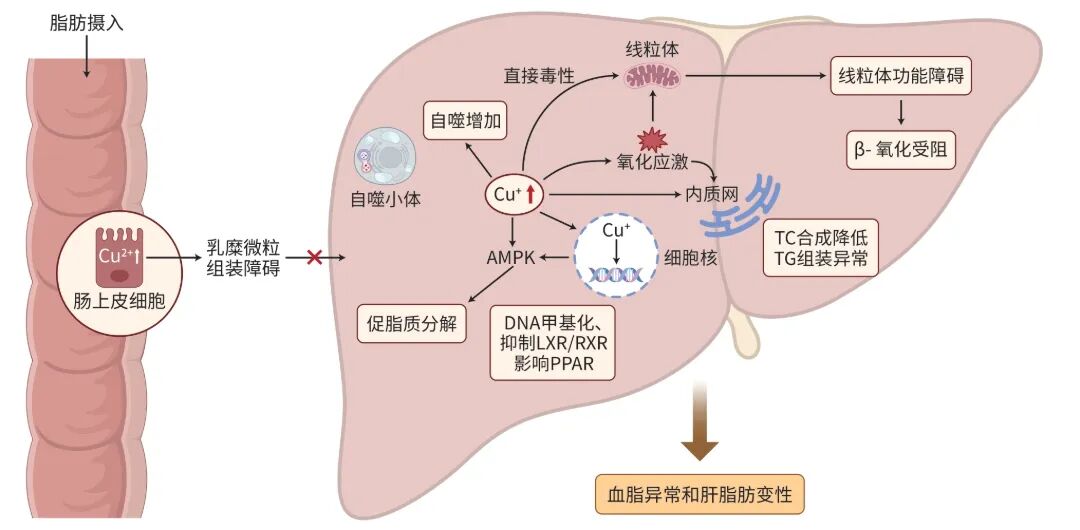
注: AMPK,腺苷一磷酸活化的蛋白质激酶;LXR,肝X受体;RXR,类视黄醇X受体;PPAR,过氧化物酶体增殖物激活受体;TC,总胆固醇;TG,甘油三酯。
图1 肝豆状核变性脂代谢紊乱的分子机制

3WD患者脂代谢紊乱的临床应用
基于WD与脂代谢紊乱之间的密切病理联系,近年研究开始探索脂质及其相关分子作为疾病诊断、分型及进展的新型生物标志物的潜力。首先,特定的脂质分子谱展现出卓越的诊断效能。如前所述,Zhi等研究发现,WD患者血清中多数饱和TG丰度增加,而Cer等其他不饱和脂质丰度降低。其中,TG(38∶0)和CerG1(d42∶2)诊断WD的受试者操作特征曲线下面积分别为0.948和0.915。Tang等通过一项靶向代谢组学研究,更系统地描述了WD患者的血清鞘脂谱,并发现5种鞘脂分子在区分WD患者与健康人群时表现出卓越的诊断性能,表明特定的鞘脂物种在WD的病理进程中发生了剧烈而特异性的改变,提示这些分子具有成为高特异性诊断生物标志物的潜力。Qiu等研究发现,辅酶Q8、磷脂酸(18∶1_18∶1)和磷脂酰胆碱(16∶1_18∶1)在区分肝型WD患者与肝硬化患者时的受试者操作特征曲线下面积分别为0.908、0.818和0.791,表明这些代谢物在临床实践中具有重要诊断价值。此外,该研究通过比较WD患者不同亚型发现,肝型与神经型WD患者的脂质谱存在显著差异:前者以多种TG水平显著升高为特征,而后者则以神经酰胺、磷脂酰乙醇胺等脂质变化更为明显,其中TG是区分两个亚型差异最显著的脂质亚类。上述结果提示,不同类型的患者在脂质代谢紊乱方面具有明显的亚型特征,可能与器官特异性损伤机制有关。
在疾病进展评估方面,血清标志物也显示出应用价值。例如,Bierła等发现,伴有肝纤维化的WD儿童其肝脏脂肪酸结合蛋白1水平显著升高,且与肝硬度及肝酶(丙氨酸氨基转移酶、天冬氨酸氨基转移酶)水平呈正相关,对肝纤维化具有良好的诊断效能,提示其具有作为无创肝纤维化标志物的潜力。该研究同时发现,所有WD儿童的血清TG水平均显著高于健康儿童,但已出现肝纤维化患者的TG水平却显著低于仅存在肝脂肪变性的患者,表明不同疾病阶段的脂代谢模式存在动态演变。
综上所述,从特异性脂质分子到脂代谢相关蛋白,脂代谢相关指标在WD中展现出多层次的应用潜力:既可作为高灵敏度的诊断辅助工具,也可作为区分临床亚型和评估肝纤维化等进展阶段的无创标志物。这些发现为WD的精准管理开辟了新视角,也为WD的诊断与识别提供了指导。
基于对WD脂代谢紊乱机制的深入理解,优化现有治疗策略并探索新的干预靶点具有重要临床意义。目前,WD的主要治疗方法仍是终身口服药物治疗(如青霉胺、曲恩汀以及锌盐等)和饮食限铜,严重病例可考虑肝移植。值得注意的是,有效的驱铜治疗即可在很大程度上逆转脂代谢异常。研究表明,经过至少两年的规范治疗后,患者间异常的脂质参数(尤其是胆固醇水平)差异消失并趋于正常,提示WD相关的脂代谢紊乱在很大程度上是可逆的,这强调了长期规范治疗的重要性。
在坚持基础治疗的前提下,针对性的饮食管理可作为重要的辅助策略。研究提示,膳食脂肪的质与量对WD病程有显著影响。Du等在LEC大鼠模型中发现,与富含饱和脂肪酸(猪油)的饮食相比,富含多不饱和脂肪酸(PUFA)(如豆油、鱼油)的饮食展现出肝脏保护效应,能够减轻肝炎并延长生存期。相反,高热量或高脂饮食则进一步加重肝损伤。WD动物模型在高脂代谢应激时,会表现出更严重的肝脂肪变性、糖脂代谢紊乱及加速的肝损伤,其机制可能与线粒体铜蓄积和功能障碍的协同恶化有关。但也有研究发现,高热量的西方饮食可下调Atp7b⁻/⁻小鼠的胆固醇生物合成通路,同时减轻肝脏炎症,说明饮食干预可能调节WD中的脂代谢与炎症平衡。此外,Zhi等研究指出,不饱和脂肪酸水平下降可能削弱肝脏的抗氧化能力,而饱和脂肪酸水平上升则促进肝脂肪沉积,并提出通过补充不饱和脂肪酸,尤其是PUFA,以及采用低血糖指数饮食,可能在WD发病前对肝脏起到保护作用,延缓肝硬化进程。此外,研究还发现溶血磷脂酰胆碱水平的下降与肝细胞凋亡和线粒体功能受损有关,提示调节溶血磷脂酰胆碱水平可能成为干预WD肝损伤的新策略。因此,对WD患者进行饮食指导,在限铜基础上,鼓励增加PUFA摄入、限制饱和脂肪酸与总热量,可能有助于改善患者的代谢表型并延缓疾病进展。
不同于传统治疗,针对脂代谢紊乱进行干预亦是一个可行的研究方向。如前所述,核受体介导的脂质代谢和炎症改变可能参与WD的发病机制,因此激活LXR/RXR通路也是改善WD肝损伤和脂代谢紊乱的潜在治疗策略。在Atp7b⁻/⁻小鼠模型中,使用LXR激动剂(如T0901317)治疗,可在不降低肝铜的前提下,显著纠正低胆固醇血症等血脂异常,并同步减轻肝脏炎症和纤维化,改善肝功能与组织学。这证明通过重建WD患者的脂代谢稳态,可直接产生肝保护效益。另一个潜在的干预环节是PUFA代谢。Mazi等在探索WD的肝损伤机制时发现,疾病早期即出现花生四烯酸等代谢的显著失调,表现为酶促和非酶促氧化通路均被广泛激活,导致促炎、促血栓形成的氧脂水平显著升高。这一发现将氧化应激、炎症与脂代谢紊乱直接联系起来,解释了部分肝损伤机制,并且提出补充抗氧化脂质、使用特定的氧脂通路抑制剂或补充抗炎的n-3系列PUFA等干预策略。此外,极早期的营养干预也展现出调控疾病表型的潜力。例如,对WD怀孕母鼠补充胆碱后,能够改善子代肝脏的代谢转录谱与生长,体现出生命早期营养干预可能在遗传代谢疾病防治中发挥重要作用。
综上所述,未来对WD脂代谢紊乱的治疗以规范驱铜治疗为核心基础,优化膳食结构为重要辅助,并积极探索LXR/RXR及其他代谢通路调控的新型靶向药物。然而,目前尚缺乏驱铜治疗以外的其他临床研究,未来需进一步阐明饮食和代谢信号通路调控在WD治疗方面的临床转化潜力,以实现对患者更全面的综合管理。

4总结
目前,WD患者存在脂代谢异常已成为共识,肝脂肪变性是其常见的病理表现。研究显示,铜可能通过氧化应激影响线粒体与内质网功能,并涉及核受体、AMPK分子、自噬、表观遗传重编程以及肠-肝轴等多种分子机制,共同调控脂代谢。此外,也有研究基于脂代谢相关分子探索WD诊断和分型的生物标志物,进一步提示铜与脂代谢相互作用的重要性,并为探索新的治疗方式提供了基础理论依据。然而,当前关于WD脂代谢特点的研究仍存在一定局限性,例如样本量有限、随访时间较短而难以评估脂代谢异常的长期预后,以及铜与脂代谢相互作用的机制尚未完全阐明等。未来需开展大规模、长期随访的多中心队列研究,并借助疾病动物模型与多组学技术,深入揭示铜-脂代谢相互作用的分子机制,从而结合遗传背景与代谢特征,实现对WD脂代谢异常的精准管理。在临床实践中,应关注WD患者的脂代谢异常,并在临床管理中加强对相关指标的监测,以全面评估患者的代谢状态,为改善整体预后提供指导。

https://www.lcgdbzz.org/cn/article/doi/10.12449/JCH260304

高东静, 王睿欣, 李新华. 肝豆状核变性患者脂代谢紊乱的临床表型与致病机制[J]. 临床肝胆病杂志, 2026, 42(3): 515-521
来源:临床肝胆病杂志
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
