面对系统性红斑狼疮(SLE)早期识别困难、异质性高、风险难以分层的临床挑战,如何借助遗传评分工具实现精准风险评估与个体化诊疗决策?
????点击下图,进入 MedSeeker,一键获取 SLE 早期筛查、风险分层与精准管理的最新证据与策略。
研究设计
本研究纳入CSTAR队列2209例女性SLE患者及顺义研究695例女性健康对照。研究分三步:首先,基于文献筛选14个SLE相关候选性状,排除无东亚GWAS数据的4个性状后,为剩余10个性状分别构建性状级PRS;其次,采用弹性网络回归将筛选后与SLE显著关联的性状级PRS整合,构建metaPRS;最后,通过逻辑回归、ROC曲线分析及Delong检验,评估metaPRS与传统SLE-PRS在疾病预测、风险分层及临床表型关联中的效能差异,并以自举法进行内部验证。
研究结果
在评估的10个性状中,有5个性状级PRS与SLE风险存在显著关联(FDR<0.05),分别是:SLE本身(OR=2.03)、格雷夫斯病(OR=1.13)、
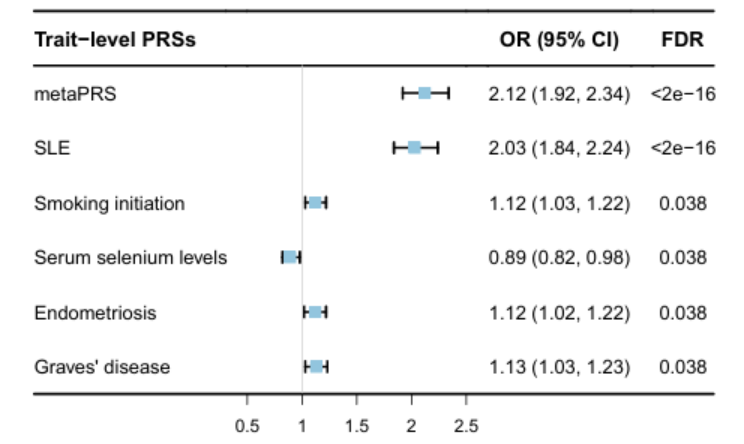
图1:多基因风险评分(PRSs)与系统性红斑狼疮(SLE)风险之间的关联。FDR,假发现率
将上述5个PRS通过弹性网络回归整合后,构建的metaPRS与SLE风险的关联(OR=2.12, FDR<2e-16)强于任一单个PRS。病例组与对照组间metaPRS分布存在极显著差异(p<2.2e-16,图2A)。剂量反应分析显示,SLE预测概率随metaPRS升高呈线性增加(图2B)。校准曲线与Hosmer-Lemeshow检验(p=0.799)均证实模型校准度良好(图3C)。自举法内部验证显示AUC的95%CI为0.67~0.71(图2D)。按metaPRS三分位数进行风险分层,高风险组SLE风险显著高于低风险组(OR=4.93, p<2e-16),风险区分能力优于传统SLE-PRS(图2E)。区分度方面,metaPRS的AUC为0.69,显著高于传统SLE-PRS的0.68(p=0.046, Delong检验,图2F),提示预测准确性有统计学意义的提升。
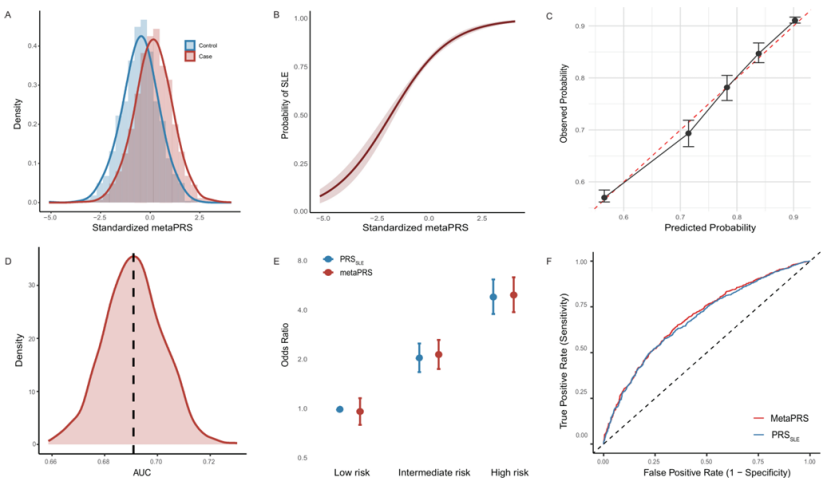
图2:使用多元多基因风险评分(metaPRS)预测系统性红斑狼疮(SLE)风险
metaPRS水平升高与多种自身抗体阳性显著相关,包括抗dsDNA、抗Sm、抗RNP及抗SSA抗体等(图3)。为解析其遗传基础,将metaPRS分解为SLE-PRS和风险因子PRS(即吸烟起始、血清硒、子宫内膜异位症、格雷夫斯病PRS的加权组合)。结果显示,SLE-PRS对SLE易感性的贡献(OR=2.03)远高于风险因子PRS(OR=1.26),且解释了metaPRS预测能力的75.4%。SLE-PRS与多种自身抗体阳性显著相关,而风险因子PRS未表现出任何与临床特征的显著关联。进一步比较两个极端亚组(高SLE-PRS/低风险因子PRS vs. 低SLE-PRS/高风险因子PRS)也证实,SLE-PRS主导了临床表型的表达。
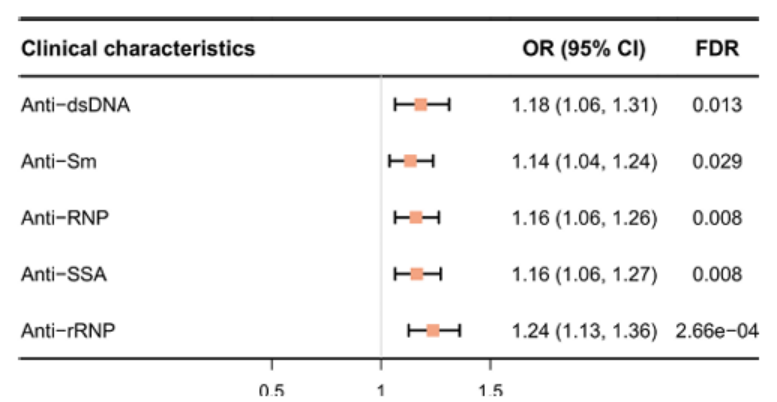
图3:临床特征与多基因风险评分(metaPRS)之间的关联
在亚组分析中发现,metaPRS在儿童期发病的SLE(诊断年龄<16岁)中显示出比成人发病SLE(诊断年龄≥16岁)更强的风险区分能力(高风险 vs. 低风险 OR: 6.24 vs. 5.03)(图4),提示其可能在早发性SLE中具有更高的预测价值。
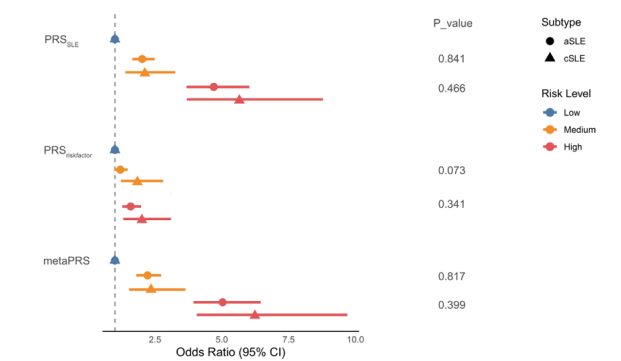
图4:三种PRS模型在cSLE和aSLE中的风险分层表现
研究结论
本研究构建了首个适用于东亚人群的SLE metaPRS模型。该模型整合SLE及四种相关性状的遗传信息,在风险预测与分层方面均显著优于仅基于SLE遗传变异的传统PRS。metaPRS与多种关键自身抗体阳性密切相关,且该关联主要由SLE-PRS组分驱动。该评分工具为SLE的早期筛查、个体化风险评估与精准管理提供了新策略,具有重要的临床应用潜力。
研究讨论
本研究通过创新的metaPRS方法,将SLE相关风险因素的遗传背景纳入预测模型,突破了传统PRS仅关注疾病本身遗传位点的局限。结果显示,metaPRS的预测效能(AUC 0.69)虽优于传统PRS(AUC 0.68),且差异具统计学意义,但提升幅度有限。这一现象与阿尔茨海默病、脑出血等其他复杂疾病的metaPRS研究结果一致,提示复杂疾病的遗传预测存在固有“天花板效应”。尽管如此,metaPRS在风险分层上的优势使其能够有效识别极少数高风险个体,对早期预防和强化监测具有明确的临床价值。
本研究鉴定出四个与SLE显著相关的非疾病本身风险因子:吸烟起始、血清硒水平、子宫内膜异位症和格雷夫斯病。这些发现验证了既往流行病学研究,并揭示其可能通过共享遗传结构、基因-环境相互作用或影响核心病理过程(如硒对免疫细胞和肠道屏障的调节)增加SLE风险。部分传统风险因素(如维生素D水平、饮酒)未显示显著遗传关联,提示这些因素可能更多通过后天获得性途径而非先天遗传易感性影响SLE发生,为理解基因-环境交互作用提供了新视角。
本研究的另一关键发现是揭示了SLE遗传架构中“易感性”与“表型”的分离现象:SLE-PRS既贡献了主要疾病风险,也驱动了自身抗体谱等临床表型;而风险因子PRS仅增加疾病易感性,却不影响确诊患者的临床表现。这提示环境风险因素可能通过启动或触发疾病发挥作用,而SLE特异性遗传变异则决定疾病的临床进程与严重程度。该发现对临床实践具有重要启示:风险因子PRS可用于识别高危人群进行一级预防,SLE-PRS则更适合已确诊患者的预后分层与并发症监测。
综上所述,本研究开发的metaPRS为SLE遗传风险评估提供了更全面的视角,证实了整合多维度遗传信息的可行性与临床价值。该工具有助于实现疾病的一级预防与早期诊断,也为推动SLE进入精准医学时代奠定了基础。未来前瞻性队列研究将进一步验证其临床应用的有效性与成本效益。
参考文献:Qiao Y, Cao M, Li M, et al. Development of a novel meta-polygenic risk score for risk assessment and clinical manifestation prediction in systemic lupus erythematosus. RMD Open. 2026;12(1):e006380.
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。