自身免疫性疾病的发生发展与体液免疫异常密切相关。患者体内会产生多种自身抗体,靶向自身组织中的不同抗原。然而,传统研究方法往往只能逐一检测已知的抗原-抗体反应,如同在广阔的信息海洋中捕捞有限的碎片,难以呈现疾病的全貌。
近年来,一种名为噬菌体免疫沉淀测序(PhIP-Seq)的高通量技术正在改变这一局面。它能够一次性检测针对数十万种不同抗原肽段的抗体反应,构建出患者个体化的“抗体反应指纹图谱”,为自身免疫病的标志物发现、发病机制研究和治疗预测开辟了新的路径。
PhIP-Seq的核心设计思路是:用覆盖人类蛋白质组或特定病原体蛋白组的噬菌体展示肽库,与患者血清或脑脊液中的抗体进行孵育;通过免疫沉淀捕获抗体结合的噬菌体;最后利用高通量测序识别这些噬菌体所展示的抗原肽段。
根据研究需求,研究者可以选用不同类型的抗原库:
人全蛋白质组库:覆盖5万以上人类蛋白,适用于系统性发现新自身抗体。
病毒组库:覆盖260种人类病毒,适用于探究病毒感染与自身免疫的关联。
自身免疫原库:深度覆盖92种自身免疫病相关的720余种蛋白抗原。
微生物组库:覆盖肠道菌群的分泌蛋白和膜蛋白。
这种灵活的设计使得PhIP-Seq能够适应从标志物发现到机制研究的多种场景。
在副肿瘤综合征领域,PhIP-Seq已展现出强大的标志物发现能力。发表于《新英格兰医学杂志》(NEJM)的一项研究中,研究者利用人全蛋白质组PhIP-Seq技术,在一名已知常规抗体阴性的精原细胞瘤相关

Mandel-Brehm C, et al. Kelch-like Protein 11 Antibodies in Seminoma-Associated Paraneoplastic Encephalitis. N Engl J Med. 2019;381:47-54.
类似的应用也出现在皮肌炎研究中。2022年《风湿病年鉴》(Ann Rheum Dis)的研究发现,转录因子Sp4自身抗体在皮肌炎患者中总体阳性率约为10%,但这些阳性患者中96.3%同时携带抗TIF1γ抗体。在抗TIF1γ阳性患者中,Sp4抗体阳性的患者无一例合并肿瘤,而Sp4抗体阴性的患者肿瘤发生率达14%。这一发现为皮肌炎患者的肿瘤风险分层提供了重要的分子依据。

Hosono Y. Coexisting autoantibodies against transcription factor Sp4 are associated with decreased cancer risk in dermatomyositis patients with anti-TIF1γ autoantibodies. Ann Rheum Dis. 2022;82:246-252.
PhIP-Seq不仅能发现新的标志物,还能揭示疾病发生的分子机制。
2022年《自然》(Nature)杂志的研究利用PhIP-Seq结合蛋白质芯片技术,揭示了EB病毒感染与

Lanz TV, et al. Clonally expanded B cells in multiple sclerosis bind EBV EBNA1 and GlialCAM. Nature. 2022;603:321-327.
通过晶体结构解析,研究者发现EBNA1和GlialCAM的结合表位具有显著相似性,而GlialCAM的磷酸化修饰进一步增强了这种交叉反应。在EAE小鼠模型(MS常用动物模型)中,用EBNA1多肽免疫后,小鼠产生了同时识别EBNA1和GlialCAM的抗体,且疾病严重程度显著加重。
这项研究首次从分子水平为EB病毒感染与MS发病的流行病学关联提供了直接的致病机制证据。
抗体组学在精准治疗和早期预警方面同样具有重要价值。
2025年《风湿病学》(Rheumatology)的研究利用PhIP-Seq在类风湿

Chen PK, et al. Anti-peptide antibodies, anti-SNRK and anti-HUWE1 antibodies as potential predictors of good response to tofacitinib therapy in rheumatoid arthritis patients. Rheumatology (Oxford). 2025;64:2451-2460.
更值得关注的是2024年《自然·医学》(Nature Medicine)的研究。研究者利用美国国防部血清库的大规模纵向队列,追踪了250名MS患者在发病前5年和发病后1年的抗体谱变化。结果显示,约10%的MS患者在发病前数年就已经存在独特的自身抗体特征,这些抗体靶向一个特定的基序序列,该序列存在于多种人类蛋白和病原体(包括EBV)中。这一抗体特征在时间上保持稳定,且携带该特征的MS患者血清神经丝轻链水平显著更高,提示更严重的神经轴索损伤。该特征在独立的发病期MS队列中得到验证,且对MS具有高度特异性,为MS的早期预警和诊断提供了潜在的分子标志物。

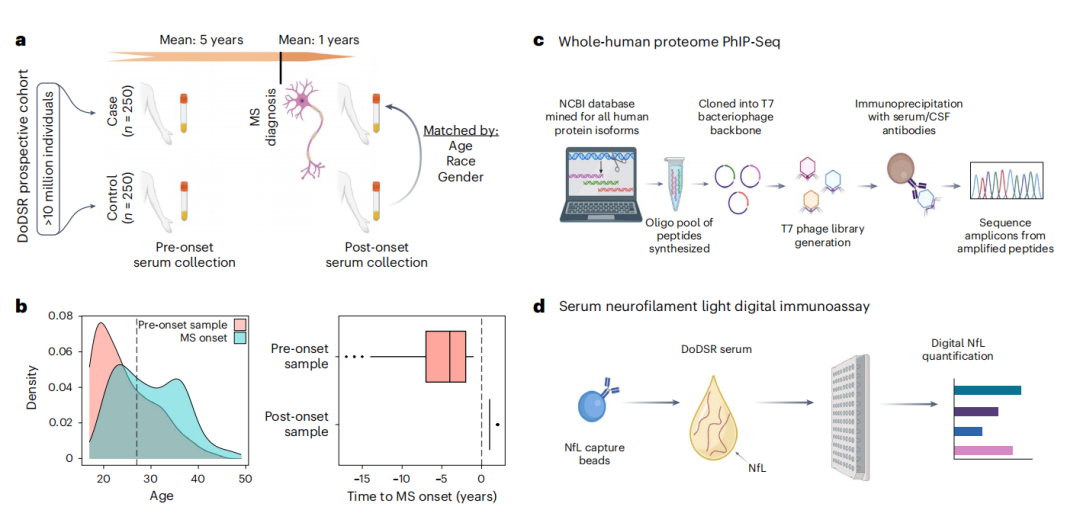
Zamecnik CR, et al. An autoantibody signature predictive for multiple sclerosis. Nat Med. 2024;30:1300-1310.
抗体组学在自身免疫病研究中形成了两种互补的研究范式。
其一是“发现-验证”范式:通过队列筛选发现差异抗体,在独立队列中验证其临床价值,适用于标志物研究和疗效预测。
其二是“机制驱动”范式:从特定的抗体线索出发,深入探究其识别的抗原、交叉反应的靶点及下游病理效应,适用于发病机制研究。
随着抗原库设计的不断优化(如引入翻译后修饰抗原、构象表位)、生物信息学分析工具的发展(如基序分析、AI辅助的抗原预测),以及多组学整合(单细胞BCR测序、蛋白质组学)的深入,抗体组学正在从“描述相关性”走向“揭示因果链”。
未来,基于抗体的精准分型、早期预警和个性化治疗策略,有望为自身免疫病患者带来更加精准和有效的诊疗方案。
医脉通是专业的在线医生平台,“感知世界医学