
糖尿病-心-肾-代谢性疾病(DCRM)包括肥胖、
一般健康管理
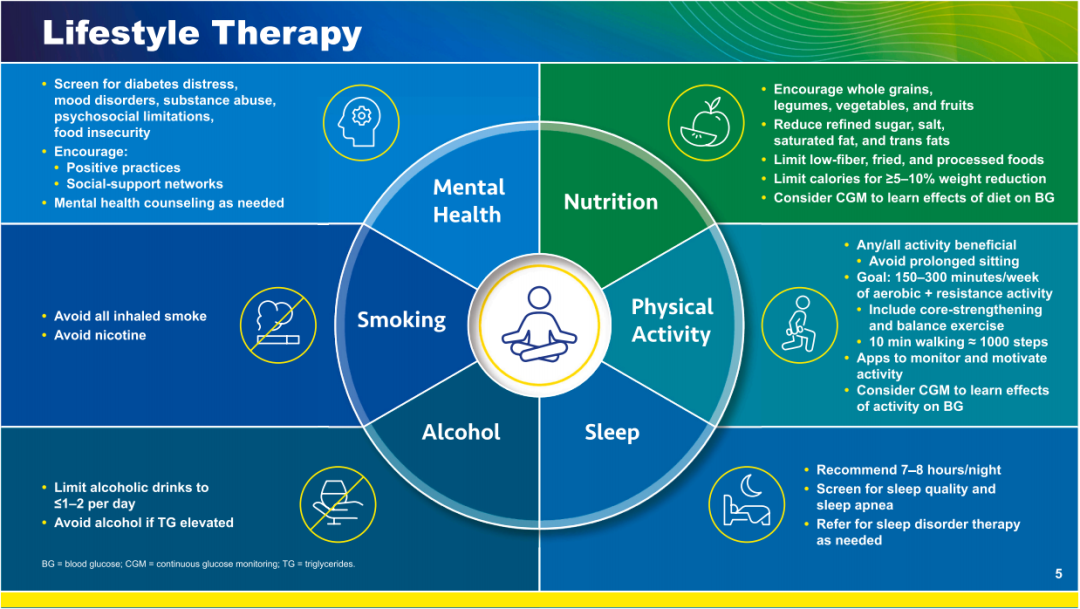
图1 生活方式干预
(1)良好的心理健康,解决情绪障碍、药物滥用、既往创伤和心理社会限制问题;
(2)营养和健康饮食,强调终身控制;
(3)运动:对于大多数人来说,建议每周至少进行150分钟的中等强度有氧运动和阻力运动,任何类型或数量的体育活动都是有用的,尤其是那些可以作为日常活动一部分的活动(例如,每天额外步行5-10分钟);
(4)改善睡眠:睡眠剥夺会加重
(5)戒烟;
(6)限制饮酒:男性每天≤350 ml的啤酒或150 ml的红酒或50 ml的白酒,女性减半。
除了血压、血糖和血脂检测,还应定期进行以下检查:
•大多数患者应每年进行
•
•冠状动脉钙化(CAC)是动脉粥样硬化斑块总负荷的替代指标,对于CAC非常低或正常的患者,可每5年重复检查一次。
•不建议将颈动脉内膜中层厚度(IMT)、负荷试验、6分钟步行距离测试和踝臂指数(ABI)作为常规筛查手段。
•每年应检查白
•当
•对于糖尿病和糖尿病前期患者,每年应进行
心肾风险管理
糖尿病前期包括空腹血糖受损(IFG)和/或糖耐量异常(IGT)。
证据表明,在血糖异常程度较轻的早期阶段进行干预,可预防其进展为2型糖尿病,甚至可能逆转为血糖正常状态。因此,糖尿病前期的管理重点在于识别高危人群并进行健康教育,强调生活方式干预、体重管理、控制心血管疾病危险因素,以及努力实现血糖正常化。
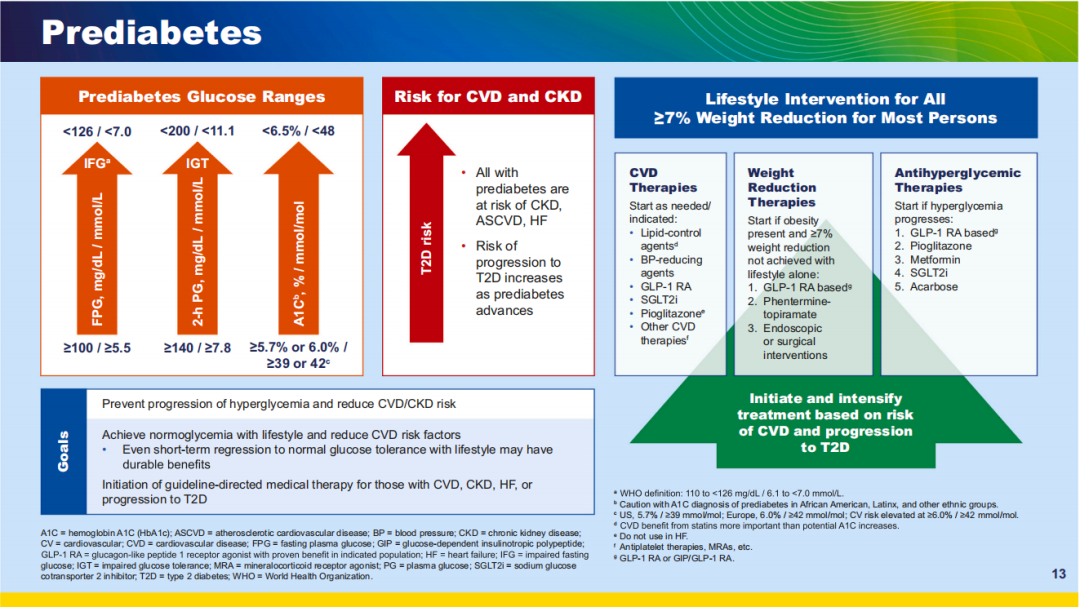
图2 糖尿病前期管理
持续减轻体重可增加实现血糖正常化的可能性。若单纯通过生活方式干预无法实现至少7%的体重减轻,应根据潜在合并症和
研究证实,
多项他汀类药物、

图3 血脂异常管理
他汀、PCSK9单抗等降LDL-C药物类别(图2中标绿色的药物)已在心血管结局试验(CVOT)中被证实具有获益。所有ASCVD风险升高者,如无禁忌证,均应接受最大耐受剂量的他汀治疗。若基线LDL-C高于目标值50%以上,应起始他汀联合依折麦布、bempedoic acid或PCSK9抑制剂(单克隆抗体或小干扰RNA)治疗。他汀基础上二线/三线药物的选择,取决于实现LDL-C目标所需的额外降幅。无论起始他汀单药还是联合治疗,均应每6-12周强化治疗直至达标。
对于纯合子型
虽然研究提示最佳甘油三酯水平可能更低,但当前公认的治疗目标(<150 mg/dL [<1.7 ncep="" atp="">150,<500 dl="">1.7,<5.7 mmol/L])者,应给与最大耐受他汀治疗和生活方式干预。REDUCE-IT试验表明,在他汀治疗基础上,加用
多项试验的亚组分析提示,甘油三酯≥200 mg/dL(≥2.3 mmol/L)且HDL-C≤40 mg/dL(≤1.0 mmol/L)者接受
甘油三酯严重升高(>500 mg/dL [5.7 mmol/L])者易发生
贝特类可降低甘油三酯达50%,被视为最强效的降甘油三酯药物。因合用某些他汀(如
总体而言,当前多数指南推荐高血压患者将血压控制在<130/80 mmHg,以降低心肾风险。尽管个体对降压药物的反应存在差异,但实现良好的血压控制应作为核心目标,必要时需采用联合治疗方案。对多数

图4 高血压管理
对于合并蛋白尿的高血压患者,降压方案应包含最大剂量的肾素-血管紧张素系统(RAS)抑制剂、钙通道阻滞剂(CCB)以及噻嗪型利尿剂(如
降压治疗期间出现的肌酐水平升高通常无需过度担忧,除非同时出现
炎症独立增加动脉粥样硬化性心血管疾病(ASCVD)风险,这一效应在LDL-C水平相对较低的人群中同样存在。CKD与ASCVD关联性的深入研究,进一步揭示了炎症在发病机制中的作用。鉴于CKD与ASCVD的密切联系,对于未确诊ASCVD的CKD患者,也需关注炎症对心血管风险的潜在影响。
改善心血管预后的基本方法包括生活方式干预(健康饮食、规律运动),以及超重/肥胖或糖尿病前期患者的体重管理。这些措施同时有助于减轻炎症反应,其中戒烟尤为关键。目前,通过抑制慢性低度炎症来降低心血管风险的治疗策略备受关注,本建议采取审慎立场,聚焦于既经心血管结局试验证实可降低主要不良心血管事件(MACE)、又对hsCRP具有明确显著抑制作用的治疗方案。此类治疗中,虽然作用机制未完全明确,但抗炎效应很可能参与了心血管获益。
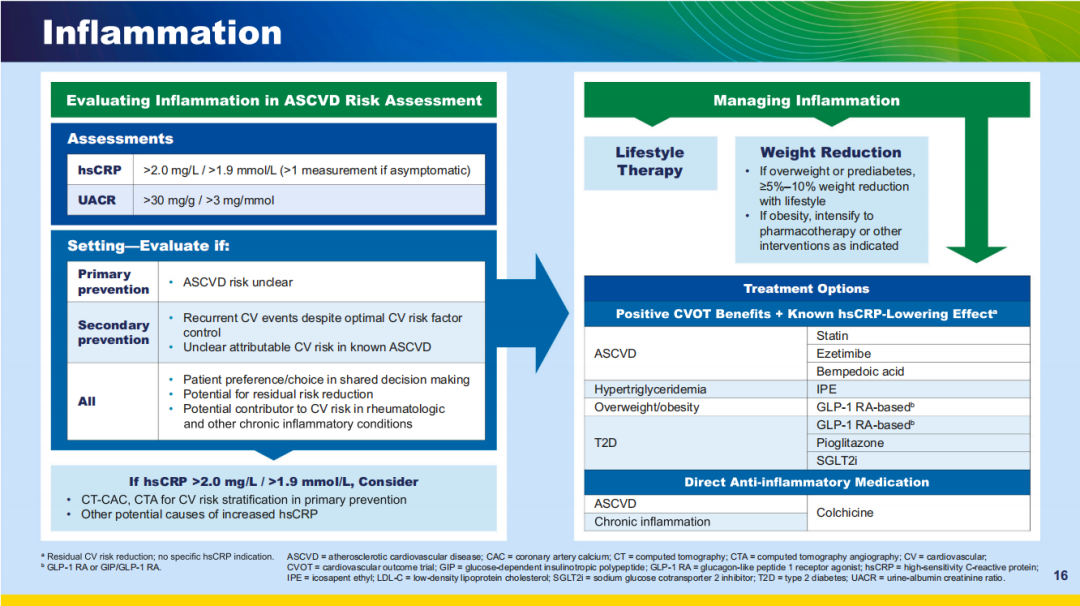
图5 炎症管理
具有潜在间接抗炎作用的治疗方案包括:
•他汀类、依折麦布或bempedoic acid(适用于ASCVD患者或有ASCVD风险的人群);
•二十碳五烯酸乙酯(IPE)(适用于甘油三酯>135 mg/dL且合并糖尿病或ASCVD者);
•GLP-1受体激动剂及GIP/GLP-1双重受体激动剂(适用于肥胖人群);
•GLP-1受体激动剂与吡格列酮(适用于2型糖尿病患者)。
对高危个体,在生活方式干预基础上联合靶向抗炎治疗具有充分依据。例如,GLP-1受体激动剂可在超重/肥胖伴ASCVD的非糖尿病人群中显著降低心血管事件。
除了生活方式干预外,对于已确诊ASCVD或ASCVD高危、CKD和/或心力衰竭的2型糖尿病患者,应处方GLP-1受体激动剂和/或SGLT2抑制剂。建议还将噻唑烷二酮类药物吡格列酮列为另一种可能具有心血管获益的药物,尤其适用于有卒中或卒中高危的患者,但需注意其导致心力衰竭的风险。

图6 2型糖尿病的降糖治疗
在解决了CVD、CKD或心力衰竭问题后,降糖方案应转向实现个体的血糖目标。ADA和AACE建议大多数T2D患者的糖化血红蛋白目标在6.5%-7.0%。心血管风险较低的年轻且更健康的个体可能受益于接近正常(<6.0%)的糖化血红蛋白目标,而对于患有更复杂疾病并伴有多种合并症的老年人,较高的糖化血红蛋白目标(约7.5%或更高)可能是合适的。
对于糖化血红蛋白水平高于其个体化目标1%-2%以上者,通常应启动联合治疗,即使是新诊断的T2D患者。联合治疗应包含作用机制互补的药物;不要将肠促胰素类药物(GIP/GLP-1 RA、GLP-1 RA和DPP4抑制剂)相互联合使用,也不要将磺脲类药物与格列奈类药物联合使用。
工作组建议根据所示的分级层次选择药物,但也应考虑患者的个体特征、偏好及药物可及性。在优选药物类别列表中,GLP-1受体激动剂(包括GIP/GLP-1 RA)位列二甲双胍之上,因为它们除了能够减轻体重、降低血压和提供心血管获益之外,还是最强效的非胰岛素类降糖药物。二甲双胍排在SGLT2抑制剂之前是由于其降糖效力,但应注意SGLT2抑制剂也能适度减轻体重和降低血压,并具有额外的肾脏和心血管获益。为实现血糖目标,许多患者需要GLP-1受体激动剂和/或SGLT2抑制剂以及二甲双胍联合治疗,尽管一些专家推荐其他药物如TZD或胰岛素。用药顺序应个体化选择。
许多2型糖尿病患者将需要胰岛素作为其血糖控制方案的重要组成部分。胰岛素与体重增加和低血糖风险相关;然而,对于无法达到血糖目标的个体,不应拒绝使用胰岛素。磺脲类药物除了能快速、相对强效(尽管是短期)地降低血糖外,获益甚少,且会增加低血糖和体重增加的风险。
确定最佳的抗栓治疗方案十分复杂。对于无ASCVD病史或其他危险因素的个体,通常不推荐使用
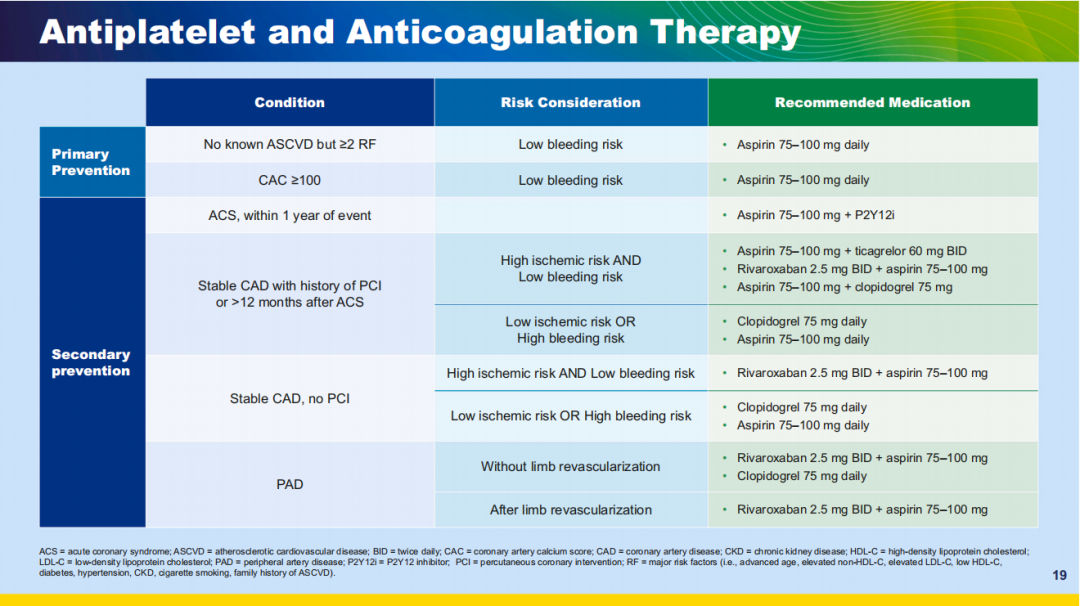
图7 抗板和抗凝治疗
对于ACS患者,包含阿司匹林和一种P2Y12抑制剂的双联抗血小板治疗(DAPT)持续至少12个月,可降低心肌梗死发生率和死亡风险。在接受药物治疗或血运重建治疗的ACS患者中,
接受PCI治疗的稳定性
无禁忌证的房颤患者应使用非
心肾和代谢合并症管理
减重策略(减重手术、GLP-1 RA、SGLT2抑制剂)在
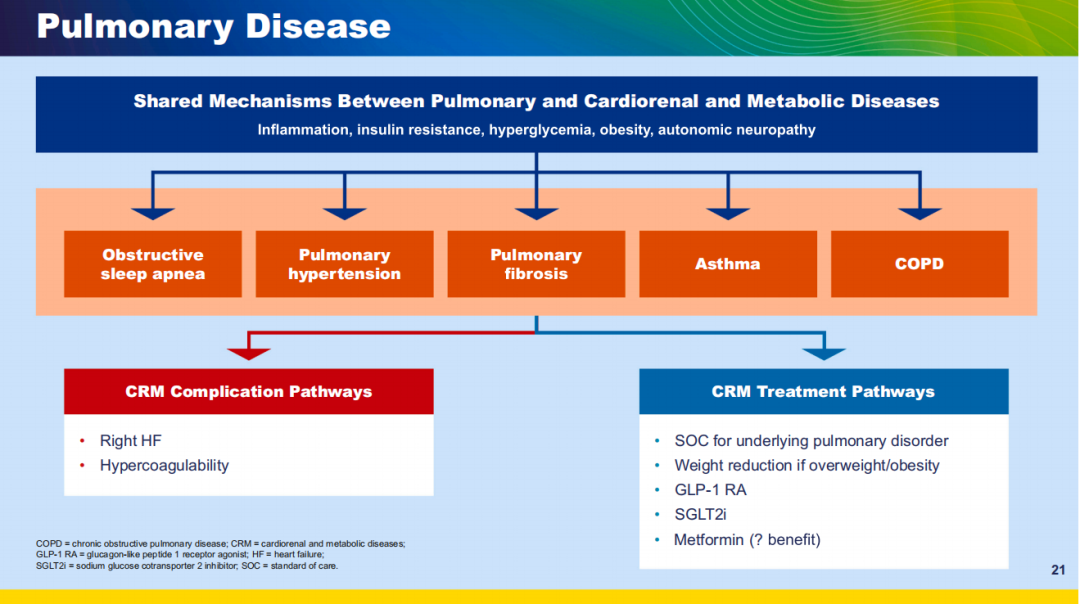
图8 肺部疾病管理
MASLD的特征是存在肝脂肪变性;且具有至少一项以下特征:超重/肥胖、2型糖尿病或代谢紊乱。应在病情发展为MASH之前筛查和识别出MASLD。
对于存在以下≥2种情况的患者,应进行肝病筛查:(1)高血糖;(2)高血压;(3)血脂异常(高甘油三酯、低HDL-C);(4)肥胖,尤其是腹型肥胖;(5)
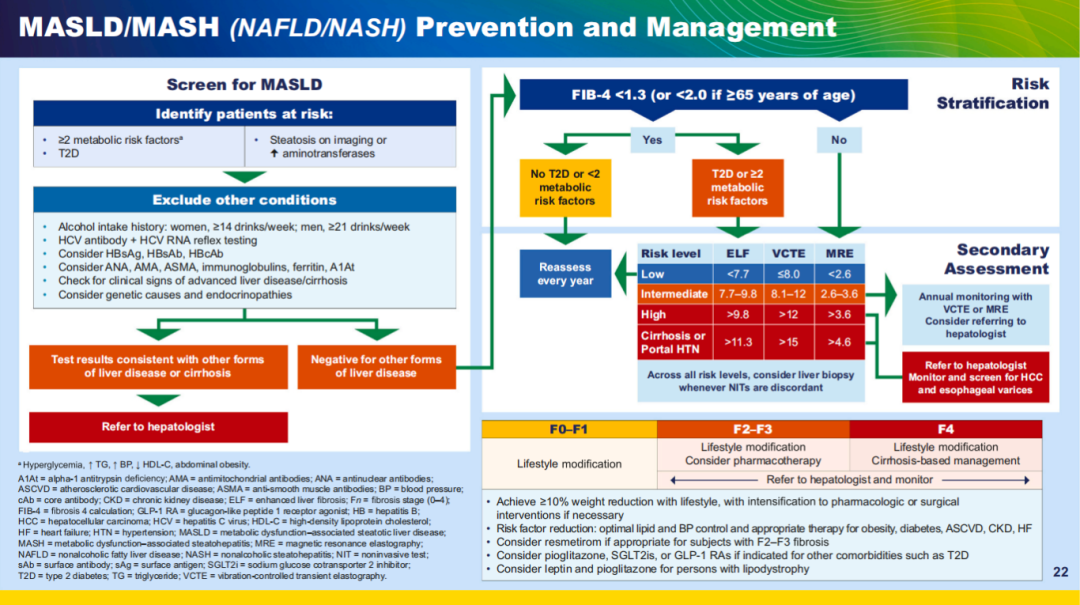
图9 MASLD/MASH预防和管理
建议检测
为了诊断MASLD,临床医生应评估其他潜在肝病病因,包括感染性肝炎、血色素沉着症、药物相关肝毒性和内分泌疾病(如甲状腺功能减退症和
对没有MASH或严重纤维化的MASLD患者,临床管理主要涉及生活方式改变(包括戒烟),以及酌情管理其他心血管和肾脏风险。对于超重或肥胖者,应根据需要给与生活方式干预、减重药物/手术,使体重降低≥10%。
对MASH或肝纤维化患者,需要一种协调的、多管齐下的方法,包括MASLD风险因素管理以及药物治疗(无论是否存在2型糖尿病),以解决活动性脂肪性肝炎并降低进行性纤维化风险。
近期,基于一项评估替代标志物的临床试验,口服、肝脏导向的甲状腺激素受体β选择性激动剂resmetirom被有条件地批准用于治疗F2-F3期纤维化的MASH。
减轻心血管风险至关重要,包括使用他汀类药物和其他降脂药物来达到血脂和血压目标。患者也可能受益于吡格列酮、SGLT2抑制剂和/或GLP-1或GIP/GLP-1 RA。
ASCVD防治措施包括生活方式干预和药物治疗,以控制血脂、血压、血糖和肥胖,并根据个人情况进行抗血小板/抗凝治疗。对于2型糖尿病患者,应使用具有心血管获益的GLP-1 RA治疗(度拉糖肽、利拉鲁肽或司美格鲁肽)以降低MACE风险。GLP-1 RA和SGLT2抑制剂也可用于2型糖尿病合并外周动脉疾病(PAD)患者,以降低心血管事件风险。
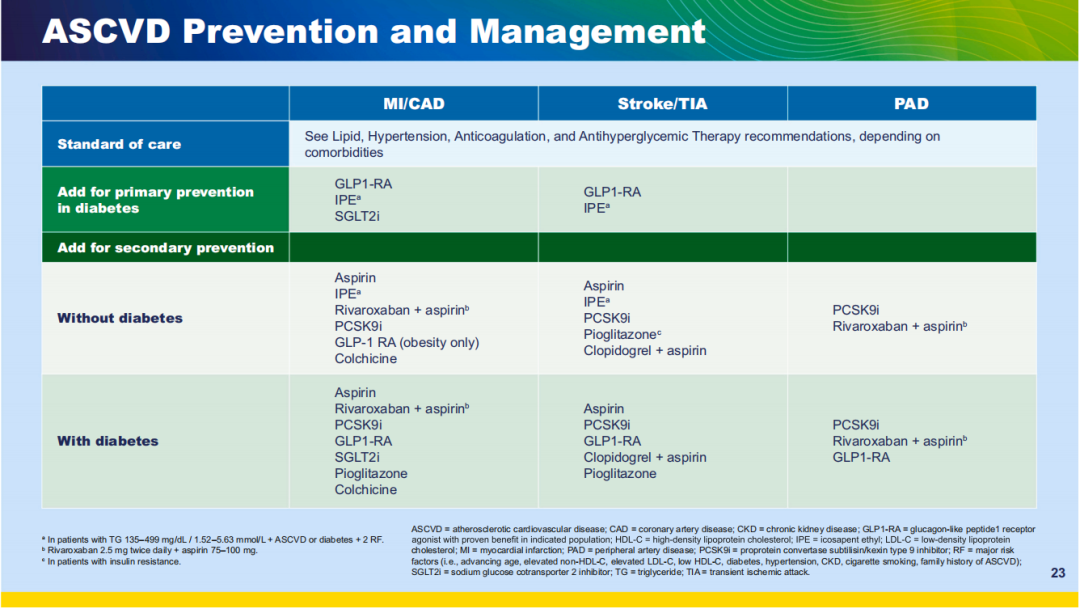
图10 ASCVD预防和管理
对于高甘油三酯血症、糖尿病和存在其他危险因素的患者,建议使用他汀类药物联合IPE进行一级预防,也可用于合并高甘油三酯血症ASCVD患者的二级预防。
通常不建议将阿司匹林用于糖尿病患者的一级预防;对于心血管风险较高的患者,应考虑使用阿司匹林。对于冠状动脉疾病或PAD患者,建议使用小剂量阿司匹林+利伐沙班2.5mg bid进行二级预防。
建议使用PCSK9抑制剂进行MACE二级预防。秋水仙碱也被证明可以预防CAD患者的MACE事件。对于卒中/TIA合并胰岛素抵抗的患者,建议使用吡格列酮进行二级预防,但禁用于心力衰竭患者。
心力衰竭的预防始于生活方式干预和危险因素控制措施。除了传统的危险因素控制外,预防心力衰竭的疗法包括:对于ASCVD事件高危的2型糖尿病以及CKD患者,使用SGLT2抑制剂;对于合并2型糖尿病的CKD患者,推荐使用非甾体类盐皮质激素受体拮抗剂来预防心力衰竭。

图10 心力衰竭预防和管理
心力衰竭的治疗基于左心室射血分数(LVEF)。
HFrEF患者应接受四联疗法,包括血管紧张素受体脑啡肽酶抑制剂(ARNI,若无法使用ARNI则用ACEI)、SGLT2抑制剂、β受体阻滞剂和甾体类MRA;如果存在充血,加用利尿剂。无论是否患有2型糖尿病,治疗方案都应包括SGLT2抑制剂。
HFmrEF患者应接受SGLT2抑制剂和利尿剂(如果存在充血),也可以考虑使用四联疗法中的其他药物。
HFpEF患者应接受SGLT2抑制剂治疗。对于部分射血分数低于正常的特定个体,ARNI(或ARB)和甾体类MRA可能是合适的。同样,对于合并2型糖尿病和CKD的HFpEF患者,可考虑使用非甾体类MRA。可考虑使用利尿剂治疗充血。LVEF≥45%且BMI≥30 kg/m²的心力衰竭、患者也可能从大剂量司美格鲁肽治疗中获益,该药已被证明可以改善心力衰竭症状。
生活方式和目标导向的治疗是降低心血管和CKD风险的关键基础。所有CKD患者都应接受最大耐受剂量的肾素-血管紧张素系统抑制剂和SGLT2抑制剂。开始使用肾素-血管紧张素系统抑制剂或SGLT2抑制剂时,预期估算肾小球滤过率会下降。对于肾素-血管紧张素系统抑制剂,估算肾小球滤过率下降幅度高达30%被认为是可接受的。SGLT2抑制剂引起的估算肾小球滤过率变化幅度较低(3%-10%)。除非怀疑发生严重的急性肾损伤,否则不应停用肾素-血管紧张素系统抑制剂或SGLT2抑制剂。估算肾小球滤过率低至20 mL/min/1.73 m²的患者可以启动SGLT2抑制剂。
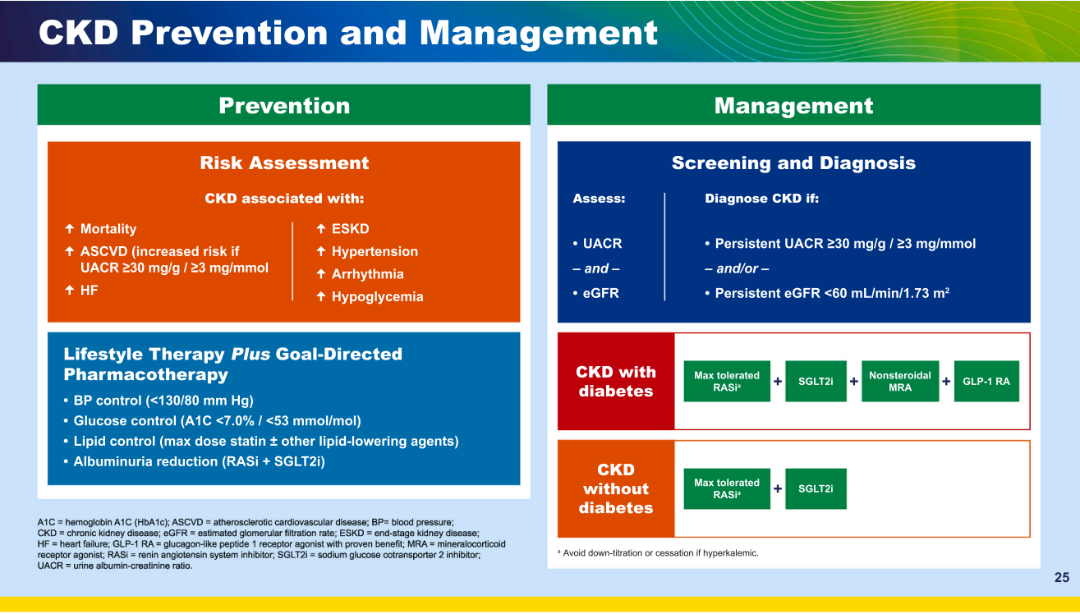
图12 CKD预防和管理
此外,2型糖尿病合并CKD的患者可以处方GLP-1受体激动剂,以降低ASCVD事件风险并改善肾脏结局。
在标准治疗基础上,加用非甾体类MRA非奈利酮可减缓2型糖尿病和蛋白尿患者的CKD进展并减少心血管事件(主要是心力衰竭)。
指南推荐的心力衰竭疗法已在广泛合并CKD的患者中进行了研究。研究表明,在eGFR低至20 mL/min/1.73 m²的心力衰竭患者中,SGLT2抑制剂的安全性和耐受性良好。其他药物,包括ACEI、ARB、ARNI和甾体类MRA(螺内酯和依普利酮),主要在eGFR低至30 mL/min/1.73 m²的患者中进行了研究。尽管在需要肾脏替代治疗的患者中使用β受体阻滞剂的证据有限,但未发现明确的安全性风险,因此可考虑在心力衰竭患者中使用。

图13 心力衰竭合并CKD的管理
非甾体类MRA非奈利酮已被证明可减少2型糖尿病合并CKD患者(eGFR低至25 mL/min/1.73 m²)的心血管和肾脏疾病事件。对于合并HFmrEF或HFpEF、2型糖尿病以及伴有蛋白尿的CKD患者,选择非奈利酮作为非甾体类MRA是合理的。在HFrEF患者中,如果患者能够耐受,则优先选择甾体类MRA。
许多用于治疗心力衰竭和CKD的药物会降低肾小球内压,治疗开始时可能出现eGFR急性下降,尤其在患者存在容量不足时。在包括或不包括心衰患者的临床试验中,这种eGFR下降与肾脏安全性信号无关。因此,在大多数情况下,不应因这种血流动力学效应而停止治疗或降级治疗。如果治疗开始后一周内eGFR下降超过30%,且在排除容量不足后,应评估其他病因,并考虑调整利尿剂剂量。
文献索引:Yehuda Handelsman, John E Anderson , George L Bakris, et al. DCRM 2.0: Multispecialty practice recommendations for the management of diabetes, cardiorenal, and metabolic diseases. 2024 Oct: 159: 155931. doi: 10.1016/j.metabol.2024.155931. Epub 2024 Jun 7.
新号「医脉循环」开通啦!深耕心血管、神经、外周血管介入及外科手术领域,及时传递国内外器械相关研究进展、临床指南更新,干货资讯持续输出,速戳关注,陪您解锁精准诊疗心视野~
编辑&排版:GXM
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)