Cronkhite-Canada综合征(CCS)是一种以胃肠道多发息肉和外胚层改变为特征的罕见非遗传性疾病。其病因尚不明确,缺乏诊断的金标准,并发消化道肿瘤风险高于一般人群,早期诊断较为困难,疾病容易复发,需长期随访。本文以临床病例为切入点,系统阐述了CCS的发病机制、临床表现、诊断及治疗策略,以供临床参考。
➤病例介绍
患者男性,53岁,因味觉障碍伴水样腹泻2个月就诊,近2周出现进行性脱发。近3个月内,患者体重下降3kg。既往有
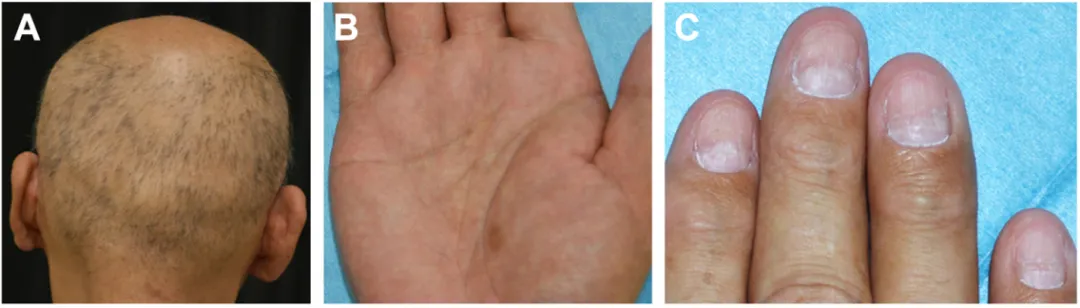
体格检查显示头发、眉毛、胡须及体毛弥漫性脱落(图A);手掌及手背见多发褐色斑疹(图B);甲床萎缩(图C)。腹部无压痛及包块。
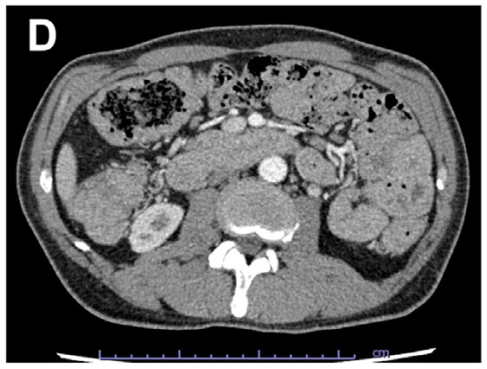
实验室检查提示低白蛋白血症(白蛋白3.0g/dL,参考范围4.1–5.1g/dL),而
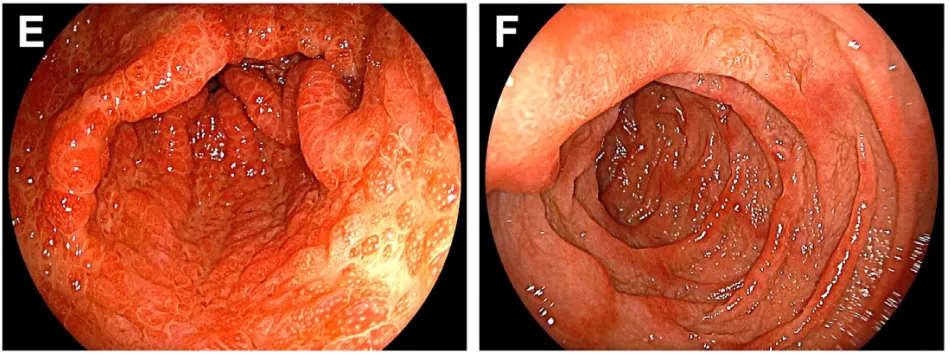
食管胃十二指肠镜检查见胃窦部多发小型红色半球状息肉(图E),十二指肠黏膜
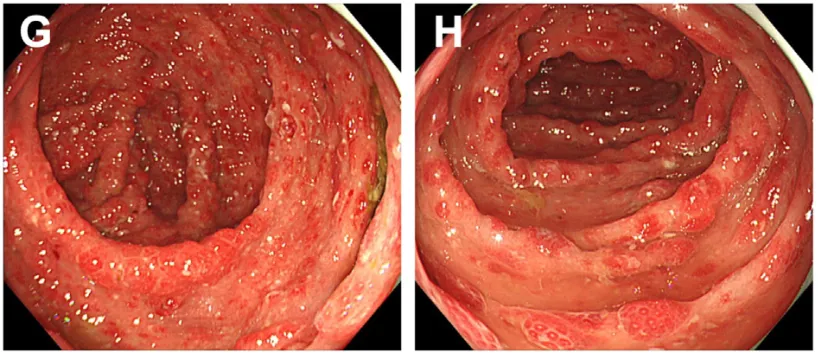
➤诊断和治疗
结合患者腹泻、味觉障碍等临床症状,脱发、色素沉着、指甲异常等特征性皮肤表现,以及胃肠道多发红色无蒂息肉的表现,最终被诊断为CCS。
患者初始每日口服30mg泼尼松龙治疗,并在10周内逐渐减量至10mg/d。用药后,患者临床症状迅速改善,但当剂量减至7.5mg/d时,腹泻症状轻度加重。考虑到症状严重程度中等,且需避免使用免疫抑制剂,遂在治疗方案中加用盐酸雷莫司琼,此后排便情况显著改善。
泼尼松龙在7个月内逐渐减量至停药,期间腹泻未复发。泼尼松龙治疗后3个月内,脱发症状有所改善;10个月时,胃及结
CCS自初报道距今已有60余年。Tomas曾估计本病发病率达百万分之一,平均发病年龄为50岁,男性稍多于女性。CCS息肉有5%-25%的恶变率,Padda于2008年曾指出,未经有效且及时治疗的CCS死亡率可高达55%。
CCS病因尚未明确,精神压力、躯体疲劳、应激、暴饮暴食、酗酒及长期服用药物是可能的诱发因素。Sweeter发现CCS息肉存在IgG4浸润。部分合并症如
CCS的消化道症状缺乏特异性,常见症状包括
CCS具有显著的外胚层受累表现,主要表现为皮肤色素沉着、指(趾)甲营养不良、
Goto根据CCS的临床病程分为5类:
表1 CCS的临床病程分类

1.CCS的临床评估
•实验室检查:CCS患者需要评估
•影像学检查:腹部/盆腔增强CT或MRI和(或)肠道CT或MRI重建可观察到胃、小肠和结直肠肠壁增厚、多发息肉样病变,可用于评估胃肠道的受累情况、息肉的负荷程度、并发症的诊断等,有助于评估CCS的病情。CCS患者常伴随蛋白从肠道中丢失,核医学检查有助于明确肠道蛋白丢失。
•
2.CCS的诊断和鉴别诊断
CCS目前尚无诊断的金标准,需结合临床表现、辅助检查进行综合诊断。综合来看,可供参考的CCS诊断标准如下:
①临床表现为慢性腹泻,伴或不伴有腹痛、恶心等;
②有明显的外胚层受累表现,如毛发脱落、皮肤色素沉着、爪甲营养不良等;
③常合并有低白蛋白血症;
④内镜下可见胃肠道多发息肉,其病理多为错构瘤性息肉;
⑤需除外其他遗传性错构瘤息肉病。
CCS需与以下疾病相鉴别:Peutz-Jeghers综合征、家族性腺瘤性息肉病、幼年息肉病、Cowden病(表2)。
表2 CCS的鉴别诊断

CCS的治疗目标是控制消化道症状及外胚层症状,减少疾病复发,改善患者预后。常见治疗方式包括一般支持性治疗、药物治疗及外科手术治疗。
1.支持性治疗
支持性治疗包括纠正水电解质紊乱,肠外或
2.药物治疗
•
•免疫抑制治疗:免疫抑制治疗是糖皮质激素依赖、无效或无法耐受的CCS患者的治疗用药选择之一,如
•其他药物:对于激素及免疫抑制剂均无效的CCS患者,有个案报道英夫利昔单抗、维得利珠单抗可用于上述患者的治疗,并有助于控制症状,改善内镜下表现,但相应报道极少,仍有待进一步完善。
3.外科手术治疗
外科手术治疗多用于CCS出现严重并发症时才考虑,譬如肠套叠、
既往认为CCS预后较差,主要死亡原因包括消化道出血、感染、营养不良、电解质紊乱、凝血异常或循环衰竭。近年来,随着糖皮质激素的广泛应用、充分的营养支持和定期的内镜监测,使CCS的预后有所改善。早期诊断,以糖皮质激素和免疫抑制剂治疗为中心的药物治疗,定期的内镜监测和新的治疗方案,长期、规范地随访,有助于进一步改善预后。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)