

前言
2026年欧洲肺癌大会(ELCC 2026)于3月25日至28日在丹麦哥本哈根拉开帷幕。Pumitamig 作为一款靶向PD-L1/VEGF-A的在研双特异性抗体,在晚期肺癌治疗领域展现出良好的应用潜力。中国研究者已针对EGFR突变NSCLC、一线PD-L1阳性NSCLC及广泛期小细胞肺癌(ES-SCLC)三大核心人群,完成多项II期临床探索,斩获了令人瞩目的疗效与安全性数据。本文整理编译了本次大会上中国学者公布的Pumitamig在国内人群中的关键临床研究内容,同时热切期待中国学者在本次学术会议上深入解读该系列研究成果,为全球肺癌精准治疗贡献重要的中国证据。
21P
Pumitamig(PD-L1/VEGF-A双抗)联合化疗治疗EGFR TKI进展后的EGFR突变晚期NSCLC:中国II期研究结果
研究背景
Pumitamig(BNT327/BMS986545)是一款在研双特异性抗体,可同时靶向肿瘤及肿瘤微环境中的PD-L1与VEGF-A。前期研究显示,该药联合化疗在经治EGFR突变
研究方法
患者接受Pumitamig联合
研究结果
截至2025年10月18日,本研究共入组64例患者,中位年龄为59岁,89.1%的患者美国东部肿瘤协作组(ECOG)体能状态评分为1分。所有入组患者均纳入安全性、疗效及PD-L1表达水平分析。中位随访时间为20.4个月,结果显示,中位PFS为9.6个月,12个月PFS率为42.4%。中位OS尚未达到,12个月OS率为79.7%。各PD-L1表达水平亚组(阴性、低表达、高表达)均观察到明确的抗肿瘤活性。
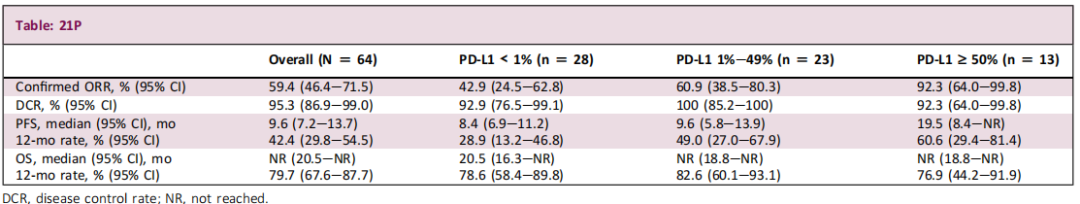
安全性方面,所有患者均报告治疗相关不良事件(TRAE,与任一研究药物相关),其中68.8%(44/64)为≥3级TRAE,主要包括血液学不良事件、转氨酶升高及
研究结论
Pumitamig联合化疗在不同PD-L1表达水平(含PD-L1<1%)的EGFR突变晚期NSCLC患者中,均显示出令人鼓舞的PFS与OS获益,安全性特征与既往EGFR-TKI治疗失败后EGFR突变NSCLC人群的报道一致,其中PD-L1高表达患者获益最为突出。
69P
Pumitamig(PD-L1/VEGF-A双抗)单药一线治疗PD-L1阳性非鳞状和鳞状NSCLC:中国Ib/IIa期试验数据
研究背景
Pumitamig(BNT327/BMS986545)是一种在研双特异性抗体,可同时靶向肿瘤及肿瘤微环境中的PD-L1与VEGF-A。前期研究已证实其在晚期NSCLC中具有令人鼓舞的抗肿瘤疗效及可耐受的安全性。本文报告该项正在进行的临床试验中Pumitamig治疗晚期NSCLC的更新数据,其中包含
研究方法
本项Ib/II期临床试验纳入既往未经治疗的PD-L1阳性晚期NSQ(EGFR/ALK野生型)及SQ NSCLC患者。患者接受Pumitamig 20 mg/kg每2周一次静脉输注,直至发生不可耐受毒性、疾病进展或撤回知情同意。肿瘤疗效评估在前1年每6周进行一次,此后每12周评估一次。主要研究终点为ORR,次要终点包括其他疗效指标及安全性特征。
研究结果
截至2025年12月22日,本研究共入组17例NSQ NSCLC患者、13例SQ NSCLC患者。总体人群未确认客观缓解率(uORR)为47.1%,NSQ NSCLC患者uORR为47.1%,SQ NSCLC患者uORR为61.5%;总体人群中位PFS为13.6个月,其中PD-L1 1%–49%亚组中位PFS为13.6个月,PD-L1≥50%亚组为17.9个月,NSQ NSCLC患者中位PFS为13.6个月,SQ NSCLC患者中位PFS未成熟。总体人群中位OS为20.7个月,其中PD-L1 1%–49%亚组中位OS为16.0个月,PD-L1≥50%亚组未达到。各PD-L1表达水平亚组均观察到确切抗肿瘤活性。
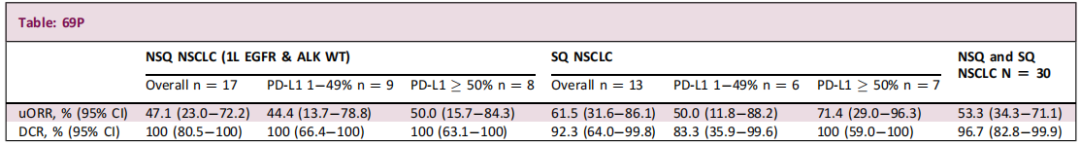
全部30例患者中,≥3级TRAEs发生率为40.0%,irAEs发生率为33.3%,其中≥3级irAEs占10.0%。无治疗相关死亡事件。NSQ与SQ亚组安全性特征总体相当。
研究结论
Pumitamig单药在晚期NSCLC(包括SQ)患者中,展现出跨PD-L1表达水平的初步抗肿瘤活性与可控可接受的安全性。Pumitamig联合化疗用于NSCLC的治疗策略,目前正在多项全球临床研究中进一步探索,包括ROSETTA Lung-02(NCT06712316)及BNT327-07(NCT06841055)。
426P
Pumitamig(PD-L1/VEGF-A双抗)联合化疗一线治疗ES-SCLC的II期研究:更新的疗效与安全性结果
研究背景
ES-SCLC经一线免疫联合化疗治疗后预后仍不佳。Pumitamig(BNT327/BMS986545)为一款在研双特异性抗体,可同时靶向肿瘤及肿瘤微环境(TME)中的PD-L1与VEGF-A,通过阻断肿瘤细胞PD-L1以恢复效应T细胞功能,并在肿瘤微环境中局部中和VEGF-A。两项II期临床研究显示,Pumitamig联合化疗一线治疗ES-SCLC在中国及美国人群中均展现出令人鼓舞的抗肿瘤活性。
研究方法
本项开放标签、单臂、多中心临床研究在中国开展。入组标准为:年龄≥18岁、ECOG体能状态评分为0-1分、经组织学或细胞学确诊ES-SCLC,且既往未接受过系统性抗肿瘤治疗的患者。患者接受Pumitamig联合铂类+
研究结果
截至2025年10月18日,研究共入组50例患者,中位年龄59岁(范围:46-75岁),ECOG体能状态评分为1分者占80%,吸烟者占66%。中位随访16.8个月(95%CI:11.3-20.8),中位治疗持续时间26.5周(95%CI:18.1-37.1),截至数据截止仍有2例患者在组治疗。
经确认ORR为82.0%,中位缓解持续时间5.52个月(95%CI:4.2-6.9),DCR为94.0%。中位PFS为6.93个月(95%CI:5.1-8.2),中位OS为16.85个月(95%CI:14.3-20.5),12个月OS率为72.0%(95%CI:57.4%-82.4%)。
安全性方面,所有患者均发生至少1项治疗突发不良事件(TEAE),其中43例(86%)出现≥3级治疗相关TEAE。最常见TEAE为中性粒细胞计数减少(92%)、
研究结论
在本项II期临床研究中,Pumitamig联合铂类化疗一线治疗ES-SCLC展现出令人鼓舞的疗效与可接受的安全性特征,其临床价值正在全球III期ROSETTA Lung-01研究(NCT06712355)中开展进一步评估。
参考文献:
[1] Yilong Wu, et al. Progression-free survival and overall survival withpumitamig (PD-L1 x VEGF-A bsAb) plus chemotherapy inpatients with EGFR-mutated advanced non-small cell Iung cancer following progression with EGFR TKI in China: Phase Il study results. 2026 ELCC Abstract 21P.
[2] Liang Zhang, et al. First-line pumitamig (PD-L1 X VEGF-A bsAb) monotherapyin PD-L1+ non-squamous and squamous non-small cell lungcancer: Data from a phase Ib/lla trial in China. 2026 ELCC Abstract 69P.
[3] Ying Liu, et al. Phase Il study of first-line pumitamig (PD-L1 x VEGF-AbsAb) plus chemotherapy for extensive-stage small cell lungcancer (ES-SCLC): Updated efficacy and safety results. 2026 ELCC Abstract 426P.
撰写:Kenken
审核:Faline
排版:Kenken
执行:Faline
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)