
前言
2026年欧洲肺癌大会(ELCC 2026)即将于3月25日至28日在丹麦哥本哈根拉开帷幕。
409O
Obrixtamig联合Ezabenlimab治疗表达DLL3的SCLC或其他NECs患者的I期剂量递增试验
研究背景
DLL3在SCLC在内的神经内分泌肿瘤(NECs)中呈高频表达。Obrixtamig为一种IgG样DLL3/CD3 T细胞衔接分子,在SCLC临床前模型中可上调PD-1与PD-L1表达。联合应用免疫检查点抑制剂Ezabenlimab有望缓解该适应性免疫检查点上调,并进一步增强抗肿瘤效应。目前一项I期临床试验(NCT05879978)正在评估Obrixtamig联合Ezabenlimab用于晚期/复发性DLL3阳性NECs(含SCLC)患者的临床疗效。
研究方法
本试验纳入至少接受1线含铂化疗失败或不适合标准治疗(SoC)的患者。Obrixtamig每周给药1次,每3
研究结果
截至2025年11月20日,共45例患者接受了至少1个周期的治疗,中位治疗周期数为5个(范围:1-31),患者中位年龄57岁(范围:33-78岁),东部肿瘤协作组体能状态评分(ECOG PS)0分与1分者分别占33%和67%。既往接受过抗PD-1/PD-L1治疗的患者比例为49%。剂量递增阶段共出现3例DLTs,目标剂量阶段未观察到DLTs,尚未达到MTD。
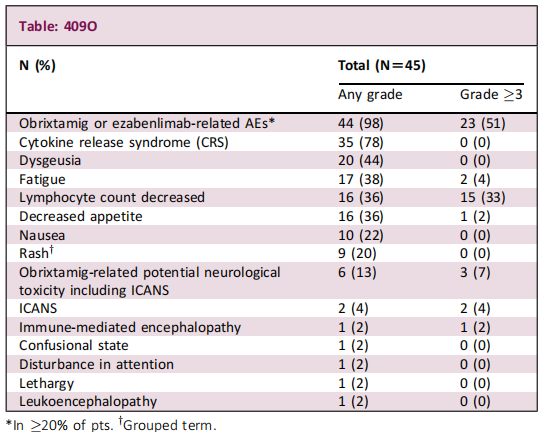
51%的患者发生≥3级治疗相关不良事件(TRAEs),13%的患者因TRAEs终止治疗。3例(7%)患者出现与Obrixtamig相关的≥3级神经系统不良事件,其中包括2例免疫效应细胞相关神经毒性综合征(ICANS)和1例脑病。未观察到≥3级的细胞因子释放综合征(CRS)。
40例患者接受了≥90 μg/kg的临床有效剂量Obrixtamig治疗,该人群ORR为30%,DCR为58%,中位PFS(mPFS)为4.4个月,中位缓解持续时间(mDoR)为8.8个月。最高剂量组(1080 μg/kg,n=12)ORR为58%,DCR为83%,mPFS为10个月,mDoR为8.8个月。在接受≥90 μg/kg剂量治疗的18例SCLC患者中,ORR为33%,DCR为67%,mPFS为5.7个月,mDoR尚未达到。
研究结论
Obrixtamig联合Ezabenlimab在经治的DLL3阳性NECs患者中展现出可控的安全性与耐受性,在高剂量Obrixtamig治疗组及SCLC患者中均观察到令人鼓舞的抗肿瘤疗效。
417P
SNC115治疗复发/难治性SCLC及LCNEC:I期研究的安全性、药代动力学及初步疗效结果
研究背景
DLL3在SCLC中呈高表达状态,提示其可作为潜在的治疗靶点。SNC115为一种经CD70武装化、靶向DLL3的CAR-T细胞。
研究方法
本项单臂、单中心、开放标签I期研究旨在评估SNC115在至少接受过一线标准治疗失败的复发/难治性SCLC及大细胞神经内分泌癌(LCNEC)患者中的初步安全性与药代动力学特征。剂量递增阶段采用加速滴定联合标准3+3设计,计划给药剂量水平为:DL1 1.0×10⁵、DL2 3.0×10⁵、DL3 1.0×10⁶、DL4 3.0×10⁶、DL5 6.0×10⁶个CAR+ T细胞/公斤体重。受试者将接受白细胞分离术、淋巴耗竭(LD)化疗(
研究结果
截至2025年12月1日,共入组7例SCLC患者,分别接受DL1(n=1)、DL2(n=3)、DL3(n=2)、DL4(n=1)剂量水平的SNC115治疗。患者中位年龄为53岁(范围:40-69岁),既往接受系统治疗的中位线数为3线(范围:2-6线),其中5例患者接受了桥接治疗。
DL1组与DL4组各有1例患者发生细胞因子释放综合征(CRS),均为1级,经托珠单抗治疗后快速缓解。≥3级血液学治疗相关不良事件(TEAE)包括淋巴细胞计数降低(7/7)、白细胞计数降低(2/7)及
研究结论
SNC115展现出良好的安全性与耐受性,未观察到DLT及ICANS,且CRS表现为轻度、可逆性,值得在后续更高剂量水平中进一步探索。同时,本研究也观察到初步的抗肿瘤疗效信号。
参考文献:
[1] Julien Mazieres, et al. A phase I dose escalation trial of obrixtamig + ezabenlimab in patients (pts) with small cell lung cancer (SCLC) or other neuroendocrine carcinomas (NECs) expressing DLL3. 2026 ELCC Abstract 409O.
[2] T. Chu, et al. SNC115 in patients with relapsed/refractory small cell lungcancer (SCLC) and large cell neuroendocrine carcinoma(LCNEC): Safety, pharmacokinetic, and preliminary efficacyresults from a phase I study. 2026 ELCC Abstract 417P.
撰写:Kenken
审核:Faline
排版:Kenken
执行:Faline