前言
在
然而,尽管新型ADC在HER2低表达群体中的疗效已经得到证实,但关于HER2低表达状态在HER2阴性乳腺癌中的诊断和预后意义尚未完全明确1,缺乏描述这类患者真实世界治疗模式与结局的数据。为此,一项源自美国的患者队列研究就此展开,旨在回顾性分析既往接受过化疗的HER2低表达mBC患者的真实治疗模式和结局,以揭示其在当前标准治疗下的临床现状1。本文对该研究进行系统梳理,为读者提供参考。
本研究是一项回顾性、观察性真实世界队列研究,首次利用美国全国性电子健康记录衍生的去标识化数据库——Flatiron Health转移性乳腺癌数据库,来评估HER2低表达mBC患者的人口统计学特征、治疗模式及结局。研究纳入了数据库中2011年1月1日至2023年4月30日期间,确诊为HER2低表达(IHC 1+或IHC 2+/ISH-)的成年mBC患者。所有患者在转移阶段接受过一线化疗后,启动了下一线(基线治疗线)治疗,且至少有90天的随访记录。
研究按激素受体(HR)状态进行分层分析,描述基线治疗线启动时的人口统计学和临床特征、后续治疗模式与结局,并对HR阳性患者按既往是否接受过内分泌治疗进行事后敏感性分析。
治疗线(LOT,line of therapy):采用Flatiron Health肿瘤学家制定的算法进行定义,不考虑手术和放疗。
◼ 基线LOT(index LOT):本研究的核心观察点,即患者在接受一线化疗后启动的首次后续治疗。
结局指标:以真实世界至治疗中断/死亡时间(rwTTD/D)、真实世界至下次治疗/死亡时间(rwTTNT/D)以及真实世界总生存期(rwOS)为主要结局指标。
研究最终纳入3765例HER2低表达mBC患者,具体特征如表1所示。其中,78.8%的患者为HR阳性,21.0%为HR阴性;31.3%为初诊IV期(首次诊断即存在远处转移)乳腺癌1。基线LOT前,患者接受治疗线数的中位数为1,52.4%的患者将基线LOT作为二线治疗;整体中位随访时间为54.5个月1。
按HR状态分层分析1,HR阳性与阴性队列患者特征基本相似(表1),但也存在差异:HR阳性队列中初诊IV期的比例更高(32.7% vs 26.0%);基线LOT前接受≥2线治疗的比例更高(56.1% vs 16.2%);转移阶段接受过内分泌治疗的比例显著更高(61.7% vs 14.1%);从mBC确诊到基线LOT的中位时间更长(13.3个月 vs 6.5个月);随访时间也更长(57.0个月vs 42.6个月)。
表1 患者基线特征1

对HR阳性患者的事后敏感性分析显示1,与未接受过内分泌治疗的患者相比,接受过的患者初诊IV期比例更低(28.1% vs 40.1%),在2011–2014年间开始基线LOT比例更低(15.8% vs 27.2%),从mBC确诊到基线LOT的中位时间更长(22.7个月vs 5.54个月),既往治疗线数也更多。
无论是在基线LOT还是其后续的治疗中,单药化疗都是HER2低表达mBC患者最主要的选择1。HR阳性队列中,有45.4%的患者接受单药化疗作为基线LOT(图1),HR阴性队列中这一比例高达66.9%(图2)。
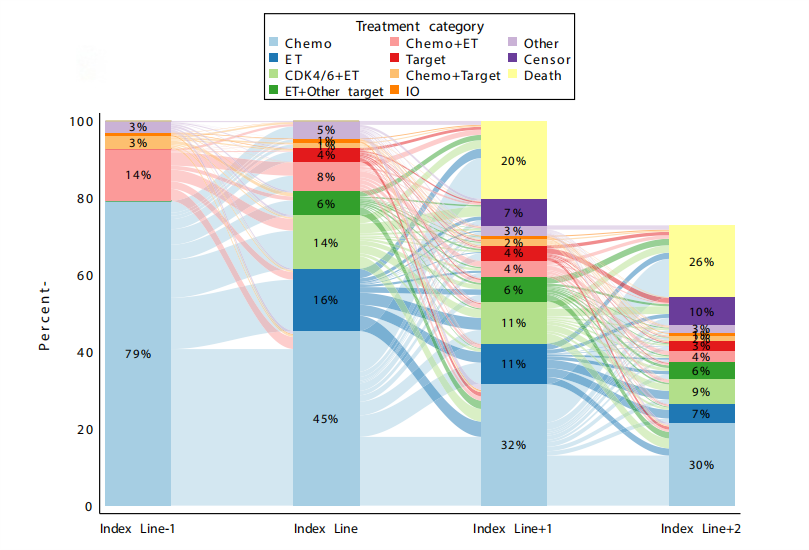
图1 HR阳性、HER2低表达mBC患者基线LOT前后的治疗模式1
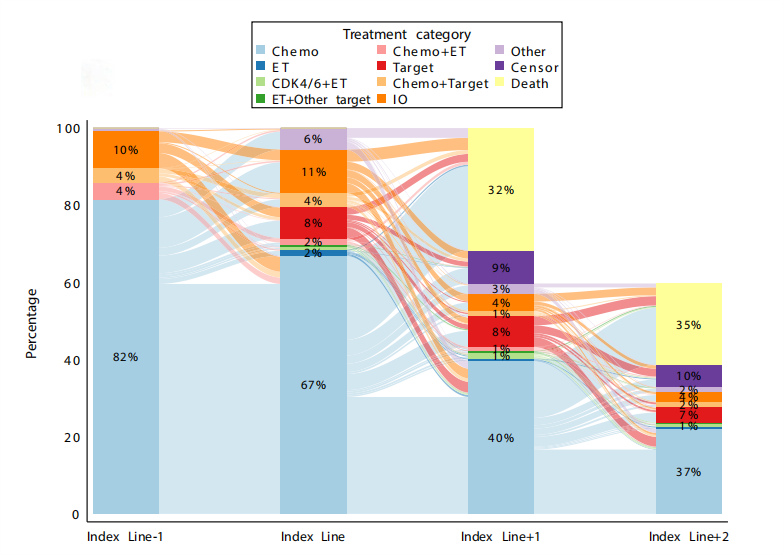
图2 HR阴性、HER2低表达mBC患者基线LOT前后的治疗模式1
整体队列结局:中位随访54.5个月后,75.5%(2843/3765)的HER2低表达mBC患者发生死亡。全队列中位rwOS为15.8个月(95% CI:15.2-16.5),中位rwTTD/D 为4.1个月(95% CI:3.9-4.2),中位rwTTNT/D为5.1个月(95% CI:4.8-5.3)。
HR状态分层结局:HR阳性的HER2低表达mBC患者各项结局指标均优于HR阴性患者(图3)。
◼ HR阳性:中位rwOS为17.6个月(95% CI:16.7-18.5),rwTTD/D为4.2个月(95% CI:4.1-4.5),rwTTNT/D为5.2个月(95% CI:5.0-5.5)。
◼ HR阴性:中位rwOS为11.1个月(95% CI:10.2-12.2),rwTTD/D为3.5个月(95% CI:3.2-3.8),rwTTNT/D为4.6个月(95% CI:4.3-5.0)。
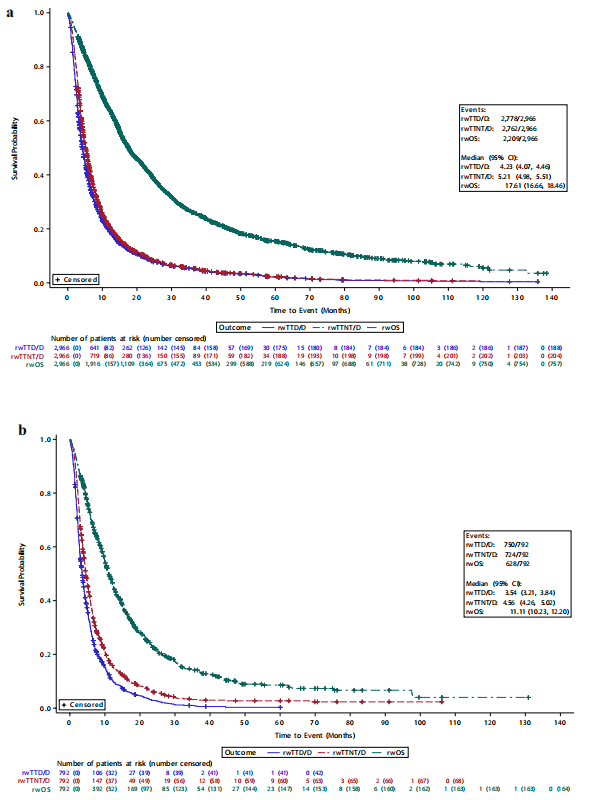
图3 HR阳性(a)、HR阴性(b)队列的真实世界结局1
本研究基于美国真实世界大样本队列,系统揭示了T-DXd适用人群——既往接受过一线化疗的HER2低表达mBC患者的治疗模式与临床结局,填补了相关数据空白,反映了这类人群所面临的临床治疗现状。
研究发现,真实世界中,化疗仍在HER2低表达mBC治疗中占据核心地位1。在HR阳性患者中,只有约三分之二的患者在基线LOT前接受过内分泌治疗,后续仍以化疗为主1。这偏离了当前临床指南的推荐,即除非存在内脏危象,HR阳性mBC应优先并连续使用多线内分泌治疗(尤其是联合CDK4/6抑制剂)。这种差距可能源于研究入组时间跨度大(研究前期CDK4/6抑制剂还未获批)、患者群体中可能包含更多高肿瘤负荷(初诊Ⅳ期比例较高)或内分泌耐药患者,以及医生偏好等因素1。
本研究观察到的生存结局(总体中位rwOS 15.8个月)与DESTINY-Breast04研究中化疗组的结果(总体中位OS 16.8个月)数据上存在相似,但低于同试验中T-DXd治疗组的结果(HR阳性患者中位OS 23.9个月;HR阴性患者18.2个月)1,提示真实世界中化疗经治HER2低表达mBC患者面临较差预后,尤其是HR阴性患者(rwOS 11.1个月),以化疗为主的后续治疗效果有限,亟需更有效的治疗方案1。T-DXd等新型靶向药物的获批有望改变这类患者的治疗格局,成为临床中重要的治疗选择。
本研究的优势在于大规模的患者队列和较长的随访期1,使得结果具有较好的代表性。其局限性则包括真实世界回顾性研究固有的问题(如缺乏随机化和潜在的偏倚)、治疗线序算法未纳入疾病进展以及治疗中断的具体原因、数据库中患者记录可能不够完整、长达十余年的研究期内治疗标准发生了显著变化(如CDK4/6抑制剂的获批)等1,导致患者特征和治疗模式存在异质性。
总结
本研究基于真实世界数据库,获得了大量数据,进一步丰富了表征HER2低表达mBC患者治疗模式与预后特征的证据体系。真实世界中,既往接受过一线化疗的HER2低表达mBC患者,其治疗结局和生存状况不够理想,当前临床仅依靠化疗方案对其进行治疗是不足的。而近期靶向治疗领域的相关进展,或许将成为满足这类患者治疗需求的关键,为该人群提供更精准、更有效的治疗选择。
参考文献:
1.Modi S, et al. Treatment patterns and outcomes in HER2-low metastatic breast cancer patients previously treated with chemotherapy: a US real-world cohort study. Breast Cancer Res Treat. 2025 Jun;211(2):351-362.
审批编号:CN-177817
有效期至:2027-02-05
本文由阿斯利康提供,仅供医疗卫生专业人士参考,不可用于推广目的。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)