前言:
在临床实践中,约15%至20%的
然而,传统的评估方法不仅耗时耗力,而且存在高度的观察者间变异性1。随着科技水平的发展,数字病理学与人工智能(AI)作为极具潜力的工具脱颖而出,有望通过深度学习等技术为HER2 IHC评分提供更客观、精准的量化标准。在此背景下,一项研究通过系统评价与荟萃分析,评估AI在HER2 IHC评分中的诊断效能,以精准筛选T-DXd的适用人群,为解决传统评分主观差异等难题提供数字化方案1。
研究方法与目的
研究人员系统检索了MEDLINE、EMBASE、Scopus和Web of Science数据库,检索时间跨度从各数据库建库起至2024年5月3日,检索词涵盖“人工智能”、“机器学习”、“深度学习”、“乳腺癌”及“HER2”等关键词1。研究纳入了使用原发性或转移性乳腺癌数字全切片图像(WSI)、以AI算法性能作为评估指标、以病理医师视觉评分作为金标准参考、提供足够的原始数据以构建2×2列联表(将AI的预测结果与病理医师的“金标准”结论进行横纵交叉对比,形成真阳性、假阳性、真阴性、假阴性四个关键指标)的文章,排除了无法分离IHC 0和1+评分、使用H&E染色、动物组织、多组学方法等研究,以及非原著文章(如综述、会议摘要等),并采用双变量随机效应模型评估AI评估HER2状态的综合灵敏度、特异性及曲线下面积(AUC),以校正研究间的异质性并评估其综合诊断效能1。研究的主要目的是通过系统评价与荟萃分析,评估AI在识别HER2评分(1+/2+/3+ vs. 0)以明确T-DXd治疗可行性方面的表现1。
研究结果
经筛选后,本次研究共纳入13项研究,涉及25个列联表,涵盖1285个病例、168张WSI及24626个切片图像块1。为评估AI在筛选T-DXd适用人群中的诊断效能,研究将阳性阈值设定为IHC 1+、2+或3+,阴性结果设定为0。结果显示,此时AI的综合敏感度达0.97(95% CI 0.96–0.98),这意味着在100名符合T-DXd治疗条件的HER2低表达/阳性患者中,AI能准确识别出97人,仅有3人被漏诊;而0.82(95% CI 0.73–0.88)的综合特异性提示,在100名原本不符合治疗条件的患者(IHC 0)中,有18人会被AI错误地判定为阳性并可能接受不必要的治疗。此外,AI的AUC达0.98(95% CI 0.96–0.99),展现出极高的诊断效能。
表1 纳入的13项研究特征分析1
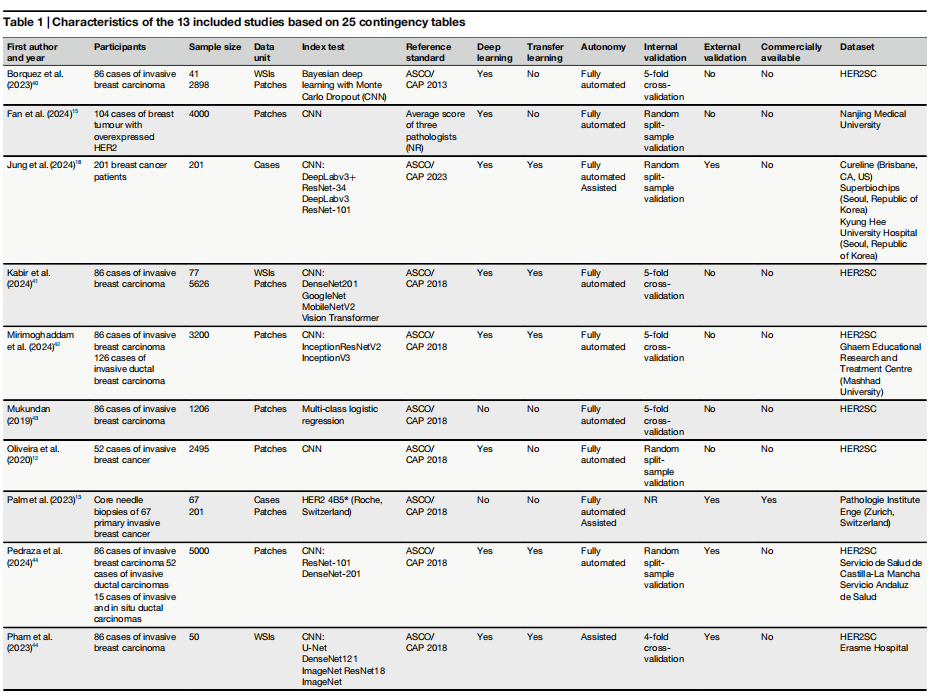
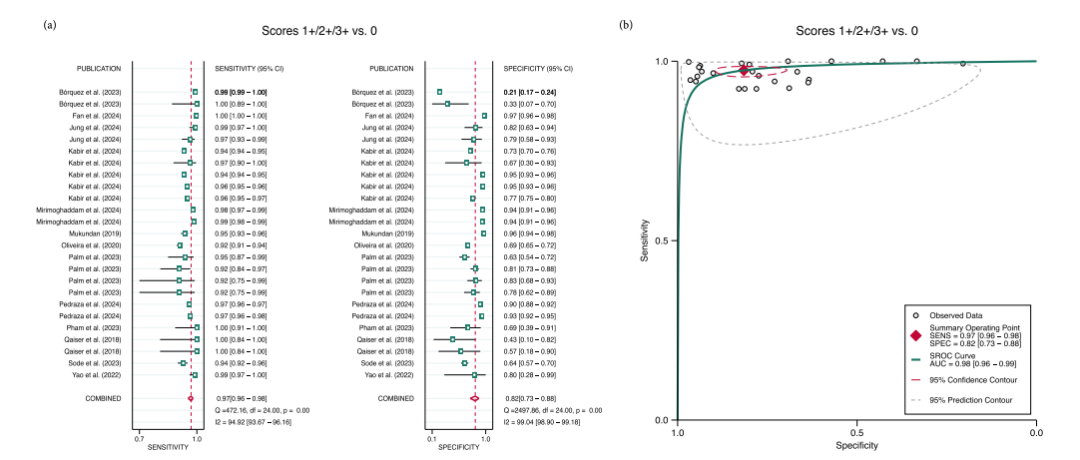
图1 AI在识别IHC评分中的综合性能表现1
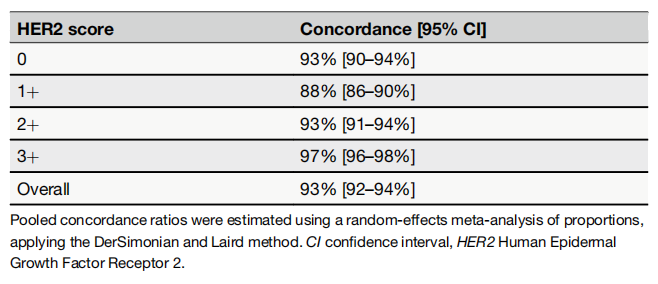
研究发现,随着HER2评分的升高,AI的表现也显著提升1。
表现近乎完美,综合灵敏度为0.97,综合特异性为0.99,AUC为1.00,与病理医师的一致性最高(97%)1。
表现稳健,综合灵敏度为0.89,综合特异性为0.96,AUC为0.981。
表现相对最弱,综合灵敏度下降至0.69,特异性为0.94,AUC为0.92。热图显示,AI对1+的错误预测大多偏向于评分01。
此外,荟萃分析结果揭示了影响AI表现的关键因素。其一,使用深度学习技术的AI灵敏度显著更高(0.98 vs. 0.94)1。其二,样本量大于761的研究(0.88)与使用图像块作为数据单位的研究(0.87)表现出更高的特异性,而以WSI/病例为单位或样本量较小的研究特异性较低(0.70)1。其三,经过外部验证并使用市售模型的研究灵敏度较低,这可能反映了样本异质性对模型泛化能力的挑战1。
研究结论
本研究通过大样本荟萃分析证实,AI在乳腺癌HER2 IHC评分中具有显著优势,可协助识别T-DXd适用人群。AI与病理医师的HER2评分一致性达到93%,在数字病理诊断中已具备与病理医师视觉评分相当的能力,AI或可降低漏诊率,让更多患者有机会接受T-DXd1。但也有部分人可能被AI错误归类为HER2低表达并接受T-DXd治疗,这种“过度治疗”的风险同样不容忽视1。
表2 不同HER2评分下AI与病例医生评估结果的一致性1
此外,本研究也存在若干局限性。首先,研究者排除了合并报告0/1+评分或未提供完整性能数据的研究,这可能对综合指标造成影响1。其次,纳入研究间存在明显的统计学异质性,且部分研究显示较高的偏倚风险1。同时,由于一些研究未充分报告样本的关键特征(如肿瘤浸润性、取材方式[活检与切除]、原发或转移状态),本研究结果难以外推至这些特征不同的其他样本1。
目前的AI模型在识别IHC 1+(微弱染色)时仍面临挑战,而随着DESTINY-Breast06试验对T-DXd治疗HER2超低表达(IHC 0,存在细胞膜染色)生存获益的证实,未来的AI模型需要跳出传统的四级评分系统,针对染色强度和比例提供更精确的连续量化,以适应不断演进的乳腺癌精准治疗需求1。
综上所述,AI在乳腺癌HER2状态评估中已展现出卓越的潜力。尽管在IHC 0-1+的细微区分上仍需优化,但其在提高病理诊断一致性和效率方面的作用毋庸置疑。随着深度学习技术的进一步发展和外部验证流程的标准化,AI有望成为乳腺癌精准医疗不可或缺的组成部分。
参考资料
1. Albuquerque DAN, et al. Systematic review and meta-analysis of artificial intelligence in classifying HER2 status in breast cancer immunohistochemistry. NPJ Digit Med. 2025 Mar 6;8(1):144.
2. Modi S, et al. Trastuzumab Deruxtecan in Previously Treated HER2-Low Advanced Breast Cancer. N Engl J Med. 2022 Jul 7;387(1):9-20.
审批编号:CN-177816
有效期至:2027/1/26
本文由阿斯利康提供,仅供医疗卫生专业人士参考,不可用于推广目的。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)