
在这样的背景下,更加可及的检测方式不断被探索。从血液标志物的快速发展,到近年来对唾液这一体液的重新关注,研究者试图寻找一种兼具准确性与可推广性的解决方案。唾液作为一种获取便捷、几乎无创的样本来源,在多个疾病领域已有应用基础,其在阿尔茨海默病中的潜力也逐渐进入研究视野。
但与其“理想属性”相比,现实中的研究结果却呈现出明显的不一致性。这种差异,并不只是简单的“效果好或不好”,而更像是一个尚未被真正校准的系统。
从生物学路径来看,唾液并非孤立存在。其成分主要来源于血液,通过腺体分泌形成,因此理论上,脑内病理相关蛋白可经“脑—血—唾液”路径进入唾液。这一间接通路,为利用唾液检测中枢神经系统疾病提供了可能。
与血液相比,唾液的优势十分明确。采集过程无需穿刺,不增加患者负担,且易于重复采样,这对于疾病监测尤其重要。在基层医疗或资源受限地区,这种检测方式也具有潜在现实意义。
但与此同时,唾液的“可变性”同样不容忽视。其成分易受口腔环境、进食状态、唾液分泌量以及全身状况影响。尤其在老年群体中,唾液分泌减少较为常见,这种生理变化本身就可能对检测结果产生干扰。
更关键的一点在于,已有研究提示,唾液中阿尔茨海默病核心标志物与血浆或脑脊液水平之间缺乏稳定相关性。这意味着,唾液并不是简单的“替代体液”,其反映的可能是一个经过多重调节后的信号。
该系统综述共纳入18项研究,涉及726名认知正常人群、361名轻度
从结果来看,不同研究之间差异显著。部分标志物在个别研究中表现出较高诊断性能。例如,乳铁蛋白在某些研究中区分AD与正常人群的AUC达到1,Raman光谱分析甚至可达到0.99的诊断准确性。
但与此同时,也有研究未能观察到显著差异。Aβ42、t-tau、NfL等经典标志物,在部分研究中并未表现出区分能力。这种“同一指标,不同结论”的现象,使得整体证据难以整合。
进一步来看,当前研究涉及的标志物种类已经从传统蛋白扩展至多维体系,包括蛋白组学、代谢组学、miRNA以及光谱学方法等。不同技术路径下,研究结果呈现出更大的离散性,这也提示单一标志物可能难以支撑稳定的诊断体系。
在对研究差异进行系统分析后,一个更为关键的结论逐渐清晰:影响结果的主要因素,并不完全来自“检测对象”,而是来自“检测过程”。
研究对前处理环节进行了详细梳理,包括采样前准备、采样时间、采样方式、容器材料、离心条件以及样本保存等多个环节。这些因素在不同研究之间存在显著差异。
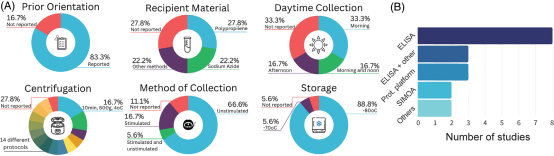
图1 纳入研究中前处理与分析方法的差异
(A)前处理流程,包括采样前准备、采集时间、容器材料、离心方式及储存条件;(B)不同分析方法的分布情况。
具体来看,大多数研究会要求受试者在采样前进行一定准备,例如禁食、漱口或避免吸烟,但具体要求差异较大。采样方式方面,以非刺激性唾液为主,但仍有部分研究采用刺激性采集方式。离心处理更是差异明显,不同研究采用了多达十余种不同参数。
这些差异看似细微,但对于低浓度蛋白的检测而言,其影响可能被显著放大。研究指出,像p-tau、GFAP等低丰度分子,对前处理条件尤为敏感,这也是结果不一致的重要原因之一。
除了前处理,检测技术本身同样影响结果。当前研究中,以ELISA为主流方法,同时也包括单分子检测、质谱分析、Raman光谱及PCR等技术路径。
有意思的是,一些在血液或脑脊液中表现优异的高灵敏度技术,在唾液中并未表现出一致优势。这提示,技术灵敏度的提升,并不能完全抵消样本来源本身的变异。
针对上述问题,已有研究团队尝试提出唾液标志物检测的标准化建议,包括采样前禁食与漱口、统一离心条件以及避免特定采样材料等。
但现实情况是,在本次纳入的研究中,没有任何一项完全符合这一标准流程。这一事实本身,就解释了为何不同研究之间难以获得一致结论。
标准化缺失带来的直接后果,是研究结果之间无法横向比较,也难以形成可推广的证据体系。这一点,与早期血液标志物发展阶段的情况具有一定相似性。
综合现有证据,唾液标志物在阿尔茨海默病中的应用前景仍然存在。一方面,其无创、便捷的特点,使其在筛查与长期监测中具有天然优势;另一方面,当前证据的不稳定性,也提示其尚未具备进入临床常规应用的条件。
未来研究的关键,可能不再仅仅是寻找新的标志物,而是建立统一的采样与检测体系,在此基础上重新评估其诊断价值。
从理论上看,唾液为阿尔茨海默病诊断提供了一种极具吸引力的路径。但从现实证据来看,这一路径仍处于早期阶段。
当前最大的限制,并不在于是否存在有效标志物,而在于检测流程的不一致性。当这一问题得到解决之后,唾液标志物的真实潜力,才有可能被准确评估。
对于神经科临床而言,这一方向值得持续关注,但其真正进入临床实践,仍需更多高质量、标准化研究的支撑。
参考文献:Borelli P V, Machado L, Carello‐Collar G, et al. Diagnostic performance of salivary markers of Alzheimer's disease: A systematic review[J]. Alzheimer's & Dementia, 2026, 22(4): e71248.