李新悦1 马帅2 马俊杰1 胡哲1 李冰倩3 姚远1 徐文嵩4△ 王列1△
(1 辽宁中医药大学,沈阳 110847;2 沈阳市第七人民医院神经内科,沈阳 110000;3 辽宁中医药大学杏林学院,沈阳 110135;4 辽宁中医药大学附属医院骨一科,沈阳 110032)

肌筋膜疼痛综合征 (MPS) 是一种常见的慢性疼痛性疾病,成年人群患病率高且多伴功能障碍。针刺作为安全有效的非药物疗法,可显著改善病人疼痛症状及生活质量。目前针刺干预 MPS 机制研究的综述较少,本文基于穴位敏化理论和 MPS 病理基础,系统总结针刺痛敏穴的镇痛作用:通过抑制致痛介质释放调控炎症-免疫应答、修复下行抑制功能以阻断“外周-中枢”敏化级联、协同调节神经传导通路逆转疼痛病理进程,以期为临床精准治疗提供循证依据。
肌筋膜疼痛综合征 (MPS) 是以肌肉及筋膜组织的局部疼痛及远端牵涉痛为特征的慢性疼痛性疾病。研究显示,普通人群中MPS终生患病率为74%~85%,高发于长期体力劳动、久坐及高工作压力人群,对个人生活功能、情绪健康及社会医疗资源造成沉重负担。目前,MPS的临床治疗仍以非甾体抗炎药、局部麻醉药、糖皮质激素注射以及肉毒毒素注射等为主要手段。这些方法虽具有一定的镇痛效果,但不良反应不容忽视,限制了其长期应用的可行性。因此,临床亟须寻找疗效明确且安全性更高的替代或联合治疗策略。
针刺治疗基于中医整体观念与辨证论治原则,通过调和气血阴阳,强调“治病必求于本”,在慢性肌肉骨骼疼痛管理中日益受到关注。针刺的作用机制与肌筋膜疼痛激痛点 (MTrPs) 的病理生理特征具有高度相关性。MTrPs被视为MPS的核心病因学标志,表现为骨骼肌紧绷带 (TB) 内的异常收缩结节,引发局部及牵涉性痛觉过敏。近年来,“痛敏穴”概念进一步将传统针刺理论与现代疼痛医学相联系。痛敏穴指某些特定穴位在反复刺激后可进入敏感状态,引起疼痛感知的增强或减弱。研究表明,痛敏穴与激痛点在解剖分布、临床表征及生理反应方面存在显著重叠,痛敏穴敏化后的区域与 MTrPs 的定位高度一致,二者均伴随(如条索状结节等)局部组织形态改变,可同属于形态学敏化范畴。在治疗层面上,激痛点的“灭活”与穴位针刺或按压所诱导的“痛可解”效应表现出临床与机制上的相似性。


穴位,又称腧穴,是人体气血输注于体表的特殊部位。以局部压痛或其他反应点来作为针刺部位的一类穴位称为阿是穴。其可以理解为穴位敏化理论的古代记载。
穴位敏化是指穴位从生理的“静息态”转变为病理的“激活态”,机体在病理过程中通过神经源性牵涉反应诱发体表对应部位产生感觉异变,穴位处会出现形态及功能状态的变化,如电敏化、光敏化、热敏化、痛敏化、声敏化等。《灵枢·背腧》谓之“欲得而验之,按其处,应在中而痛解,乃其腧也”。通过“验之”产生感觉变化而定位腧穴之所在,说明穴位是动态变化的。穴位痛敏是敏化穴位最普遍、最易于探查的一种现象,痛敏穴为广义上阿是穴的具体分支,具体是指机体在疾病状态时,相关经脉循行部位或局部腧穴表现出痛阈值的降低和对疼痛敏感性的升高,使得腧穴或局部出现“小刺激、大效应”的表现。
(1)外周敏化机制:
C伤害感受器激活与神经源性炎症(见图1)。神经源性炎症是穴位致敏的重要病理特征,由 C 伤害性感受器介导的轴突反射和背根反射所引发。C 伤害感受器通过无髓鞘 C 纤维传导,与慢性疼痛及继发性痛觉产生密切相关。其亚型沉默型伤害感受器 (SNs) 在正常状态下对常规刺激无反应,但在组织损伤或炎症时被激活,显著参与痛觉过敏的形成。
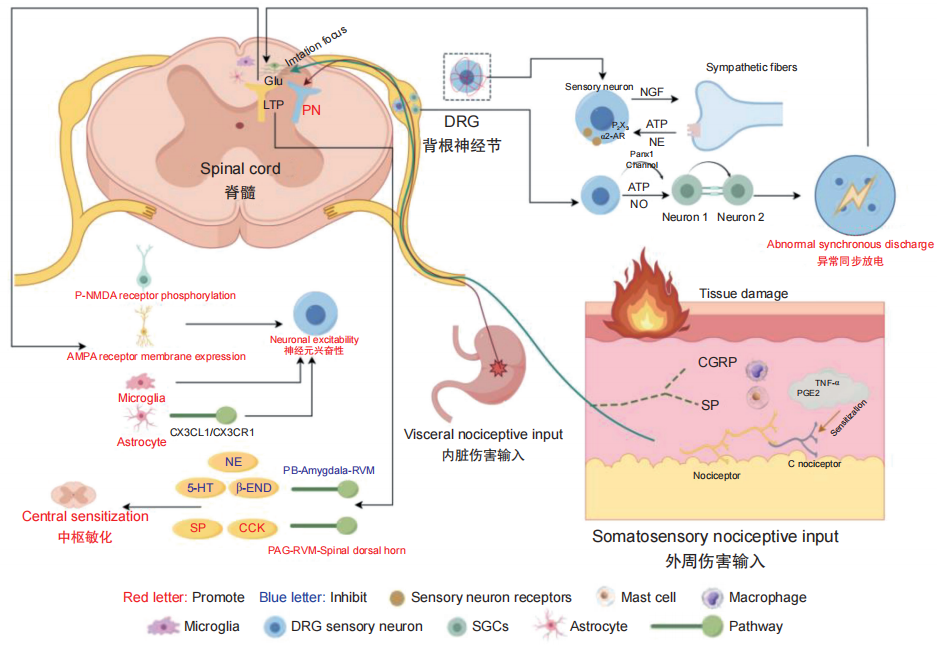
图1 穴位敏化的神经免疫轴:从外周致敏到中枢可塑的动态演化
LTP:长时程增强;PN:伤害性神经元;GLU:谷氨酸;NE:去甲肾上腺素;SP:P物质;CGRP:降钙素基因相关肽;NGF:神经营养因子;NO:一氧化氮;TNF-α:肿瘤坏死因子-α;PGE2:前列腺素 E2;CX3CL1:C-X3-C motif 趋化因子配体 1;CX3CR1:C-X3-C motif 趋化子受体 1;5-HT:5-羟色胺;β-END:β-内啡肽;CCK:胆囊收缩素;α2-AR:肾上腺素 α2 受体;P2X3:嘌呤能配体门控离子通道 3
组织损伤或炎症刺激可激活伤害感受器,信号经背根神经节 (DRG) 传入脊髓后,背角中间神经元或胶质细胞相应激活,并且信号继而通过同一或邻近感觉神经元的轴突逆向传至外周,促使神经末梢释放神经营养因子 (NGF)、缓激肽、组胺、前列腺素等炎性物质,以及神经肽如降钙素基因相关肽 (CGRP) 与 P 物质 (SP),从而形成“炎性汤”并唤醒沉默的 C 伤害感受器,放大伤害性输入,扩大疼痛信号范围,最终导致穴位区域持续敏化。
(2)中枢敏化机制:
脊髓与 DRG 神经元的可塑性变化(见图1)。DRG 作为连接外周与中枢信号传递的关键枢纽,其敏化机制主要涉及神经元-卫星胶质细胞 (SGCs) 互作及交感神经系统的异常重塑。在炎症或损伤条件下,DRG 神经元释放的三磷酸腺苷 (ATP)和一氧化氮 (NO) 诱导 SGCs 活化,并通过缝隙连接介导促炎分子和电信号扩散,引发 DRG神经元群体异常同步放电,持续向脊髓背角传递异常信号。此类信号增强谷氨酸能突触传递,诱发长时程增强 (LTP) 效应,具体表现为谷氨酸 N-甲基-D-天冬氨酸 (NMDA) 受体磷酸化与 α氨基-3-羟基-5-甲基-4-异恶唑丙酸 (AMPA) 受体膜表达上调。
同时,NGF 驱动交感神经末梢增生包绕感觉神经元,并释放去甲肾上腺素 (NE) 和ATP,激活肾上腺素 α2 受体 (α2-AR) 和嘌呤能配体门控离子通道 3 (P2X3) 受体,从而显著加剧伤害性信息传导。这一系列反应诱发脊髓背角突触可塑性变化,包括动作电位发放频率递增,最终导致穴位敏化。脊髓小胶质细胞和星形胶质细胞被炎性信号激活后释放更多促炎介质,形成正反馈环路,进一步加剧中枢敏化。
此外,慢性异常输入同时导致脑干下行抑制通路功能衰减与臂旁核等下行易化通路亢进,共同促成痛觉信号的调控失衡。特别值得注意的是,内脏与躯体来源的 C 类传入纤维可在脊髓背角 I 层会聚于同一投射神经元,内脏疼痛“激惹灶”可显著强化体表信号的传递,这不仅为牵涉痛发生提供机制解释,也突显脊髓背角在中枢敏化与疼痛维持中的核心作用。
(3)神经免疫串扰介导炎性疼痛的发生和维持:
穴位敏化本质上是局部神经免疫网络失衡的病理表现,其发生取决于促炎因子与抗炎因子的动态平衡状态。研究表明,巨噬细胞和中性粒细胞在损伤部位的浸润动态与疼痛超敏反应高度同步,其中血小板反应蛋白-1 (TSP-1) 起关键调控作用。TSP-1 通过与感觉神经元表面 CD47 受体结合,抑制前列腺素 E2 (PGE2) 诱导的瞬时受体电位香草酸亚型 1 (TRPV1)通道敏化,从而缓解疼痛传导。该通路活性直接影响穴位敏化程度:TSP-1不足时PGE2等促炎介质主导微环境,加剧敏化;而 TSP-1/CD47信号激活则可减轻敏化。值得注意的是,TSP-1在DRG中高表达于痛觉相关神经元(如PEP1、PEP2、NP),而在低阈值机械感受器(如NF1、NF2)中表达较低,这一分布特征解释了穴位敏化为何主要表现为痛觉过敏而非触觉异常。
在炎症状态下,DRG 神经元还上调再生胰岛衍生蛋白 3β (Reg3β),作为趋化因子招募血液单核细胞浸润 DRG,并促其分化为 M1 样促炎巨噬细胞,其释放肿瘤坏死因子-α (TNF-α)直接增强神经元 TRPV1 通道活性,进一步加剧痛觉敏化。同时,泛连接蛋白 1 (Panx1) 通过激活 Wnt/β-catenin 信号通路促进 DRG 神经元突触可塑性分化,并增强电压门控钠/钙通道活性以提高神经元兴奋性。炎症条件下,Panx1 介导的 ATP 释放可激活邻近细胞 P2X/P2Y 受体,形成“ATP-免疫激活-神经元敏化”的正反馈循环,持续驱动穴位敏化进程。TSP-1/CD47 与 Panx1-ATP 信号共同构成神经免疫交互调控的分子基础,为精准干预穴位敏化提供了潜在靶点。
(4)表观遗传修饰调控基因表达的可遗传性变化:
环状 RNA (circular RNAs, circRNAs) 作为一类新型非编码 RNA,通过竞争性内源性 RNA (ceRNA) 机制介导表观遗传调控,在疼痛与中枢敏化中发挥核心作用。其病理调控网络主要包括:通过吸附特定 miRNA(如脊髓 circRNA-Filip1l结合miR-1224)解除靶基因抑制,上调泛素蛋白连接酶E3组分N-识别蛋白5 (UBR5) 表达,增强 DRG 神经元对炎症刺激的敏感性,调控单核细胞趋化蛋白CCL2等因子的转录,促进巨噬细胞和中性粒细胞浸润,形成炎症-痛觉自我维持环路;通过增强TNF-α、IL-6等促炎因子表达放大神经元反应,并与TRPV1、NMDA受体相互作用调节其活性,促进痛觉过敏,激活MAPK/ERK通路,增强脊髓神经元兴奋性,同时通过调控胶质细胞活性释放促炎因子,共同加剧中枢敏化。慢性痛症相关circRNA(如 circKcnk9)的表达水平与临床症状严重程度显著相关,提示其兼具生物标志物价值及治疗靶点潜力,为慢性疼痛及中枢敏化的干预提供新策略。


MTrPs是MPS的核心病理特征,由美国医师Janet Travell和David Simons博士于1942年首先提出,其表现为骨骼肌内可触及的疼痛结节和紧绷肌纤维带,其形成机制复杂,涉及外周组织病理改变、神经系统调控异常及全身代谢失衡等(见图2)。
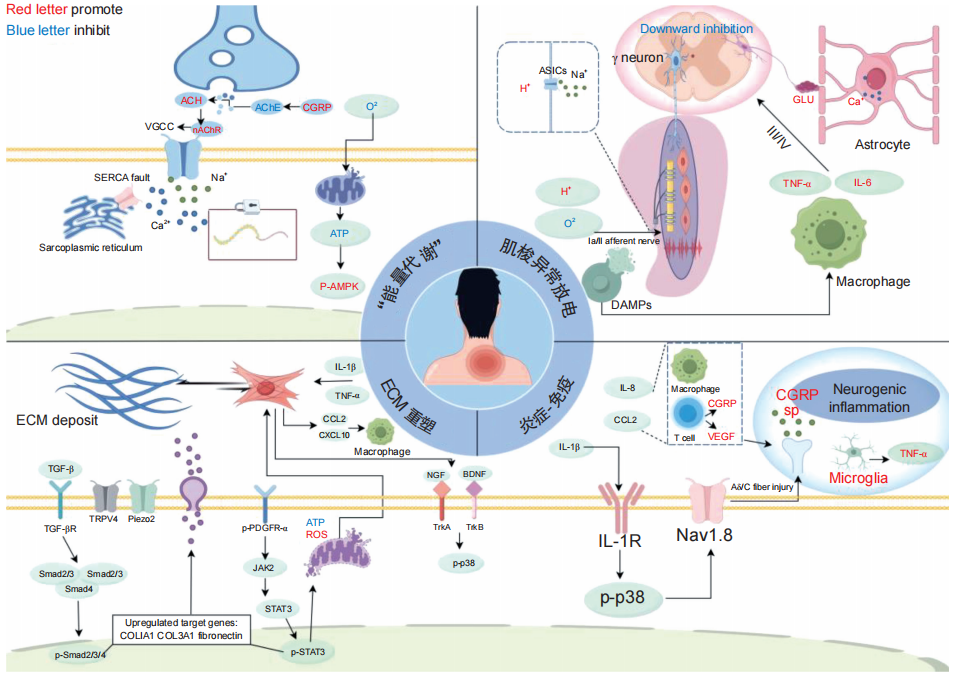
图2 肌筋膜疼痛综合征病理机制
ACH:乙酰胆碱;VGCC:电压门控钙通道;AChE:乙酰胆碱酯酶;p-AMPK:磷酸化 AMP 蛋白激酶;ASICs:酸敏感离子通道;DAMPs:损伤相关分子模式;GLU :谷氨酸;VEGF:血管内皮生长因子;CCL2:趋化因子配体 2 ;CXCL10:C-X-C 基序趋化因子配体 10;NGF:神经生长因子;BDNF:脑源性神经营养因子;Piezo2:压电离子通道蛋白2;TRPV4:瞬时受体电位香草素亚型 4;PDGFR-α:血小板衍生生长因子受体-α;TGF-β:转化生长因子-β
在 MPS 的初始阶段,骨骼肌过度负荷或微损伤是常见的触发因素。该学说核心在于运动终板功能障碍引发的“能量危机”。正常生理状态下,乙酰胆碱 (Ach) 在神经肌肉接头的释放受到严格调控。在病理状态下,运动终板区出现ACh 的病理性泄漏,同时 CGRP 介导了对乙酰胆碱酯酶的抑制,导致ACh异常堆积,ACh的过度积累持续激活烟碱型受体,引起肌细胞膜持续性去极化,这不仅直接导致肌动蛋白-肌球蛋白横桥异常锁定、形成收缩结节,更触发肌浆网中钙离子的大量释放。
与此同时,肌浆网钙泵 (SERCA) 功能受损,造成胞质内Ca2+浓度显著升高。另一方面,由于微循环障碍导致组织缺氧,进一步抑制线粒体的氧化磷酸化过程,致使ATP合成效率急剧下降乃至耗竭。ATP缺乏可进一步削弱SERCA及钠钾泵的功能,加重钙离子稳态失衡,形成正反馈。局部环境中堆积的代谢废物(如K+、H+及ATP本身)持续刺激伤害性感受器,这些异常信号传入中枢后,通过兴奋γ运动神经元反馈性地加剧肌肉收缩,最终构筑成一个完整的“收缩-缺氧-ATP耗竭”恶性循环,成为MTrPs形成和疼痛维持的核心机制。
肌梭由大型有髓鞘初级传入纤维 (Ia) 和 II 类传入纤维支配,这些传入神经在正常情况下传递肌肉长度和拉伸速度的信息,而疼痛通常由小型无髓鞘的III和IV类传入神经(伤害感受器)传递。肌肉损伤诱发的缺血缺氧和局部酸中毒,可直接激活酸敏感离子通道 (ASICs),兴奋肌梭初级传入末梢。更为重要的是,由能量代谢障碍和微损伤释放的损伤相关分子模式 (DAMPs) 和ATP,通过激活巨噬细胞释放促炎因子,协同星形胶质细胞Ca2+依赖性谷氨酸释放,交叉激活 III/IV 类伤害性传入通路。持续性疼痛信号导致脊髓中枢敏化与下行抑制通路功能减弱,进而通过交感-运动耦联促进γ神经元放电,迫使肌梭内肌纤维持续收缩。该过程加重局部缺血,引起线粒体功能障碍及ATP耗竭,最终导致膜电位异常 (PACS/PIPS),构成“缺血缺氧-异常放电-肌梭收缩”的自我维持环路。
炎症免疫反应是对前述“能量危机”与“组织损伤”的适应性应答,并在疼痛信号放大中起核心作用。MPS 导致持续的外周伤害输入,在 MTrPs 微环境中检测到高浓度的炎症标志物,如白细胞介素-1β (IL-1β)、白细胞介素-8 (IL-8) 和趋化因子配体2 (CCL2)。促炎细胞因子通过直接作用于神经元上的特异性受体(如 IL-1R),降低其兴奋阈值,并且激活疼痛传导神经元上的伤害性感受器,诱导神经元去极化,从而传导疼痛信号至中枢神经系统。此外,IL-8和CCL2等细胞因子可以招募巨噬细胞和T细胞等免疫细胞的聚集。巨噬细胞通过释放更多促炎细胞因子进一步增强局部的炎症反应,活化的T细胞上调血管内皮生长因子 (VEGF) 及CGRP等表达,加剧神经炎症反应及神经递质失衡,进一步刺激周围的疼痛感受器,形成恶性循环。
MPS的迁延不愈与肌肉组织的病理性重塑密切相关。这一过程源于炎症、机械应力及异常收缩等长期后果。在MTrPs微环境中,持续的炎症因子,如转化生长因子-β (TGF-β) 与机械应力协同驱动筋膜成纤维细胞向肌成纤维细胞的转化。此过程涉及多条关键信号通路的激活,包括 PDGFR-α/JAK2/STAT3与TGF-β/Smad的协同作用。活化的肌成纤维细胞大量合成I/III型胶原及纤连蛋白,导致细胞外基质 (ECM) 异常沉积与硬化。
僵化的ECM通过两重机制维持疼痛:一方面直接物理压迫神经末梢,另一方面持续激活机械敏感离子通道(如Piezo2、TRPV4),产生伤害信号,使疼痛在初始炎症消退后仍得以延续。此外,活化的成纤维细胞本身也分泌趋化因子(如 CCL2、CXCL10)与神经营养因子 (NGF/BDNF),不仅能够募集体液免疫细胞以放大炎症,还能直接与神经元相互作用,降低痛阈并促进中枢敏化。上述病理性 ECM 重塑与肌成纤维细胞活化共同构成“肌肉纤维化”的关键环节,成为维持慢性疼痛与功能障碍的核心机制之一。


针刺痛敏穴干预MPS的本质是以“通”治“痛”。《针灸甲乙经》:“针灸者,所以通经脉,调气血,使营卫流行,阴阳相合,而邪气自除。”基于此,针刺通过调节疼痛介质、影响疼痛传递与处理过程,有效缓解MPS的外周与中枢敏化。这一多靶点整合机制,既深刻体现了中医“通经络、调气血”的核心理论,也与现代医学揭示的MPS“敏化”病理本质深度呼应(见图3)。
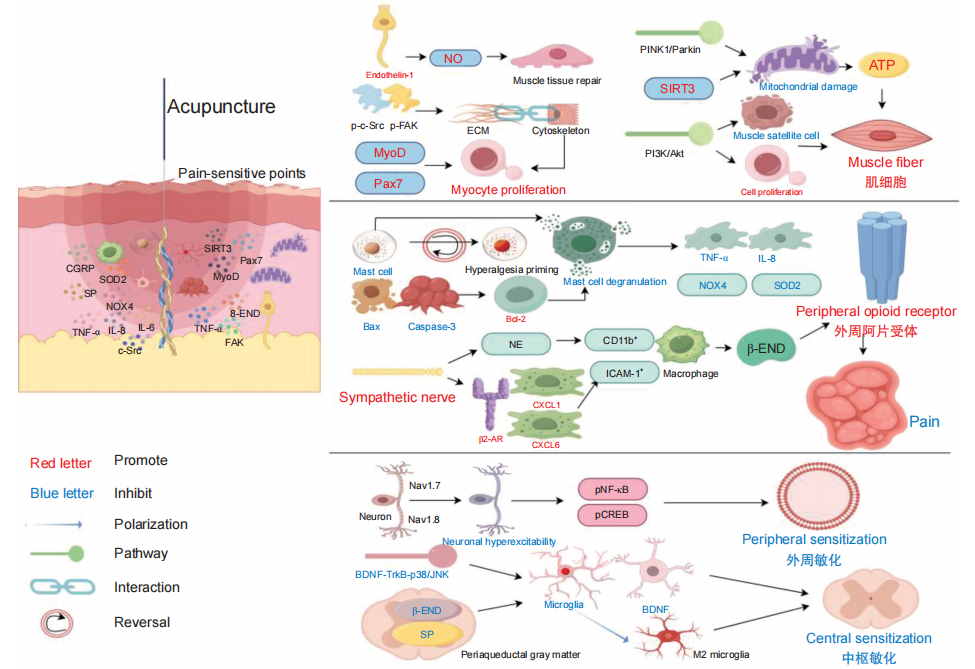
图3 针刺痛敏穴治疗肌筋膜疼痛综合征的作用机制
P-FAK:磷酸化黏着斑激酶;P-c-Src:磷酸化原癌基因酪氨酸蛋白激酶;MyoD:肌源性分化因子;Pax7:配对盒转录因子 7;ECM:细胞外基质;SIRT3:去乙酰化酶 3;Bax:Bcl-2相关X蛋白;Caspase-3:胱天蛋白酶-3;Bcl-2:B 细胞淋巴瘤-2蛋白;NOX4:NADPH氧化酶4;SOD2:超氧化物歧化酶 2;β2-AR:β2-去甲肾上腺素能受体;CXCL1:C-X-C基序趋化因子配体 1;CXCL6:C-X-C基序趋化因子配体6;β-END:β-内啡肽
(1)针刺痛敏穴应对“能量危机”机制:
在MPS 的病理过程中,“能量危机”表现为钙离子超载、ATP 耗竭以及运动终板 ACh 异常释放,最终导致肌纤维萎缩与胶原沉积。在这一背景下,针刺痛敏穴通过多信号通路协同作用,有效缓解疼痛并促进组织修复。
电针刺激可下调内皮素-1 (ET-1) 表达,提升NO水平,从而改善局部微循环灌注,缓解组织缺血与缺氧状态,为后续修复创造有利条件。随后,针刺通过激活PINK1/Parkin介导的线粒体自噬及PI3K/Akt信号通路,恢复ATP合成,逆转钠钾泵和钙泵功能障碍,从根本上改善能量代谢。此外,银质针热疗能够上调SIRT3蛋白表达,修复线粒体功能并提高痛阈,进一步增强治疗效果。针刺联合低频电刺激则通过激活肌卫星细胞(上调Pax7/MyoD),促进肌纤维再生与微损伤修复,同时调节筋膜系统的生物张力完整性,缓解肌成纤维细胞网络的机械异常,可观察到MTrPs处肌原纤维排列趋于整齐,挛缩结节减少,肌筋膜及肌纤维结构得到修复,疼痛阈值显著提高。
在分子层面,电针通过促进黏着斑激酶FAK与c-Src的磷酸化,增强细胞骨架-ECM之间的相互作用,缓解局部机械压迫,促进成纤维细胞内应力纤维增厚与黏着斑成熟,提升细胞对机械刺激的适应性,抑制肌筋膜硬化。此外,电针可通过血清信号激活 PI3K/Akt 通路,改善肌卫星细胞的自噬-凋亡平衡,抑制过度自噬,促进其增殖与肌纤维成熟,从而加速损伤修复。
(2)针刺痛敏穴介导外周炎症-免疫-神经调控机制:
在有效改善局部能量代谢和内环境稳态的基础上,针刺痛敏穴的调控效应进一步延伸至更广泛的外周免疫与神经调控层面。
在MTrPs区域,氧化应激 (SOD2、NOX4)、炎症因子 (IL-8、TNF-α)、神经肽 (SP、CGRP) 与生长因子等共同异常表达,形成“炎症-氧化应激-痛觉敏化”轴。电针刺激痛敏穴可通过多途径抑制神经源性炎症:下调促炎与促氧化基因(如 IL-8、TNF-α、NOX4),上调抗氧化酶 SOD2,减轻局部氧化应激;促进巨噬细胞向抗炎表型极化,稳定肥大细胞功能,缓解组织炎症;并通过降低炎症与氧化应激对神经元的刺激,抑制疼痛信号传导。临床随机对照试验进一步证实,针刺能显著降低血清 SP并提升 5-羟色胺 (5-HT) 水平,增强系统镇痛效应。与远端穴位相比,近端痛敏穴在降低血清IL-8及肌肉 SP、CGRP 方面作用更显著。
在神经传导层面,针刺通过下调中枢神经系统的痛觉受体表达以降低痛觉敏化。具体来说,其干预方式能够抑制DRG与体感皮层中的痛觉受体TRPV1及电压门控钠通道 (Nav1.7/Nav1.8) 的表达,并抑制pNF-κB/pCREB信号轴,从而阻断促炎基因转录,遏制外周敏化。与此同时,针刺还通过激活交感神经释放 NE,上调 β2-肾上腺素受体 (β2-AR) 及趋化因子CXCL1/CXCL6,进而募集 ICAM-1+/CD11b+ 免疫细胞至炎症区,并通过其释放的β-内啡肽激活外周阿片受体通路实现镇痛。针刺通过抑制凋亡蛋白Bax/Caspase-3 表达并上调B淋巴细胞瘤-2基因 (Bcl-2),减少其脱颗粒及局部浸润,逆转高痛敏状态 (HP),维持炎症消退微环境。
(3)针刺痛敏穴介导中枢敏化机制:
针对由持续外周敏化所引发的中枢神经系统功能重塑,针刺痛敏穴同样展现出多层次的中枢调控机制。穴位区域富集的肥大细胞在针刺镇痛中扮演关键角色。针刺的机械刺激促使肥大细胞脱颗粒,释放的生物活性物质与神经末梢的特异性空间接触,激活神经-中枢信号传递通路。与此同时,电针通过激活脊髓Aβ纤维,通过门控机制抑制 C 纤维传导,提升局部痛阈。
在慢性疼痛状态下,脊髓背角神经元的 NMDA受体(尤其是NR2B亚基)过度激活,导致谷氨酸能突触传递增强并诱发LTP,在大脑(如前扣带回、岛叶等)区域出现过度激活。电针通过阻断BDNFTrkB-p38/JNK级联反应,减少小胶质细胞的活化与增殖,抑制IL-1β、TNF-α等炎症因子释放,降低胶质细胞活化与 BDNF 分泌,阻断神经元敏化从而抑制疼痛信号持续放大。
此外,针灸还可通过修复下行抑制通路功能障碍发挥镇痛作用:调节中脑导水管周围灰质 (PAG) 和延髓头端内侧区 (RVM) 的5-HT与NE能通路,抑制RVM“ON 细胞”活性并增强“OFF细胞”抑制效应。滞动针疗法可通过抑制PAG区SP表达、促进小胶质细胞向M2表型极化以及下调BDNF,进一步有效缓解中枢敏化。
综上所述,针刺痛敏穴通过多靶点、多层次调控机制缓解 MPS 的症状,其作用包括直接改善局部能量代谢障碍、调节成纤维细胞功能、缓解肌筋膜挛缩、修复线粒体功能及有效抑制炎性因子传递。同时,针刺通过抑制神经炎症反应、协同激活内源性镇痛系统并重塑神经信号传递网络,实现系统性干预:由外周阻断炎性介质释放与神经敏化,在脊髓增强痛觉门控抑制并抑制胶质细胞活化,至中枢重塑疼痛相关脑区活动并修复下行抑制通路功能,最终协同调控疼痛信号传导、神经免疫应答及中枢敏化病理环节。


MPS 属慢性肌肉骨骼疼痛类疾病,中医归为“痹病”“筋痹”范畴,其典型特征MTrPs的形成机制复杂,文献分析显示,痛敏穴与MTrPs具有共同的神经敏化基础。针刺可通过机械松解、神经与免疫系统调节等多重机制发挥疗效。然而,目前临床研究多为小样本单中心试验,缺乏多中心、长时间随访的高质量证据,限制了其临床推广力度。此外,机制研究多为碎片化,对局部机制与整体调控的系统性理解仍缺乏,技术参数的标准化缺失也影响了疗效的可比性。
未来将致力于构建痛敏穴区与MTrPs组合定位模型,结合筋膜力学与经络循行,实现局部解结与远端调气的协同治疗,进行大样本、多中心、分层随机对照试验,结合超声弹性成像、血清生物标志物等客观指标,以及空间转录组学与脑功能成像,阐明“穴位-脊髓-脑”通路的机制。最后,结合中西医优势,将针刺与药物、物理治疗相结合,制订个性化的阶梯式综合治疗方案,以期实现肌筋膜疼痛的系统性、精准性和长效治疗。
信源:李新悦 马帅 马俊杰 胡哲 姚远 李冰倩 王列 徐文嵩.针刺痛敏穴治疗肌筋膜疼痛综合征的研究进[J].中国疼痛医学杂志,2026,32(3):215~223
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)