小麦纤维通过非短链脂肪酸微生物代谢物训练的肠道巨噬细胞缓解结肠炎
Wheat fiber mitigates colitis via non-SCFA microbial metabolite-trained intestinal macrophages
Science Advances
PMID: 41880488 [IF=12.5]
来源:IBD Daily
工业化进程深刻改变了食品生产与膳食结构,导致人群中膳食纤维摄入量普遍下降。流行病学证据表明,膳食纤维摄入不足与
研究采用6周龄C57BL/6小鼠,分别饲喂标准谷物饲料 (GBC)、低纤维饲料 (LF,含5%
➤小麦纤维独立于SCFA、IL-22及FXR通路,显著减轻DSS诱导的结肠炎
为评估小麦纤维对肠道炎症的影响,研究将C57BL/6小鼠从标准谷物饲料 (GBC) 切换至低纤维饲料 (LF,含5%纤维素) 或添加小麦纤维的饲料 (WF,总纤维约15%),1周后给予2.5% DSS饮水诱导结肠炎。结果显示,LF组小鼠结肠炎最为严重,表现为体重显著下降、DAI升高、结肠明显缩短、脾脏肿大及组织病理学评分升高。相比之下,WF组小鼠仅出现轻度结肠炎,其体重下降、DAI评分及结肠缩短程度均显著低于LF组,甚至优于GBC组。进一步检测结肠炎症因子表达发现,WF组小鼠的表达水平显著低于LF组,提示WF具有免疫调节作用。机制探索方面,WF并未提高盲肠丁酸水平,仅轻度升高乙酸;添加抑制SCFA产生的啤酒花β酸不影响WF的保护效果,说明其保护作用不依赖SCFA。同时,WF未诱导IL-22表达,且在FXR基因敲除小鼠中仍能减轻结肠炎,排除了IL-22及FXR通路的参与。综上,WF通过非SCFA、非IL-22、非FXR的机制独立保护小鼠免受DSS诱导的结肠炎。
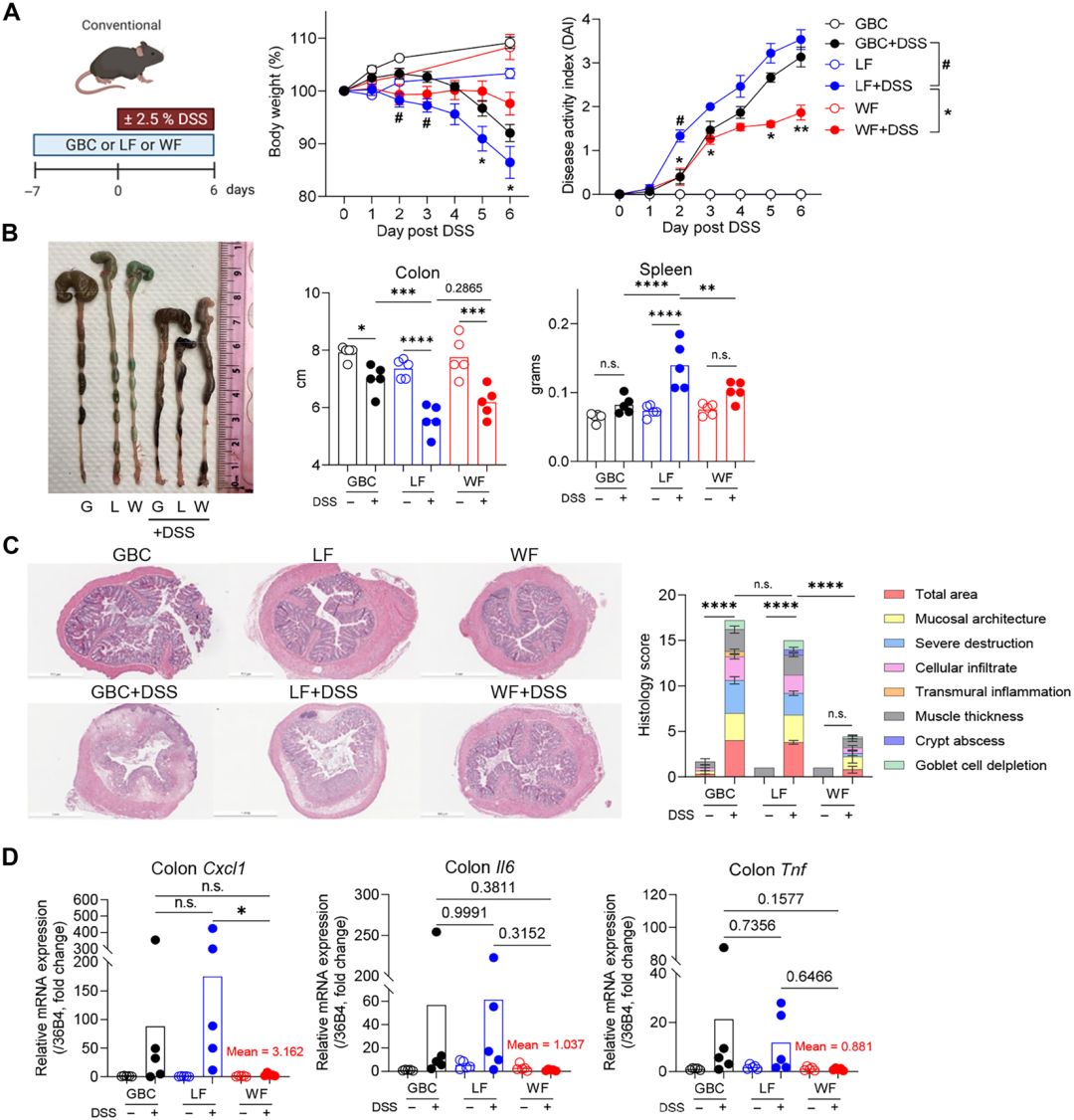
图1WF可保护小鼠免受DSS诱导的结肠炎
➤小麦纤维维持菌群多样性,且B. theta是介导保护作用的关键菌种
为明确菌群是否参与WF的保护作用,研究对小鼠粪便进行16S rRNA测序及qPCR分析。结果显示,LF饮食导致菌群α多样性显著下降、β多样性发生明显偏移,而WF饮食虽未增加总菌量,但有效维持了α多样性,并显著改变菌群组成。在属水平上,WF富集了多种具有碳水化合物代谢能力的细菌,尤其显著维持了B. theta的丰度,同时进一步增加了由LF饮食诱导升高的Akkermansia muciniphila (A. muc)。抗生素清除菌群后,WF对结肠炎的保护作用完全消失,证实其保护依赖于菌群。为进一步验证特定菌种的功能,研究采用限菌 (ASF) 小鼠模型。ASF小鼠本身不携带B. theta或A. muc,WF饮食不能保护其免受DSS结肠炎。当在ASF小鼠中单独定植B. theta后,WF饮食重新恢复了保护作用,表现为体重下降减轻、DAI降低、结肠长度及组织病理学改善;而定植A. muc虽有一定效果,但显著弱于B. theta。此外,B. theta的丰度与膳食纤维摄入呈正相关,进一步支持B. theta是WF发挥抗结肠炎作用的关键介导菌。
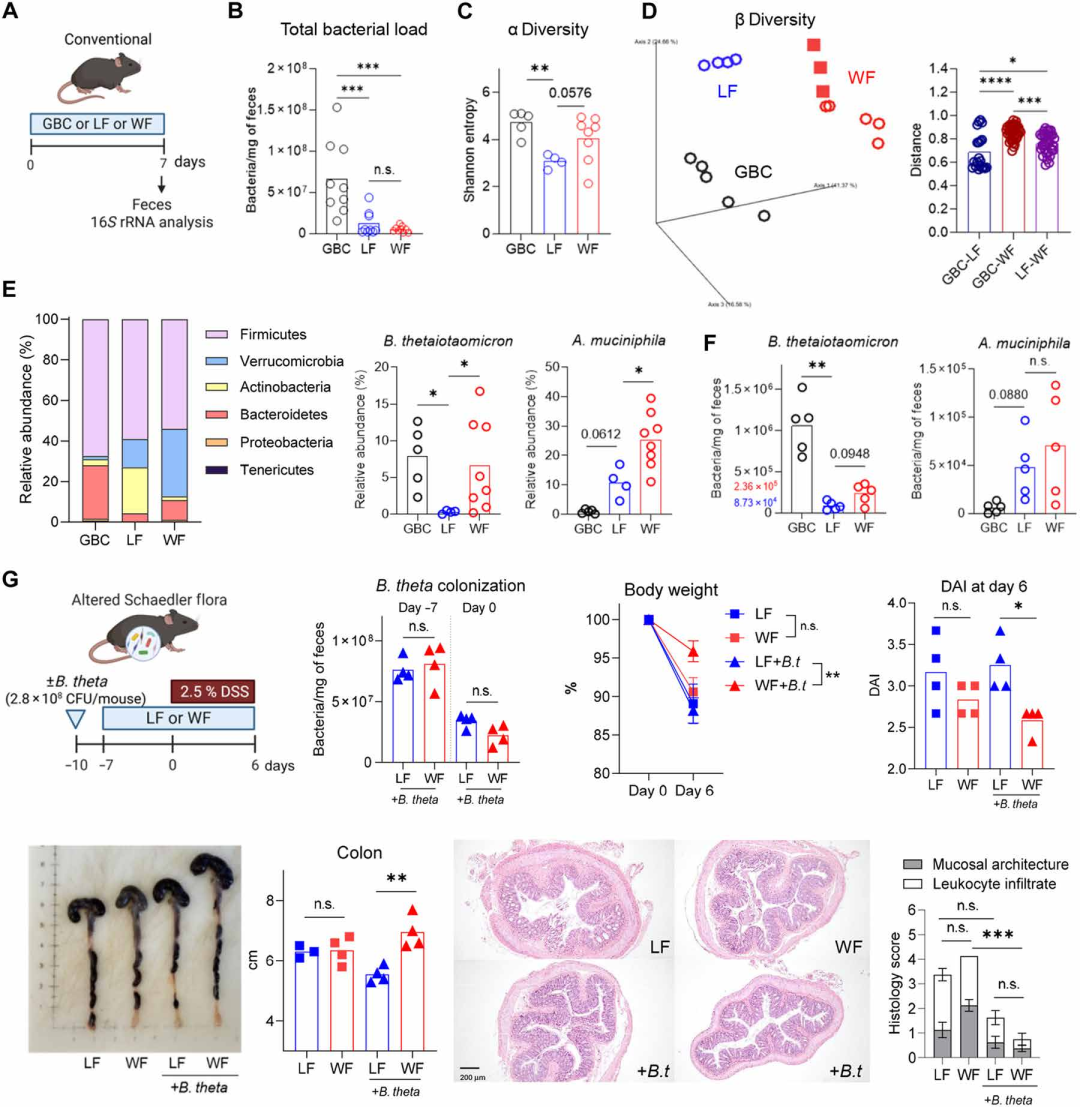
图2WF诱导的肠道菌群多样性对结肠炎保护作用具有必要性,且B. theta足以介导该保护效应
➤小麦纤维通过诱导M2型巨噬细胞极化并重塑其代谢表型发挥保护作用
为探究WF保护作用的细胞机制,研究采用流式细胞术分析结肠固有层免疫细胞。结果显示,在常规小鼠中,WF饮食显著降低了M1型巨噬细胞 (CD86+)、炎性单核细胞、中性粒细胞及嗜酸性粒细胞的绝对数量与比例,同时增加了M2型巨噬细胞 (CD206+) 及CD103+CD11b-树突状细胞的丰度,从而使M1/M2比值显著下降,提示肠道炎症基调向抗炎方向转变。在ASF小鼠中,WF单独不能诱导上述巨噬细胞变化;只有在同时存在WF和B. theta时,M2型巨噬细胞才明显增加,M1/M2比值降低。进一步分离结肠F4/80+巨噬细胞进行代谢分析发现,来自LF喂养小鼠的巨噬细胞表现为高细胞外酸化率 (ECAR),即依赖糖酵解,这是促炎M1型巨噬细胞的代谢特征;而来自WF喂养小鼠的巨噬细胞则表现为高氧消耗率 (OCR),即依赖氧化磷酸化,这与抗炎M2型巨噬细胞一致。当用DSS处理小鼠的粪便或结肠上清刺激巨噬细胞时,WF来源的巨噬细胞仍能维持较高OCR,仅轻度向ECAR偏移,显示其对炎症刺激具有较强的代谢韧性。转录组分析进一步证实,WF可部分逆转LF诱导的巨噬细胞基因表达变化,恢复122个与免疫应答、细胞应激及伤口愈合相关的基因表达,这些基因多参与M1/M2极化调控。
➤小麦纤维驱动的菌群代谢物可直接训练巨噬细胞,过继转移后减轻结肠炎
为验证WF是否通过可溶性代谢物影响巨噬细胞,研究收集LF及WF喂养小鼠的粪便上清 (FS),体外处理BMDM。结果显示,与LF-FS相比,WF-FS处理可显著降低LPS刺激下BMDM的M1/M2比值及IL-6分泌,并诱导代谢表型从糖酵解向氧化磷酸化转变,与体内结肠巨噬细胞变化一致。为进一步证明这些代谢物训练的巨噬细胞具有抗炎功能,研究将LF-FS或WF-FS处理的BMDM (CD45.1+) 经腹腔过继转移至LF饮食的受体小鼠 (CD45.2+),随后进行DSS处理。结果发现,接受WF-FS训练BMDM的小鼠,其体重下降、DAI评分、结肠缩短及组织病理学评分均显著优于接受LF-FS训练BMDM的小鼠。流式检测显示,约10%的过转移植细胞 (CD45.1+) 可在受体结肠中被检出,提示这些巨噬细胞能够归巢至肠道并在炎症环境中存活。上述结果表明,WF通过菌群代谢产生的可溶性代谢物对巨噬细胞进行“训练”,使其获得抗炎表型,并能过继转移以减轻结肠炎。
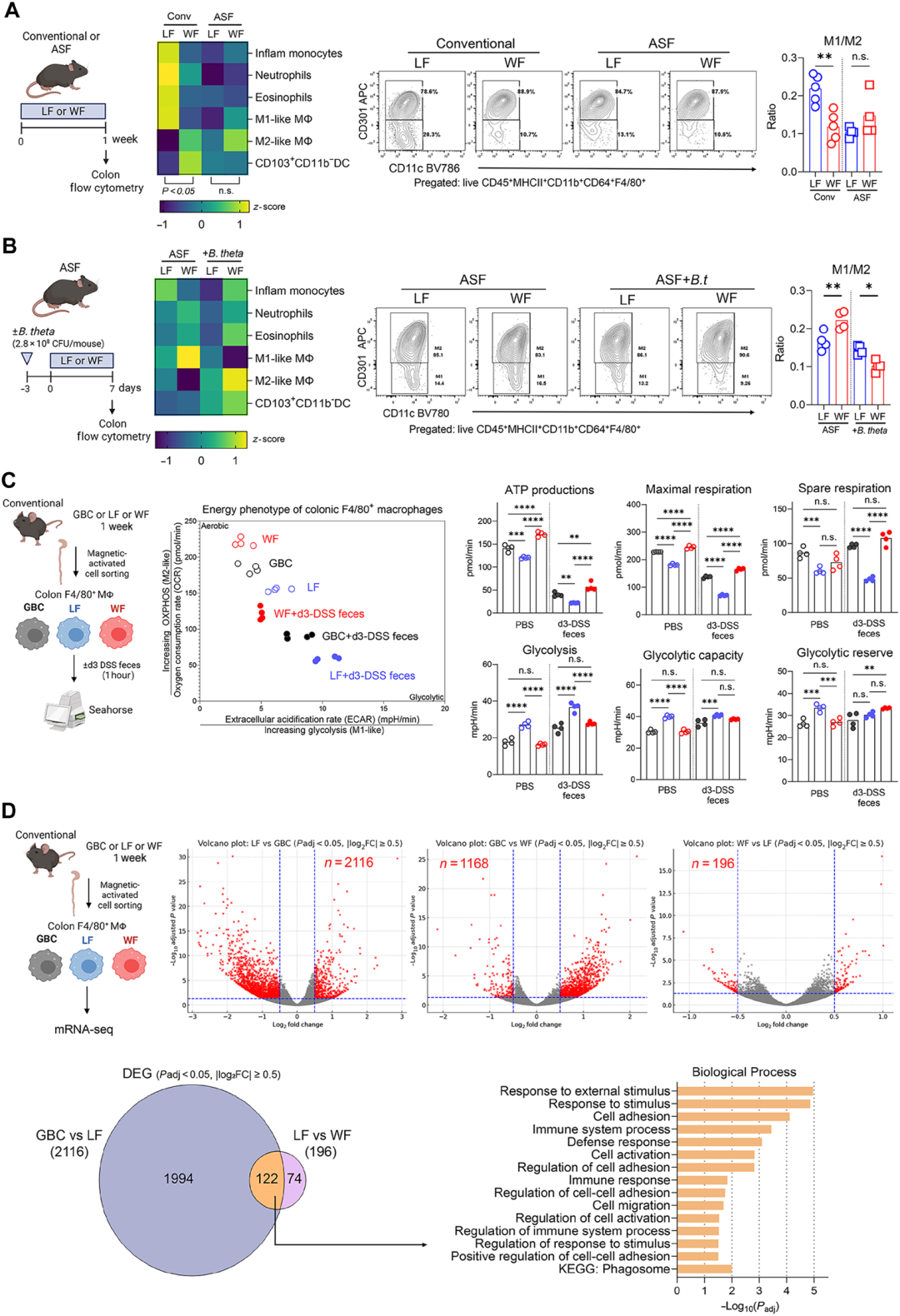
图3B. theta恢复了结肠中与小麦纤维相关、依赖微生物群的巨噬细胞表型
➤异嗪皮啶是WF与B. theta协同产生、训练巨噬细胞的关键代谢物
为鉴定WF-B. theta协同产生的具体代谢物,研究对ASF小鼠 (有无B. theta定植、饲喂LF或WF) 的粪上清进行非靶向代谢组学分析。主坐标分析显示,WF与B. theta共同存在时,代谢谱发生显著偏移。通过差异筛选,共发现9种代谢物仅在WF+B. theta组中显著升高,排除亲水性无已知转运体的物质后,剩余7种候选物。其中,异嗪皮啶和N,N-二甲基鞘
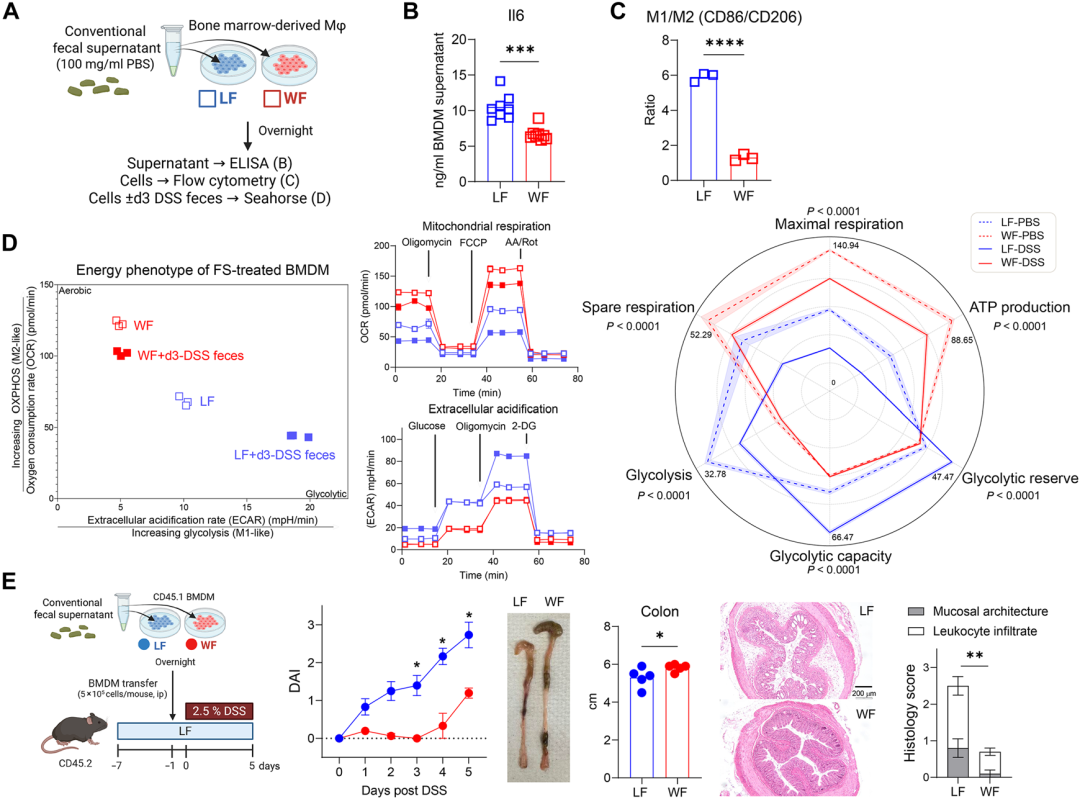
图4小麦纤维来源的代谢物训练巨噬细胞介导结肠炎保护作用
此项研究揭示了小麦纤维通过依赖菌群 (尤其是B. theta) 产生特定代谢物 (如异嗪皮啶),重编程结肠巨噬细胞能量代谢,诱导其向M2型抗炎表型极化,从而减轻DSS诱导结肠炎的新机制。该作用不依赖于经典的SCFA、IL-22或FXR通路。研究结果提示,现代食品加工中去除了小麦中的纤维成分,可能增加了IBD的发病风险;而补充小麦纤维或通过菌群代谢产生的活性小分子,有望成为预防或辅助治疗IBD的新策略。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)