心脏再同步化治疗(CRT),亦称“心脏生理起搏”,是射血分数降低的
近年来,以希氏束起搏与左束支起搏为代表的传导系统起搏技术快速发展,为心衰合并传导系统疾病的治疗带来了突破性变革。随着该领域理念更新、大型临床试验推进、新版指南发布以及接受CRT治疗的患者数量持续增加,临床医师有必要系统掌握CRT的核心机制、双心室起搏与传导系统起搏的差异、循证医学证据、心电图特征、器械管理及未来发展方向。同时,建议将CRT术语更名为“冠状窦导线心脏生理性起搏”或“传导系统导线心脏生理性起搏”,以更准确地描述其特征。

心脏传导系统的生理功能是维持心脏机械收缩,确保房室同步、室内同步与室间同步。当左右心室激动失同步,如出现左束支传导阻滞(LBBB),或单纯行右心室心内膜起搏时,左心室功能或进一步下降,这一现象在左心室收缩功能本身已降低的患者中更为显著。
过去20年间,双心室起搏是改善HFrEF患者左心室失同步的主要手段。该技术通过冠状窦将导线置入左心室侧方或后外侧静脉分支,以捕获心外膜(图1);若经冠状窦途径无法完成左心室导线植入时,可通过开胸或胸腔镜手术将导线直接固定于左心室心外膜。
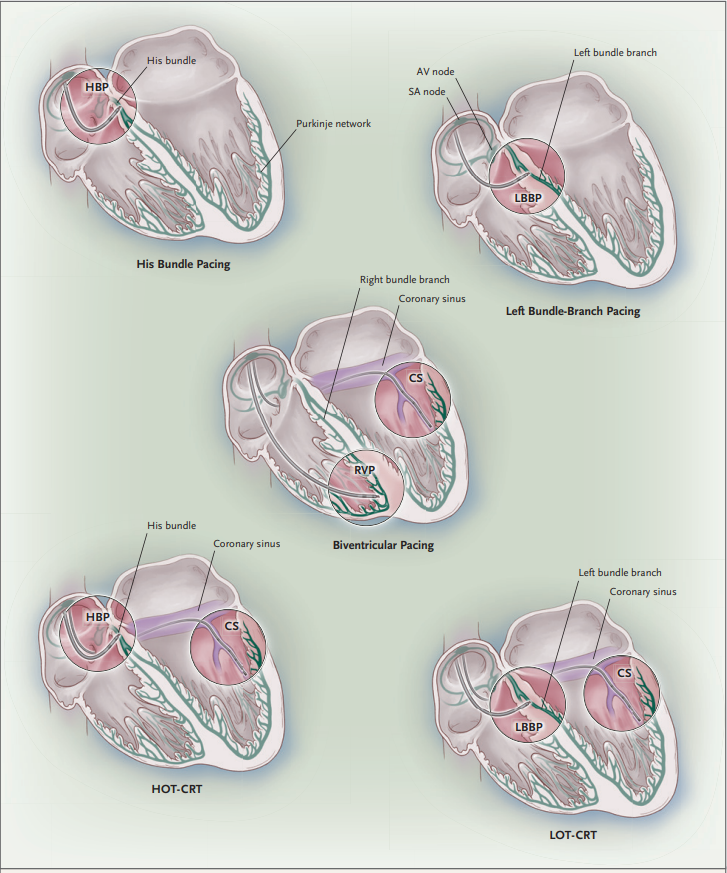
图1 电极配置
注:图示为希氏束起搏(HBP)、左束支起搏(LBBP)、双心室起搏、希氏束支优化心脏再同步化治疗(HOT-CRT)及左束支优化心脏再同步化治疗(LOT-CRT)的导线配置。AV代表房室结,CS代表冠状窦,RVP代表右心室起搏,SA代表窦房结。
双心室起搏通过将起搏导线或植入式心律转复除颤器(ICD)导线放置于右心室,使右心室心内膜与左心室外膜激活同步,从而达到心室逆向重塑。激活过程在心肌细胞间传递,不直接涉及传导系统,从而融合右心室和左心室刺激产生的电波阵面。
在临床实践中,双心室起搏仍面临诸多挑战:冠状窦内缺乏合适的靶血管、导线脱位、左心室侧壁心肌瘢痕组织、疗效受QRS形态与时限影响显著等。目前已通过器械算法优化,将右束支自身下传激动与冠状窦导线起搏信号融合,进一步提升起搏效果。
双心室起搏已在多项随机对照试验中得到验证,累计纳入超过10000例心衰患者,证实其可显著改善临床预后(表1)。早期研究显示,双心室起搏能够改善LVEF、减轻二尖瓣反流、缩小心室容积、提升患者生活质量。在此基础上,多项大型随机对照研究以死亡与住院为终点,进一步验证了其远期价值。
表1 通过双心室起搏实现心脏生理性起搏的相关试验
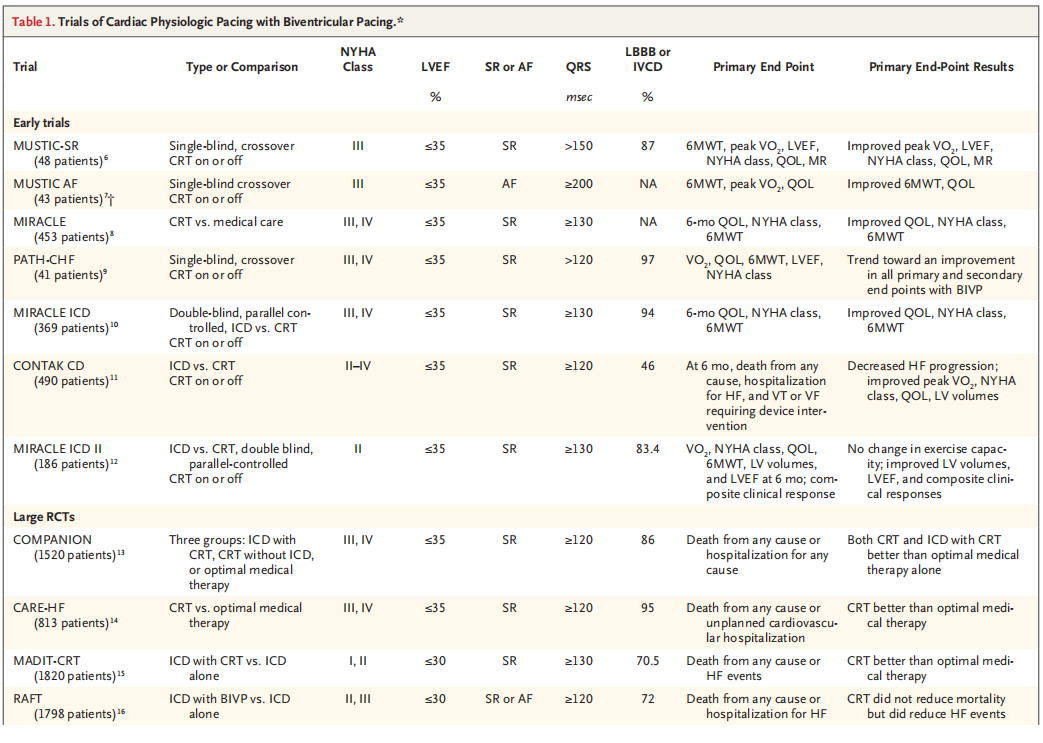
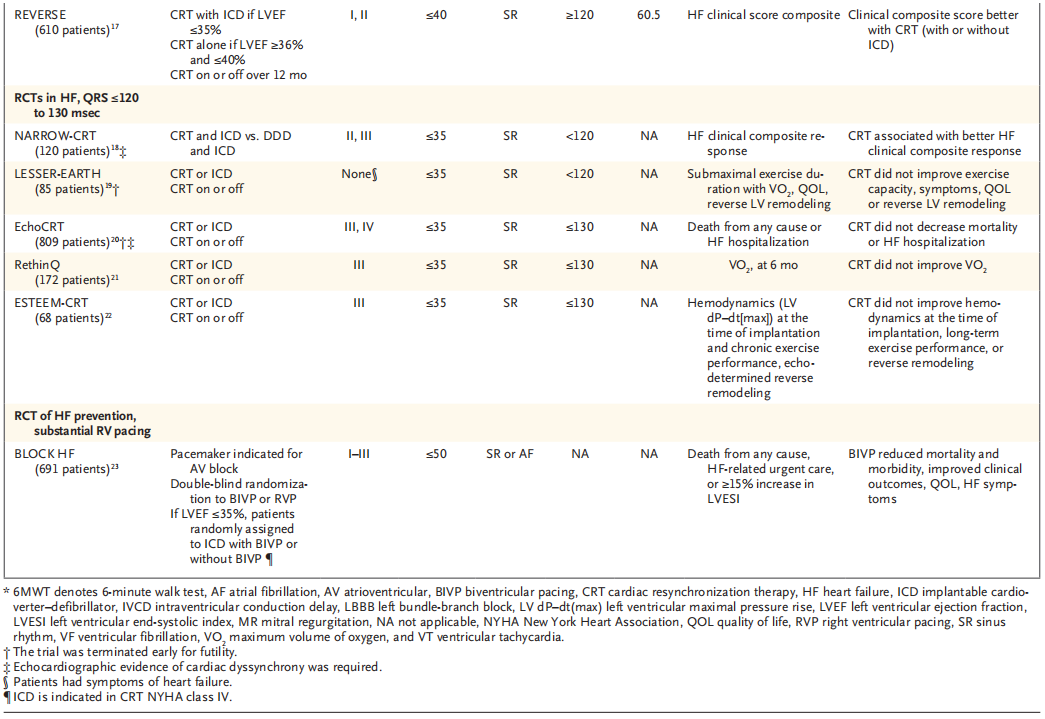
COMPANION和CARE-HF试验均纳入NYHA Ⅲ~Ⅳ级、QRS时限≥120 ms、LVEF≤35% 的晚期心衰患者。COMPANION研究将1520例患者分为双心室起搏组、双心室起搏联合ICD组与对照组(不植入器械),结果显示,双心室起搏可显著降低全因死亡或任意原因住院的复合终点事件;其中联合ICD治疗对全因死亡的降低更为显著,且在QRS时限≥150 ms 的患者中获益最大。CARE-HF研究纳入813 例患者,结果证实双心室起搏可显著降低全因死亡或主要心血管事件住院的复合终点,长期随访还提示其可减少
在MADIT-CRT与RAFT试验中,所有患者均按指南植入ICD,并随机分为ICD联合双心室起搏组与单纯ICD 组。两项研究均证实,双心室起搏可显著降低死亡与心衰的复合事件终点及全因死亡率,尤其在QRS时限≥150ms且呈左束支传导阻滞特征的患者中获益突出。MADIT-CRT事后分析提示,非左束支传导阻滞患者未从CRT治疗中获益。
REVERSE试验的结果亦支持上述现象。该试验以中度心衰患者为对象,证实开启双心室起搏12个月可显著改善心衰复合临床终点;事后分析显示,获益随QRS时限延长而增加,QRS≤130ms者获益几乎可以忽略。后续的四项随机对照试验进一步证实,QRS时限偏窄的患者无法从双心室起搏中获益。
此外,普遍的观察性试验结果显示,约三分之一合并传导系统病变的心衰患者对双心室起搏无反应。反应与否通常以心室逆重构证据(左心室收缩末期容积减小)、心功能分级改善、LVEF提升、6 min步行距离增加等作为判断标准。在大型研究中,双心室起搏可稳定降低心衰事件与住院率,对个体患者而言,即便左心室舒张末期容积或LVEF无明显变化,只要心衰症状稳定,仍可认为达到临床获益。
无反应常见原因包括:非左束支传导阻滞、QRS时限 120~130 ms、冠状窦侧支血管条件差、起搏阈值过高导致失夺获、终末期心衰、室性早搏或
总体而言,非缺血性
在LVEF≤50%且接受右心室起搏的患者中,或可出现左心室功能下降,即起搏诱发的心肌病。这类患者主要包括自发性
针对房室传导阻滞患者,Block HF研究是目前规模最大的随机对照试验。该研究纳入691例LVEF≤50% 且具备起搏指征的患者,随机分为单纯右心室起搏组与双心室起搏组;其中合并ICD指征者分别接受双心室起搏联合ICD或单纯右心室起搏联合ICD治疗。结果显示,无论是否联合ICD,双心室起搏均可显著降低全因死亡、心衰紧急住院或左心室收缩末期容积指数增加≥15%的复合终点事件。当前指南强调,应通过合理的起搏器参数设置,避免不必要的右心室起搏,预防起搏诱导性心肌病。
心脏传导系统起源于上腔静脉与右心房交界处的窦房结,电信号依次经房室结、希氏束、左右束支及浦肯野纤维网传导(图1)。希氏束是连接心房与心室的特殊心肌纤维,平均长2.6 mm、宽3.7 mm、厚1.4 mm,穿过膜性间隔,并在其中被中央纤维体完全包裹。
由于希氏束体积微小且定位困难,因此其大小和位置对希氏束起搏具有重大临床意义。周围纤维组织可能导致起搏阈值升高并随时间推移持续增加,最终引发捕获丧失。此外,导线轻微移位也会改变起搏阈值。相比之下,左束支是宽达14 mm的弥漫性心内膜下结构,紧邻室间隔心肌,分成前分支、后分支及常见的间隔支。因此,相较希氏束,左束支导线植入的目标区更大,捕获丧失风险更低。
希氏束起搏是最符合生理的起搏方式,因为它保留了左心室和右心室的自然激活(图1),适用于房室结及希氏束内传导病变伴症状性心动过缓的患者,还可纠正希氏束浦肯野系统病变所致左束支传导阻滞。
左束支起搏需将导线经室间隔植入左心室心内膜下左束支或其分支区域。由于成功率更高、起搏阈值更低且更稳定,可有效纠正希氏束以下水平病变导致的左束支传导阻滞,左束支起搏已迅速成为传导系统起搏的主流技术。
欧洲多中心MELOS试验显示,在心动过缓与心衰患者中,左束支起搏成功率分别达92.4%与82.2%,总体安全性良好;最常见并发症为间隔急性穿孔(约 3.7%),可术中及时调整导线位置,远期无明显不良事件。左束支起搏通常会单独捕获传导系统,但最常见的是捕获传导系统和局部心室心肌(非选择性左束支起搏器)。左束支起搏可以捕获左束干或其中一个束;其中哪一束被捕获将反映在特征性QRS形态特征中。
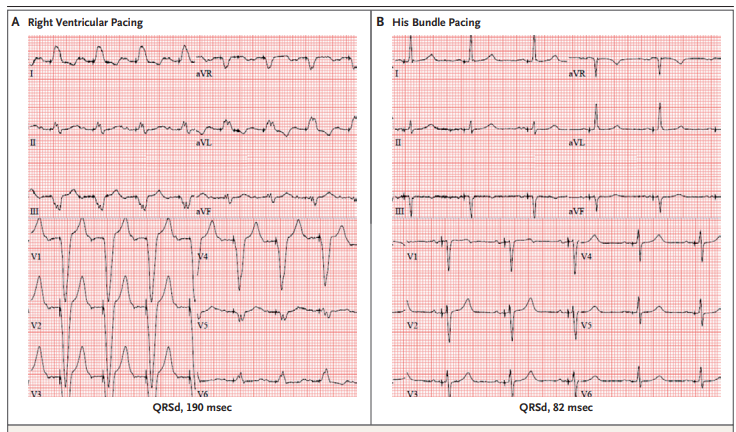
图2 心电图显示的希氏束起搏
注:图A. 右心室
多项小样本随机对照研究评估了希氏束或左束支起搏在心衰、LVEF 35%~40%、需左心室同步化治疗患者中的作用,涵盖左束支传导阻滞、房颤房室结消融后、PR间期延长等场景。部分研究提示,希氏束起搏可缩窄QRS时限,在生活质量、心功能分级、6 min步行距离与LVEF改善方面与双心室起搏相当;但因QRS缩窄要求严格、起搏阈值限制,希氏束起搏转为双心室起搏的比例较高。
LBBP-RESYNC试验纳入40例患者,显示左束支起搏在提升LVEF、减小左心室收缩末期容积、降低NT-proBNP 方面更具优势,在心功能分级、6 min步行距离、QRS时限及CRT反应率方面与双心室起搏相当。
LEVEL-AT 试验未发现传导系统起搏与双心室起搏在左心室激动时间、QRS时限、LVEF、左心室收缩末期容积指数、心功能分级及死亡/心衰住院复合终点上存在显著差异。
尽管上述小样本随机试验统计学效能不足以评估死亡与心衰住院终点,但回顾性对照研究提示,希氏束起搏或左束支起搏在这些临床结局方面或优于双心室起搏。
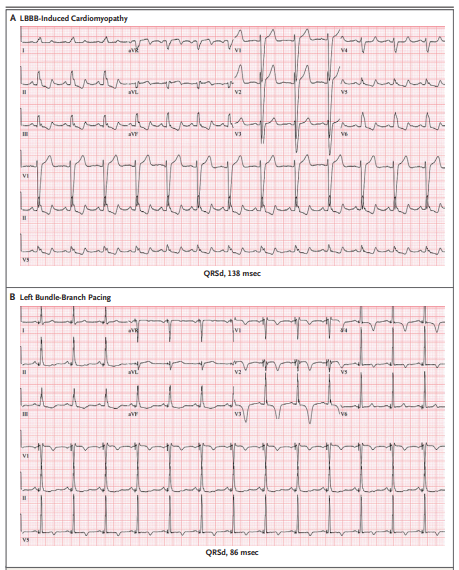
图3 心电图显示的左束支起搏
注:图A. LBBB诱发心肌病患者的基线心电图(QRS时限,138 ms),LVEF为30%~35%。图B. 同一患者实施左束支起搏后的心电图,起搏QRS时限为86 ms。经左束支起搏后,LVEF改善至50%~54%。V1导联出现的右束支形态学特征提示左束支起搏或左室间隔起搏。通过额外起搏操作可区分左束支起搏与左室间隔起搏,本例患者最终确认为左束支起搏。
I-CLAS试验是迄今为止最大的回顾性病例对照研究,其结果显示,在LVEF≤35%及36%~50%的心衰患者中,左束支起搏或可显著降低全因死亡与心衰住院复合终点,同时减少新发房颤与室性
在技术上,左束支起搏
尽管缺乏大型随机临床试验,但近期心律学会-亚太地区心律学会-拉丁美洲心律学会联合发布的指南指出,当无法实现有效的CRT治疗时,传导系统起搏可作为传统双心室起搏的替代方案。目前多项大型随机试验正在进行中,这些试验具有足够的能力来确定传导系统起搏是否优于当前的标准起搏策略。
由心衰团队与电生理团队共同组建的多学科诊疗模式,可优化指南导向药物治疗并合理选择生理起搏策略,与提升医疗质量、提高患者依从性、保障用药安全、降低住院率与死亡率相关。
鉴于磁共振成像在临床中的广泛应用,起搏导线与器械的MRI兼容性至关重要。目前部分传导系统起搏导线与系统已标注MRI兼容,正在开展的临床试验将进一步完善安全性数据,推动更多导线与器械获得MRI兼容认证。
传导系统起搏导线拔除经验逐步积累,导线分为无管腔型与导丝驱动型。已有国际多中心研究显示,无管腔导线拔除成功率可达100%,少数患者残留远端片段,轻微并发症发生率仅2.1%。由于传导系统起搏临床应用时间较短,导线植入时间偏短,拔除难度相对更低;导丝驱动型希氏束或左束支起搏导线的拔除数据仍有限。
生理性起搏是一个动态发展的领域,近年来在多个方向持续进展。目前,双心室起搏在治疗心功能异常及传导系统疾病患者中的作用已得到充分证实,并经多项大型随机试验验证,这些试验均采用包括死亡率等在内的具有临床意义的终点。关于传导系统起搏(特别是左束支起搏)的证据体系正在快速扩充。目前进行中的随机临床试验将确立传导系统起搏相较双心室起搏的相对疗效与安全性。如果两种起搏策略效果相当,则需综合其他因素进行选择。
与双心室起搏相比,希氏束起搏和左束支起搏系统更为简单,植入术时间更短,或带来一系列积极影响,如降低费用、减少辐射剂量、降低造影剂用量并延长电池寿命。费用降低或源于更经济的起搏脉冲发生器,以及更少或更经济的导线。CRT ICD或起搏脉冲发生器(用于双心室起搏)的价格远高于单纯ICD或无CRT功能的起搏器,而后者是传导系统起搏所用的起搏脉冲发生器类型。起搏导线的价格也低于双心室起搏系统中使用的冠状窦左心室导线。另外,鉴于希氏束起搏导线或左束支起搏导线兼具起搏与心脏再同步双重功能,因此单根导线即可实现功能,而双心室起搏则需两根导线。尤为重要的是,对于症状性窦房结功能障碍及房室传导阻滞的适应证,传导系统起搏或可取代传统右心室起搏。
未来5~10年,随着大型随机对照试验结果公布,诸多临床问题将得到解答:希氏束起搏是否会被左束支起搏完全替代?传导系统起搏能否改善右束支传导阻滞或非特异性室内传导延迟患者的心室失同步(这类患者从双心室起搏中获益有限)?心衰合并左束支传导阻滞患者是否应以传导系统起搏为首选、双心室起搏为备选?部分患者可能从HOT-CRT及LOT-CRT中获益(图2),即传导系统起搏联合冠状窦左心室起搏。随着技术进步,起搏导线、输送工具、器械及程控算法仍将持续优化,或为患者带来更大益处。
参考文献:Physiologic Pacing in Heart Failure.Chelu MG, Poole JE, Ellenbogen KA.N Engl J Med. 2026 Jan 22;394(4):367-381. doi: 10.1056/NEJMra2415650.
•现任泰达国际心血管病医院特聘专家
•中国
•《中华老年心脑血管病杂志》编委,《中华临床 医师杂志》(电子版)特邀审稿专家,《中华诊断学电子杂志》审稿专家,《华夏医学》杂志副主编,《中国心血管杂志》常务编委,《中国心血管病研究》杂志第四届编委,《世界临床药物》杂志编委、《医学综述》杂志会编委、《中国医药导报》杂志编委、《中国现代医生》杂志编委、《心血管外科杂志(电子版)》审稿专家
•本人在专业期刊和心血管网发表文章948篇其中第一作者759篇,参加著书11部
作者:郑刚教授
编辑&排版:GXM
医脉通是专业的在线医生平台,“感知世界医学
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)