自2018年以来,以免疫检查点抑制剂(CPI)为基础的联合方案已正式成为转移性
既往METEOR等关键研究已证实卡博替尼用于VEGF靶向治疗进展后mRCC患者的二线治疗可显著改善生存与缓解率,但CONTACT‑03、CANTATA等后续研究虽纳入CPI经治患者,却并非聚焦于一线CPI联合治疗进展后的纯二线治疗场景,研究人群混杂多线治疗病例,导致一线CPI联合治疗进展后纯二线卡博替尼单药的前瞻性疗效证据始终缺失。
为填补这一核心临床证据空白,一项欧洲多中心、开放标签的Ⅱ期CaboPoint研究正式公布最终结果,该研究以前瞻性设计专门评估“一线CPI联合治疗进展后” mRCC患者直接使用卡博替尼单药二线治疗的疗效与安全性,相关成果“CaboPoint: A Phase 2 Study of Second-line Cabozantinib After Checkpoint Inhibitor–based Combination Therapy in Patients with Metastatic Renal Cell Carcinoma”发表于《European Urology》,旨在及时填补这一关键证据空白。医脉通泌尿外科现对该研究进行深度解读,以飨读者。

CaboPoint研究(临床试验编号:NCT03945773)是一项多中心、开放标签的Ⅱ期前瞻性临床试验,研究时间为2020年1月8日至2023年11月13日,在欧洲多国开展。入组患者此前均接受过
研究主要终点为独立中心评估(ICR)的队列A客观缓解率(ORR),次要终点包括队列B客观缓解率、当地研究者评估(LIR)的客观缓解率、无进展生存期(PFS)、总生存期(OS)、缓解持续时间(DOR)、疾病控制率、安全性及患者生活质量(QoL),统计学分析采用单样本精确检验对主要终点进行统计推断,安全性依据CTCAE 5.0标准进行分级评估。
1、患者基线特征
在接受筛选的148例受试者中,有127例来自40个研究中心并被纳入研究,平均年龄为64.2岁,75.6%为男性。绝大多数患者(65/75,86.7%)确诊时的国际转移性肾细胞癌数据库联盟(IMDC)风险分级为中危或高危;另有52例患者存在数据缺失。A队列(n = 85)与B队列(n = 42)的基线特征总体保持平衡。确诊时,大部分患者已出现局部进展(17.6%)或远处转移(61.6%)。(表1)
表1 入组患者基线特征
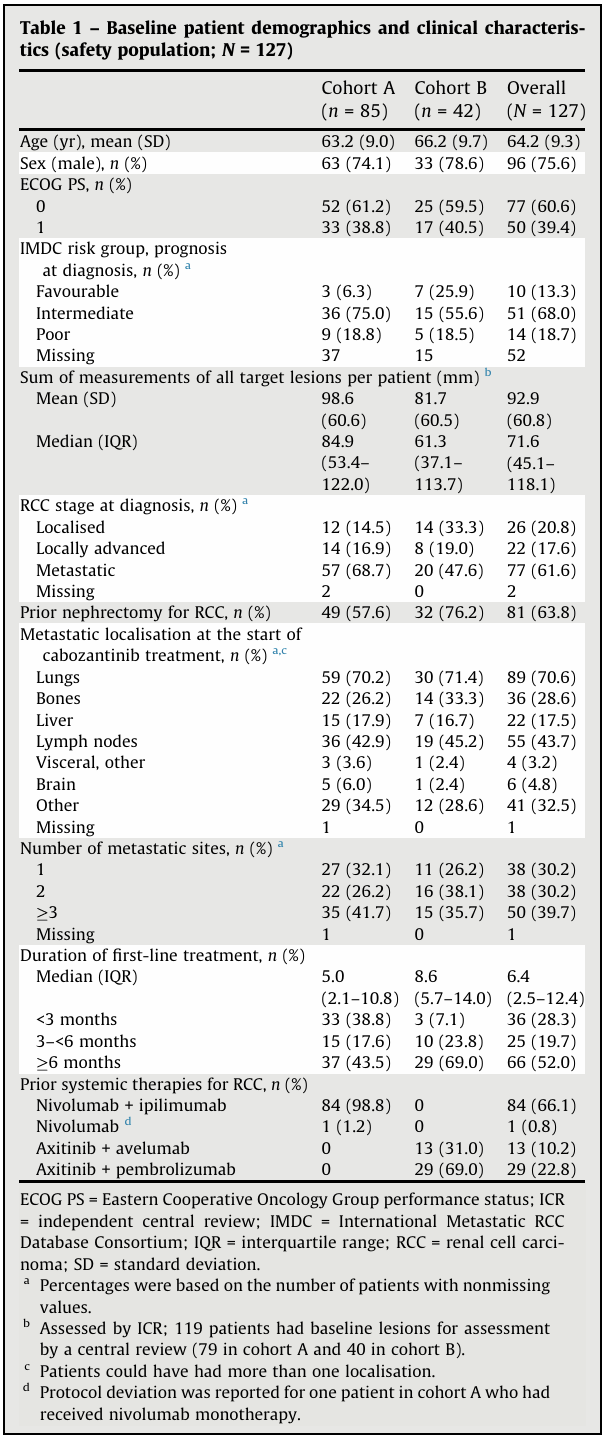
2、疗效
中位随访时间为19.3(10.9–26.3)个月:A队列19.3(11.2–26.5)个月;B队列20.4(10.3–24.3)个月。所有患者均纳入研究者报告结局的疗效分析人群。8例患者(A队列6例、B队列2例)缺乏靶病灶的基线中心评估,因此119例患者(A队列79例、B队列40例)纳入ICR报告结局的疗效分析人群。
队列A的ORR(95% CI)为40.5%(29.6%–52.1%;32/79),此为主要终点;队列B的ORR为27.5%(14.6%–43.9%;11/40);总体ORR为36.1%(27.5%–45.4%;43/119)。相较于10%的阈值,主要终点的差异具有统计学意义(p < 0.0001)。两个队列及总体的疾病控制率均超80%(图1A)。队列A和队列B的部分缓解病例数分别为32/76例(42.1%)和10/37例(27.0%);完全缓解病例数分别为0/76例(0%)和1/37例(2.7%)。为保证客观缓解率分析的严谨性,将数据缺失的患者(每个队列各3例)均视为无缓解者(疾病进展患者),但未呈现其最佳总体缓解数据(图1A、B)。
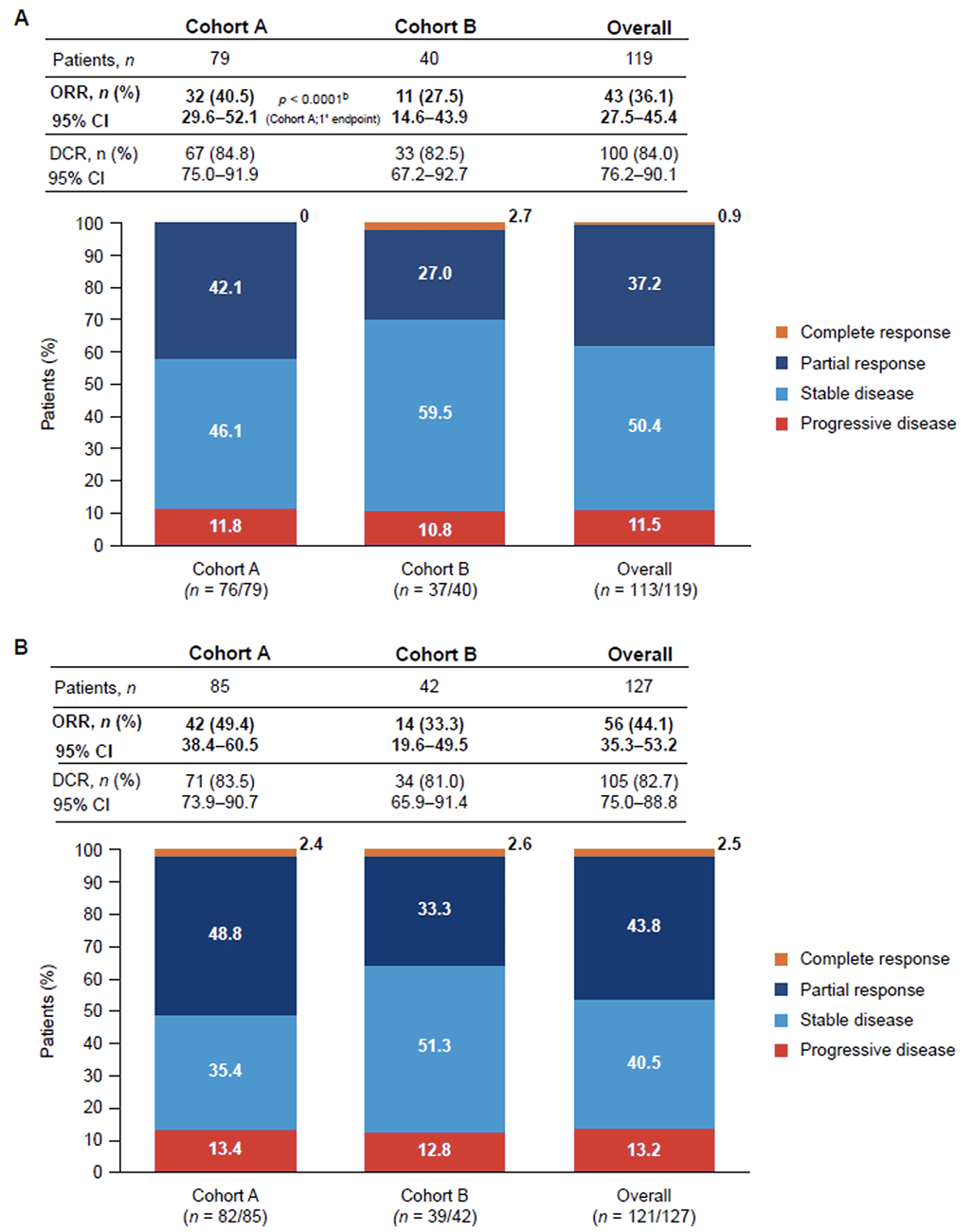
图1 队列A和队列B中,由ICR评估(A)和由LIR评估(B)得出的ORR与DCR。
队列A的应答一致率为77.6%,队列B为73.0%。基线肿瘤大小的最佳中位缩小百分比为<31.2%,尽管未进行统计学比较,但无论采用何种评估方式,队列A的该数值在数字上均高于队列B。
无统计学比较情况下,队列A的PFS和DOR在数值上长于队列B,而两组的至缓解时间(TTR)和OS则相近(图 2)。
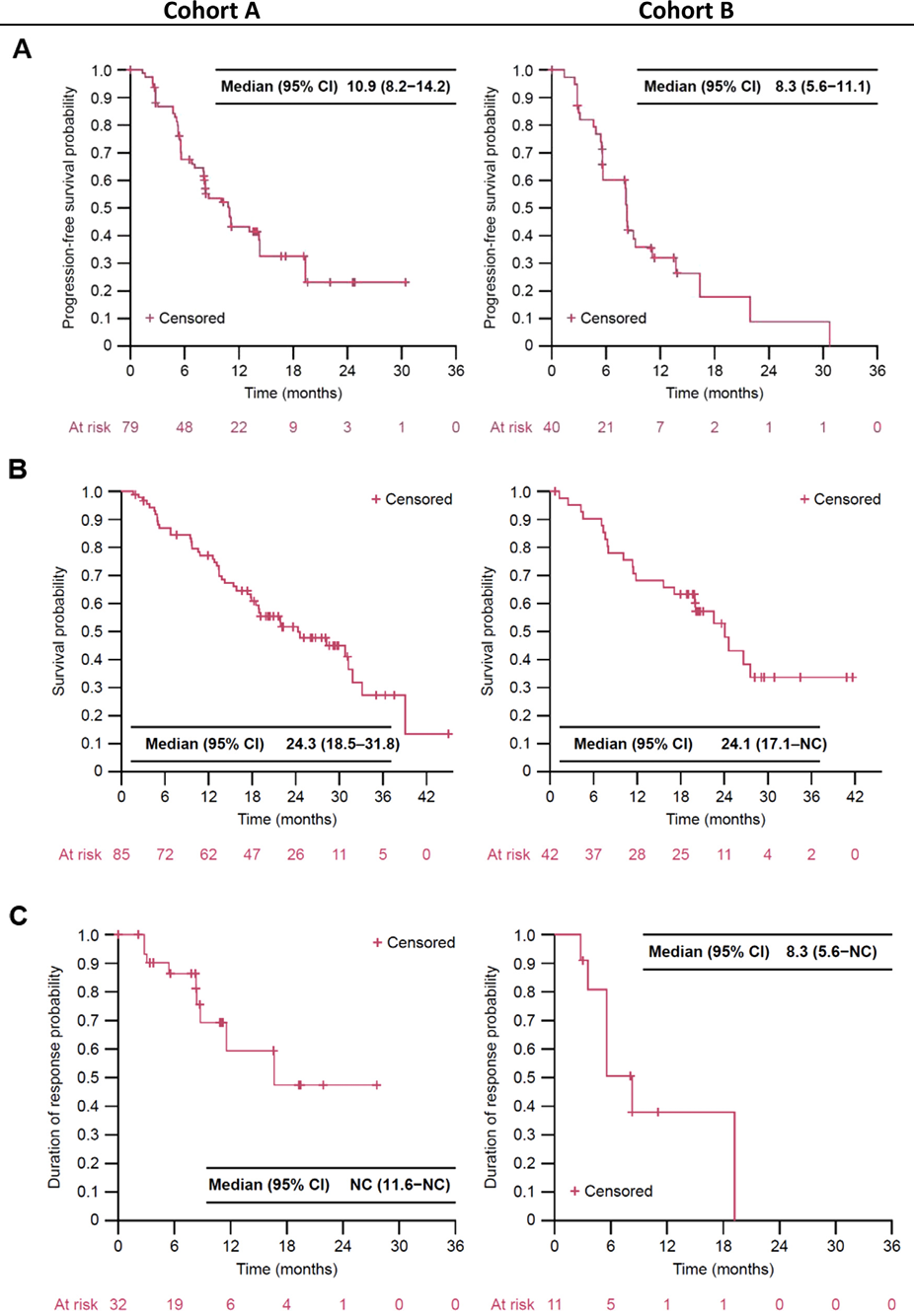
图2 队列A和队列B中由ICR评估的PFS(A)、OS(B)以及DOR(C)
尽管患者数量较少,但在两个队列的以下患者亚组中,由ICR评估的ORR在名义上均更高(未进行统计学比较):年龄<65岁 vs 年龄≥65岁、东部肿瘤协作组(ECOG)体力状况评分0分 vs 1分、转移灶数目1-2个 vs 3个及以上、IMDC预后风险分层良好 vs 中危/高危;以及接受过肾切除术 vs 未接受肾切除术(仅针对A队列)。两个队列的患者均接受了后续治疗,其中48.8%的患者接受了三线治疗。在这些接受后续治疗的患者中,A队列患者最多接受了六线治疗,B队列患者最多接受了四线治疗。根据
3、事后分析
由ICR评估的确认ORRs(即连续两次影像学评估均显示缓解),在A队列中为34.2%(95% CI:23.9–45.7%; 27/79),B队列中为20.0%(95% CI:9.1–35.6%;8/40),总体为29.4%(95% CI:21.4–38.5%;35/119)。
由LIR评估的确认ORRs(95% CI),在A队列中为29.4%(95% CI:20.0–40.3%;25/85),B 队列中为19.0%(95% CI:8.6–34.1%;8/42),总体为26.0%(95% CI:18.6–34.5%;33/127)。
4、安全性
卡博替尼的药物暴露量、剂量降低以及剂量中断情况在各队列间总体相似。卡博替尼的中位总药物暴露时长为8.8(4.8–17.5)个月,队列A为9.2(4.8–19.8)个月,队列B为8.4(5.0–14.8)个月。在93例具备可用数据的患者中,有73例(78.5%)坚持治疗;各队列间的结果相似(表2)。
表2 安全性数据分析
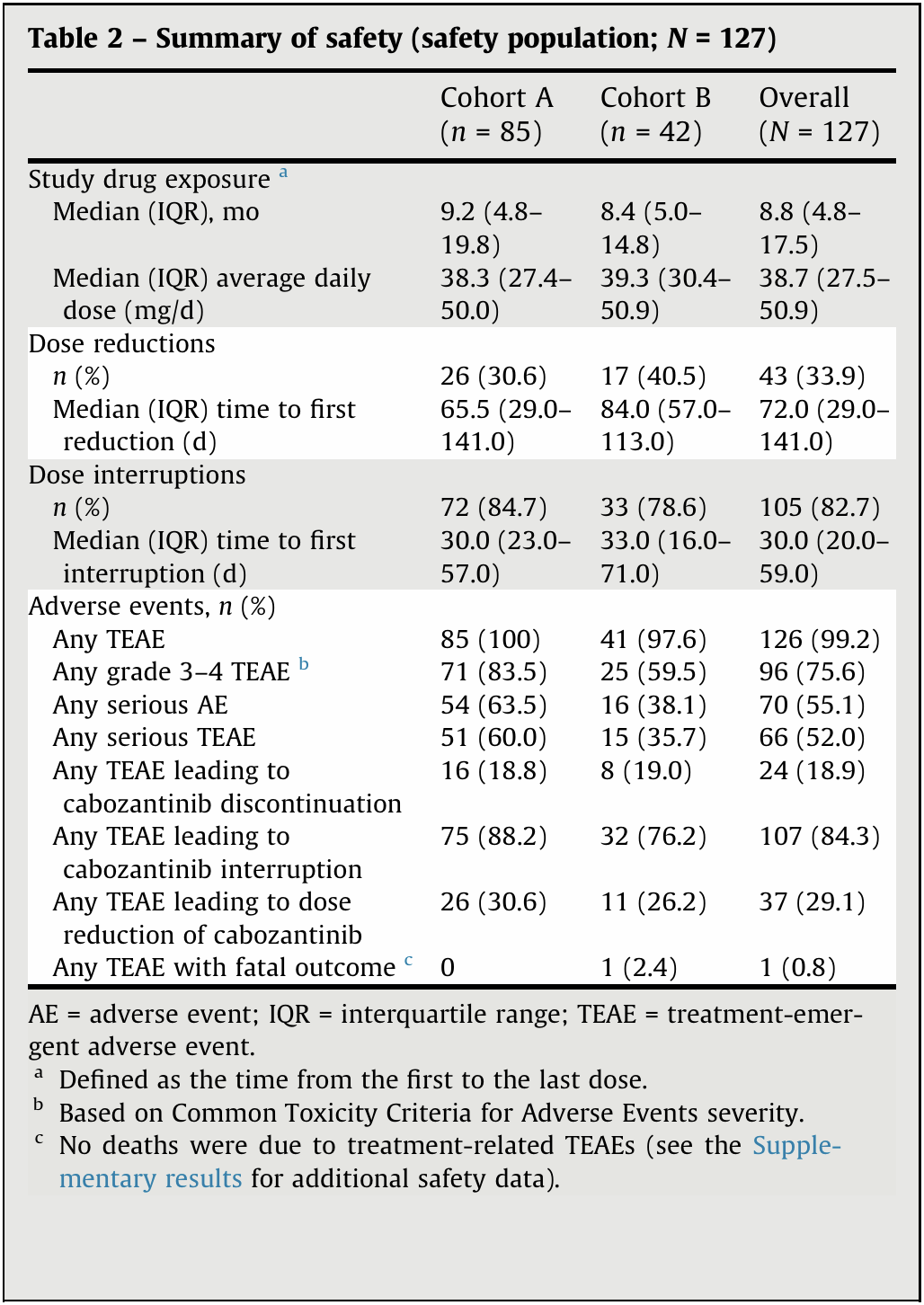
多数患者报告出现了任意级别的治疗期间出现的不良事件(TEAEs),其中大部分为轻至中度。
大多数TEAEs与治疗相关;最常见的不良事件为
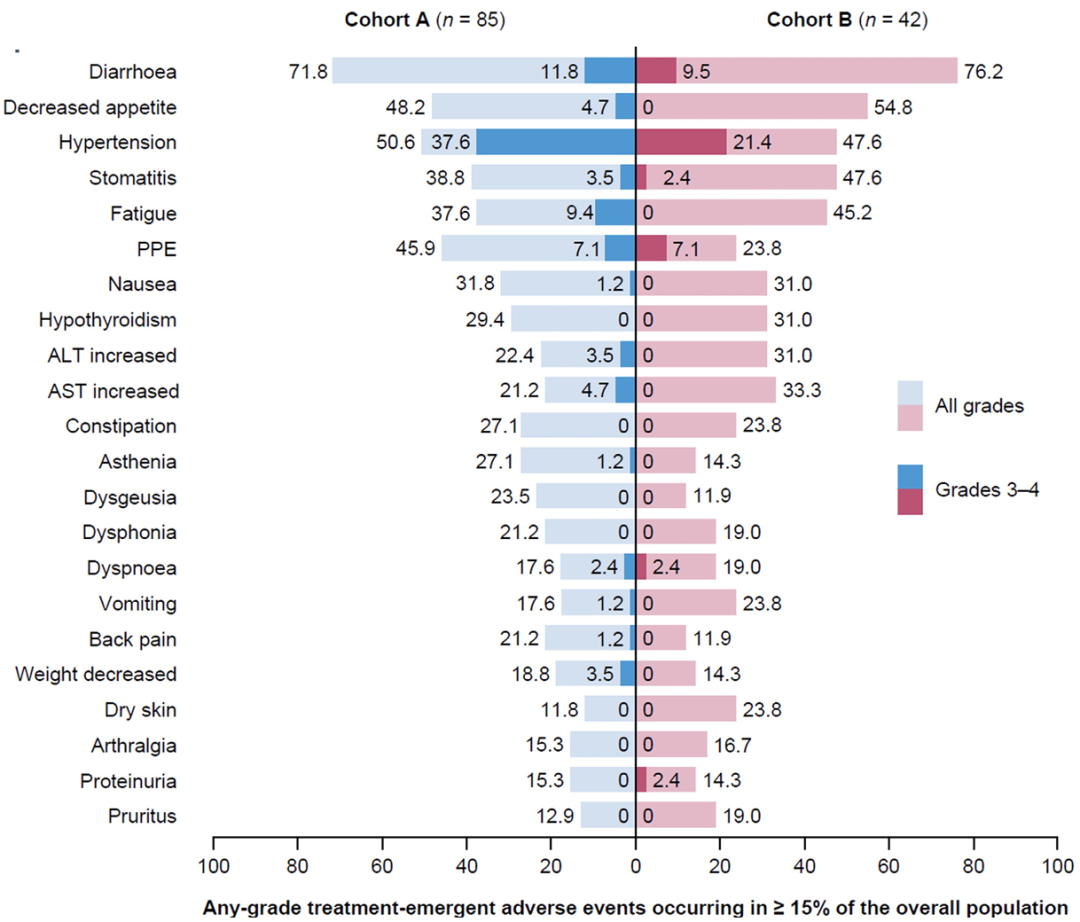
图3 按等级划分的最常见的TEAEs
CaboPoint研究是首个专门评估一线免疫检查点抑制剂联合治疗进展后,纯二线单药卡博替尼治疗晚期肾细胞癌疗效与安全性的前瞻性研究,研究结果证实卡博替尼用于该场景下的二线治疗疗效确切、安全可控,其中一线双免疫联合进展后患者的客观缓解率更高、无进展生存期更长,获益更为显著。该研究填补了晚期肾细胞癌二线治疗的关键证据空白,明确了卡博替尼作为一线免疫联合进展后标准二线单药治疗的地位,同时为后续晚期肾细胞癌二线新型治疗方案的研究提供了重要的对照基准,推动了转移性肾细胞癌个体化二线治疗决策的优化。
参考文献
1.Albiges L, Borkowetz A, Gravis G, et al. CaboPoint: A Phase 2 Study of Second-line Cabozantinib After Checkpoint Inhibitor–based Combination Therapy in Patients with Metastatic Renal Cell Carcinoma[J]. European Urology, 2026, 89:210-219.
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
医脉通是专业的在线医生平台,“感知世界医学
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)