Metadata Card
文献题目:CD40-CD40L inhibition attenuates platelet-neutrophil interaction and neutrophil extracellular trap release in primary antiphospholipid syndrome
发表期刊:Annals of the Rheumatic Diseases
发表时间:26.01.21 Online
影响因子:20.6(中科院1区)
通讯作者/单位:Maria G. Tektonidou @ 雅典大学医学院第一内科【APS方向的专家】
一句话总结:研究首次证明 CD40-CD40L 轴通过介导血小板-中性粒细胞聚合与自噬,驱动携带组织因子的 NETs 释放,阻断该轴可显著抑制 PAPS 的促栓过程。
Graphical Abstract

Abstract
中文摘要:
目的:中性粒细胞胞外诱捕网(NETs)在原发
方法:我们检测了PAPS患者、无症状
结果:与无症状aPL携带者和HCs相比,PAPS患者的中性粒细胞表现出更高的NET释放。PAPS患者来源的NET表达组织因子(TF),可在HCs的血小板缺乏血浆中诱导
结论:通过抑制CD40-CD40L通路靶向血小板-中性粒细胞/自噬/TF阳性NET轴,可减轻PAPS中的血栓炎症反应,值得进一步探索其作为潜在治疗策略的价值。
Background & Problem
背景:抗磷脂综合征(APS)以反复血栓形成和
痛点:尽管已知NETs参与PAPS,但驱动其释放的精确上游机制、NETs如何直接导致血栓,以及如何精准抑制这一过程仍存在大量未知。特别是组织因子(TF)在NETs上的表达及其功能性作用在PAPS中尚未完全阐明。
Methodology
策略:研究采用了“临床样本验证 + 体外机制研究 + 动物模型干预”的综合策略。
逻辑:
临床验证:对比PAPS患者、无症状aPL携带者及健康对照的NETs 释放水平。
组织学分析:在PAPS患者的肾脏、皮肤溃疡及动脉血栓组织中寻找TF阳性NETs。
体外模拟:用健康人中性粒细胞,探究aPL、血小板、自噬在NETs 产生中的协同作用。
靶向干预:使用CD40-CD40L抑制剂(DRI-C21045)及自噬抑制剂进行验证。
体内实验:在aPL诱导的下腔静脉结扎小鼠模型中测试anti-CD40L 抗体的疗效。
Key Results & Interpretation
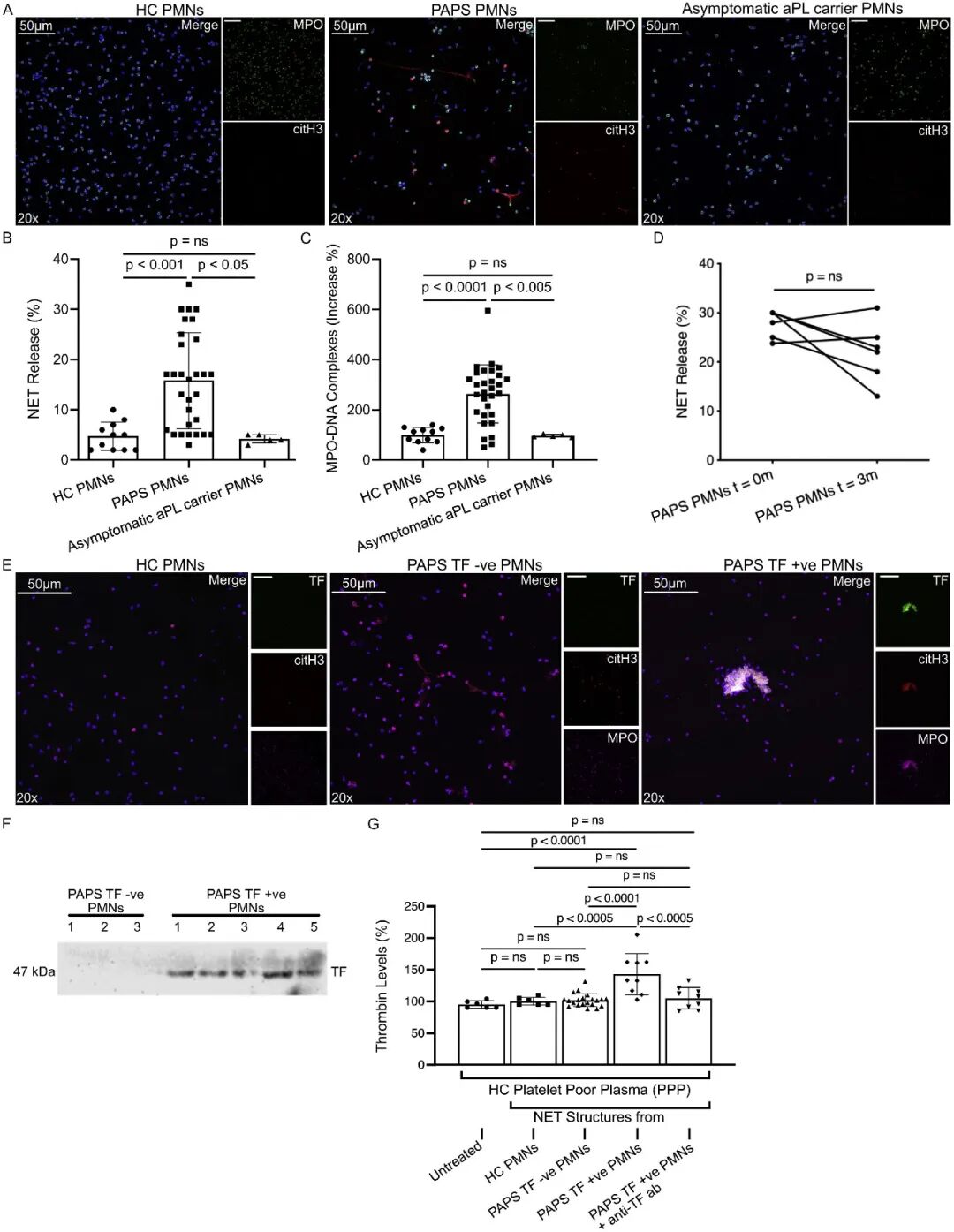
1A & 1B:共聚焦显微镜显示,PAPS患者的中性粒细胞自发释放NETs 的比例显著高于健康对照和无症状aPL携带者。
1C:ELISA检测证实PAPS患者中MPO-DNA复合物(NETs 的标志物)浓度升高。
1D:追踪 3 个月发现,PAPS 患者这种自发产生 NETs 的特征具有持续性。
1E:免疫荧光显示 PAPS 的 NETs 表面装饰有组织因子(TF)。
1F: Western Blot验证了 PAPS 患者 NETs 蛋白中 TF 的高表达。
1G:功能实验显示,PAPS 患者的 TF-NETs 能显著诱导血浆产生凝血酶,而加入 anti-TF 中和抗体后,该效应消失,证明了其促凝依赖于 TF。
发现点2:受累器官组织中的 TF-NETs 沉积
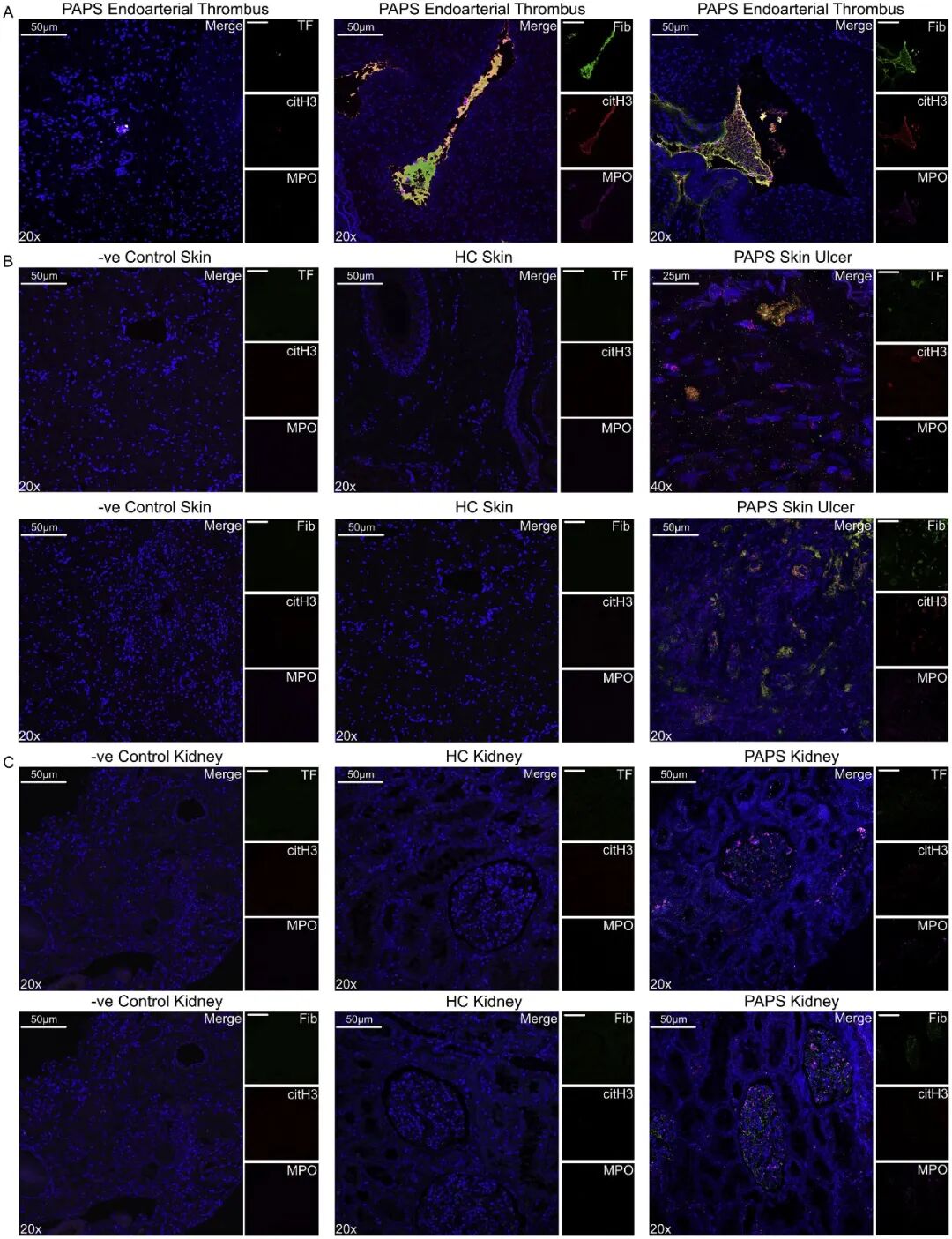
2A:在PAPS患者的机化性动脉血栓中,可观察到TF阳性的NETs与纤维蛋白原(Fib)紧密结合。
2B:在PAPS相关的皮肤溃疡活检中,血栓血管内外均分布着大量TF-NETs。
2C:在PAPS
发现点3:血小板是 aPL 诱导 NETs 释放的关键媒介
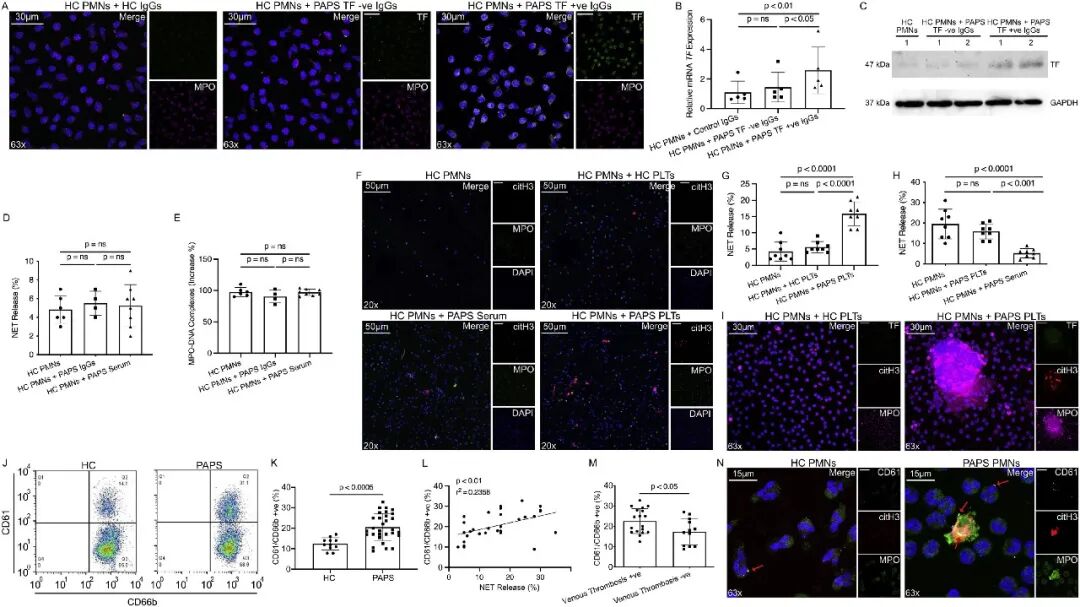
3A-3C:只有来自TF+患者的aPL IgG能诱导健康人中性粒细胞胞内 TF 的 mRNA 和蛋白表达。
3D & 3E:aPL IgG本身并不能直接诱导健康中性粒细胞释放NETs。
3F & 3G:当加入来自PAPS患者的血小板(PLTs)后,健康中性粒细胞才开始大量产生NETs。
3H:证明了PAPS患者的血小板具有独立诱导NETs的能力,优于血清或 aPL IgG。
3I:仅由PAPS血小板诱导的NETs为TF阴性(除非预先用aPL刺激中性粒细胞产生TF)。
3J & 3K:流式细胞术显示PAPS患者外周血中CD61+/CD66b+(血小板-中性粒细胞聚合体,PNCs)显著增加。
3L:患者体内PNCs的比例与NETs释放水平呈强正相关。
3M:合并静脉血栓病史的患者,其PNCs水平更高。
3N:共聚焦显微镜直接观察到了附着在PAPS患者中性粒细胞表面的血小板。
发现点4:aPL 通过激活血小板发挥促 NETs 作用
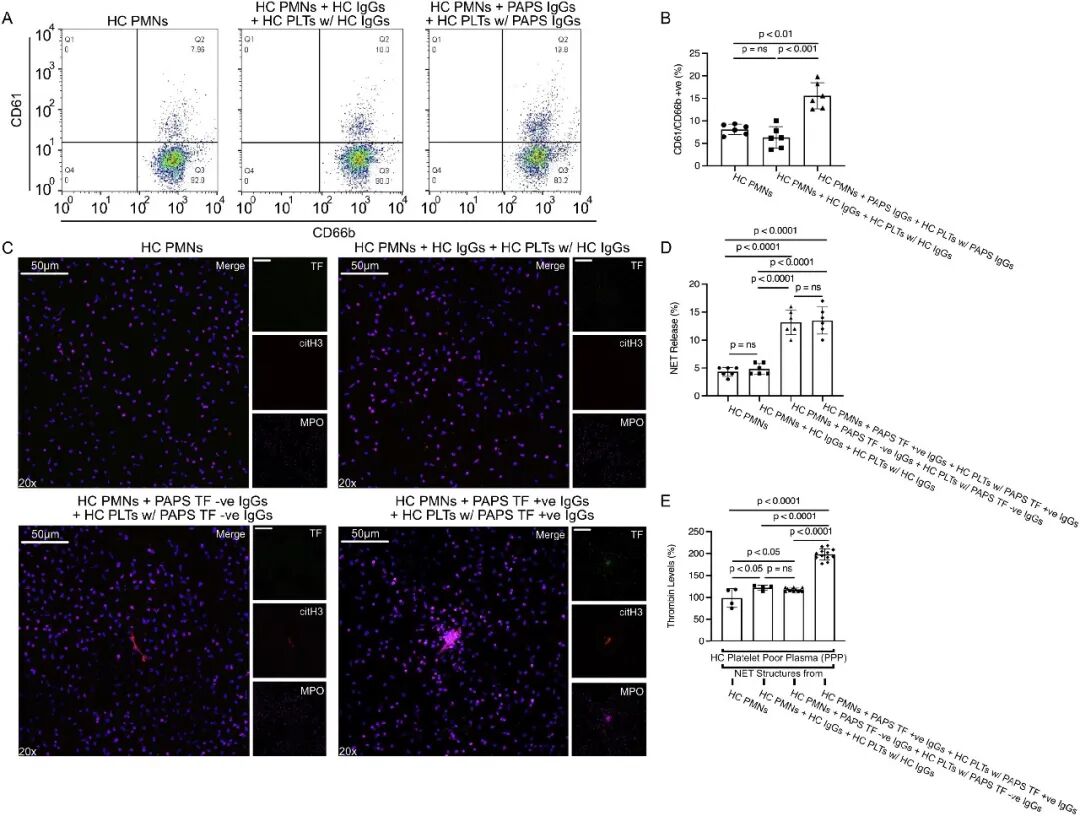
4A & 4B:aPL IgG处理过的血小板能显著增加与中性粒细胞的聚合形成(PNCs)。
4C & 4D:aPL先诱导中性粒细胞表达TF,再通过aPL激活的血小板触发其释放,最终产生TF阳性的NETs。
4E:该过程产生的 NETs 具有显著的致凝血酶生成能力。
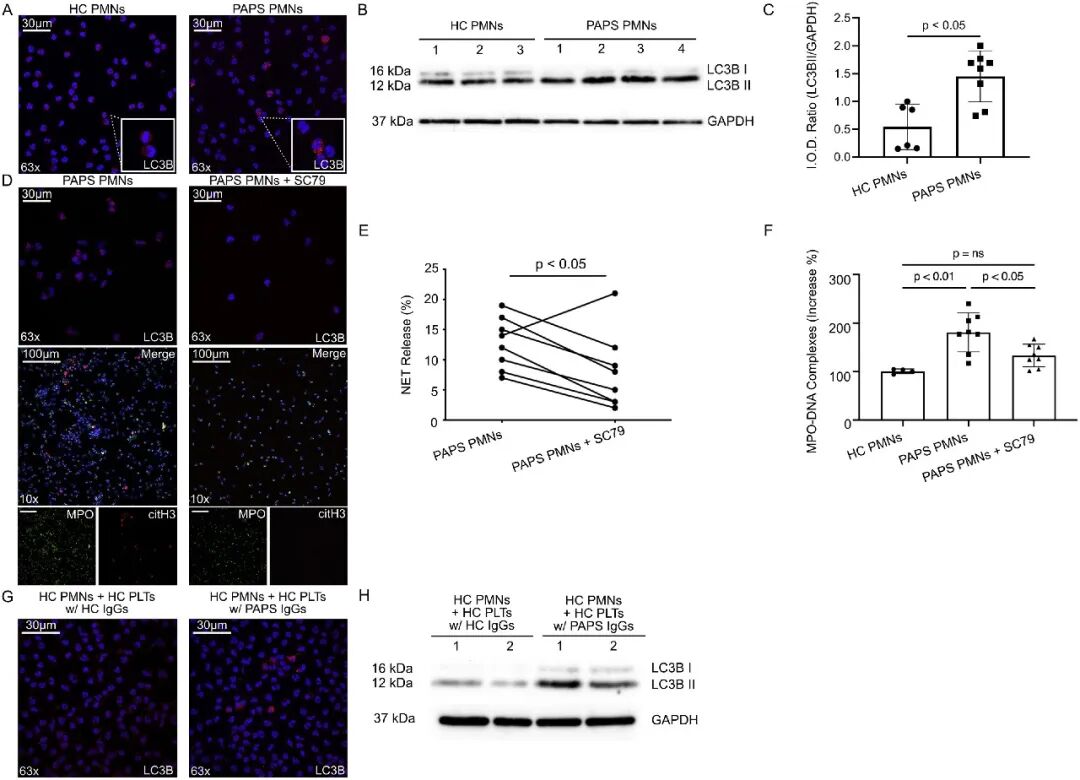
5A-5C:PAPS 患者中性粒细胞的自噬标志物 LC3B-II 蛋白水平显著升高,且胞内可见点状自噬体。
5D-5F:使用自噬抑制剂 SC79 处理后,PAPS患者中性粒细胞释放 NETs 的能力被大幅抑制。
5G & 5H:证明被 aPL 激活的血小板可以通过接触直接诱导中性粒细胞发生自噬。
发现点6:阻断 CD40-CD40L 轴可消除血栓炎症
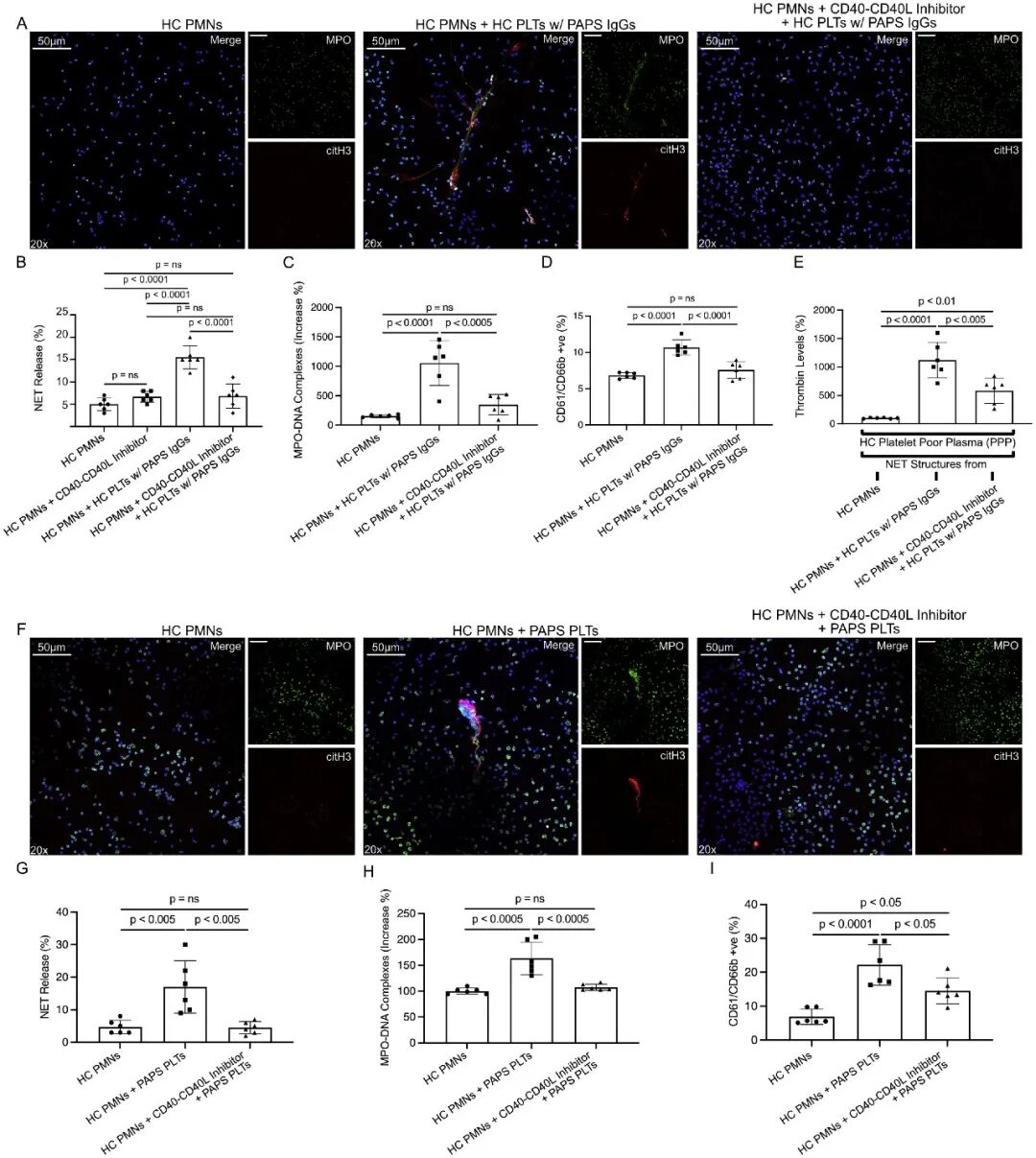
6A-6C:抑制剂DRI-C21045能显著减少由aPL处理血小板诱导的中性粒细胞NETs释放。
6D:该药物成功阻断了PNCs的形成。
6E:抑制剂干预后,NETs诱导的凝血酶生成水平显著下降。
6F-6I:使用PAPS患者来源的真实血小板进行重复实验,DRI-C21045 同样能有效减少NETs产生、PNCs形成及后续凝血反应。
发现点7:CD40-CD40L 阻断在 APS 小鼠模型中的表现
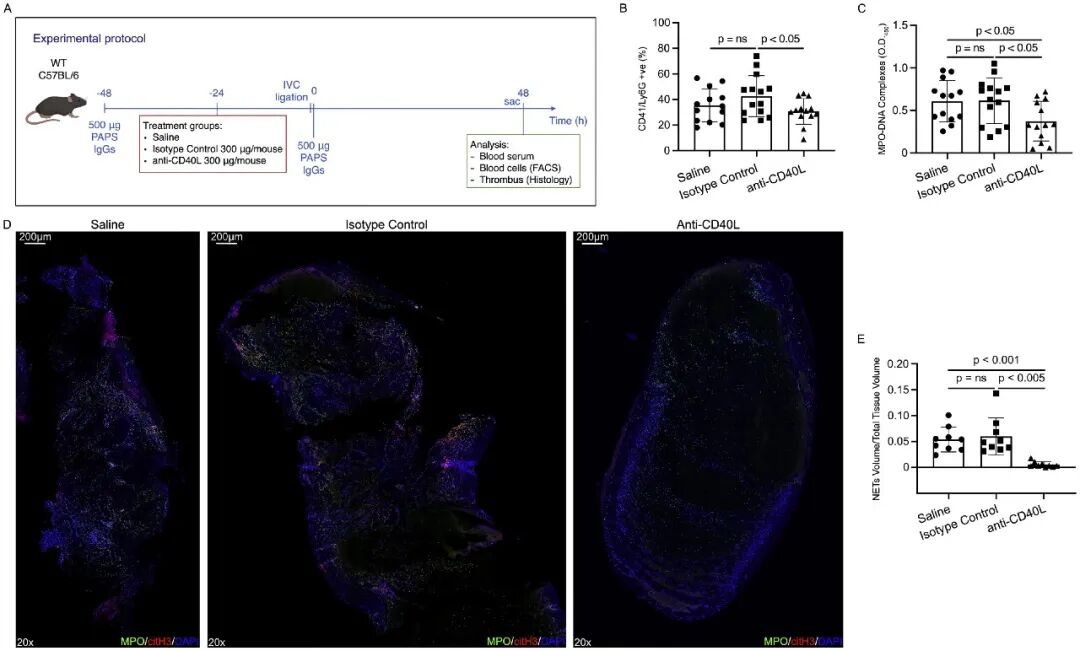
7A:注射PAPS IgG并结扎下腔静脉,同时给予anti-CD40L抗体治疗。
7B:抗体治疗组小鼠体内的血小板-中性粒细胞复合物(CD41+/Ly6G+)显著减少。
7C:治疗组小鼠血清中的MPO-DNA 复合物(NETs)水平显著降低。
7D & 7E:治疗组小鼠形成的血栓中,NETs的体积密度(MPO/citH3 染色)显著下降,血栓成分发生改变。
Innovation & Takeaway
✨ 创新点
1、证明了 PAPS 患者中性粒细胞能释放带有生物活性的 TF-NETs。
2、阐明了“aPL → 血小板激活 → CD40L/CD40 交互 → 中性粒细胞自噬 → TF-NETs 释放”这一完整的促栓轴。
3、证实了 CD40-CD40L 抑制剂作为 APS 新疗法的潜力。
✨ 科研启示
本研究强调了先天免疫(中性粒细胞/NETs)与凝血系统(血小板/TF)之间的密切互作,为“血栓炎症”(thromboinflammation)学说提供了有力支撑。
✨ 临床/应用价值
对于抗凝治疗无效或反复血栓的PAPS患者,靶向CD40-CD40L 轴的第二代抗体药物可能成为新的联合治疗方案。鉴于该类药物已在SLE临床试验中显示出安全性,其在APS中的转化前景值得期待。
局限性
1、研究人群(PAPS患者、无症状aPL携带者及健康对照)均为欧洲白人,限制了研究结果向其他族群的推广性。本研究样本量有限,可能缺乏检测某些潜在关联(如NET释放与特定aPL亚型或临床表型之间关系)的统计效能。
2、在小鼠模型中,虽然CD40-CD40L抑制显著减少了血栓中的NETs沉积和外周血NETs水平,但血栓的体积和重量在统计学上并未显著减少。研究者推测可能是观察时间点太短,未能观察到血栓消退,但这使得该干预手段在“直接溶栓”或“减小血栓负荷”方面的有效性缺乏直接证据支持。
医脉通是专业的在线医生平台,“感知世界医学