嗜酸性粒细胞性胃肠疾病(EGIDs)是一种以胃肠道嗜酸性粒细胞异常浸润为特征的慢性炎症性疾病。根据炎症仅局限于食管还是累及其他胃肠道节段,分为嗜酸性粒细胞性食管炎(EoE)与非EoE EGIDs(non-EoE EGIDs)。近30年来,EGIDs发病率与患病率持续上升且未见平台期,尤以EoE为著,已迅速成为消化领域的研究热点。近日,发表于Gastroenterology(IF:25.1)的一篇综述文章系统梳理了EoE和non-EoE EGIDs在流行病学、自然病程及危险因素方面的最新进展,并结合最新临床指南更新治疗策略,为未来的研究方向提供参考。本文重点整理EoE和non-EoE EGIDs诊断和治疗策略进展部分,以供临床参考。
历史上,EGIDs的命名一直存在模糊性。2022年国际首个EGIDs共识命名系统将“EGID”确立为该疾病类别的统称,分为EoE和non-EoE EGIDs,后者又根据累及部位进一步细分为嗜酸性粒细胞性
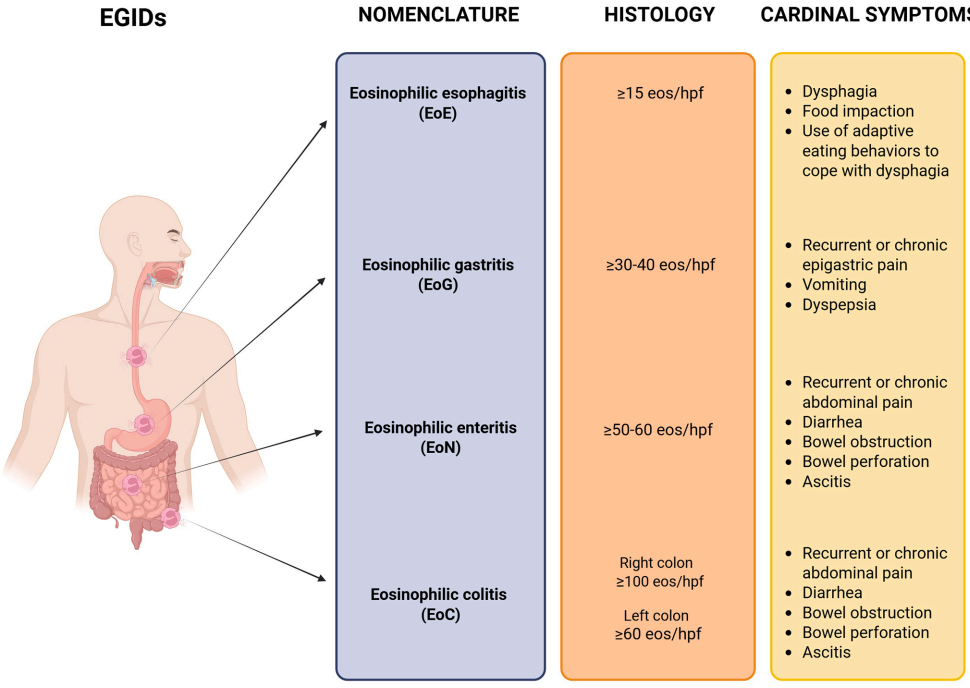
图1 EGIDs的命名、组织学诊断临界值及主要症状
EGIDs的诊断基于其是慢性免疫介导性疾病的概念,临床表现为胃肠道症状,组织学上以嗜酸性粒细胞为主的炎症病理性增加为特征。
•EoE:EoE的诊断需满足食管功能障碍症状、食管活检每高倍视野嗜酸性粒细胞≥15个(eos/hpf),并排除其他导致食管嗜酸性粒细胞增多的竞争性病因。诊断时可采用EoE严重程度指数(I-SEE)评估病情。
•non-EoE EGIDs:non-EoE EGIDs诊断过程更具挑战性,总体诊断思路与EoE相似:胃肠道症状与病变部位相关、活检提示胃肠道嗜酸性粒细胞病理性升高,并排除其他导致胃肠道嗜酸性粒细胞增多的疾病。
目前已有学者提出了病理性嗜酸性粒细胞增多的临界值(图1),总体规律为:从胃到回肠末端/盲肠区域,正常嗜酸性粒细胞数量呈递增梯度(该区域正常数量最高),自右半结肠到左半结肠呈递减梯度。嗜酸性粒细胞数量越高,对EGIDs的诊断特异性越高,特别是合并慢性炎症组织学特征时。
现阶段建议的诊断临界值如下:胃部≥30-40 eos/hpf,十二指肠≥50-60 eos/hpf,回肠末端≥60 eos/hpf,盲肠和右半结肠≥100 eos/hpf,左半结肠≥60 eos/hpf,相关国际共识指南仍在制定中。
EoE的治疗终点包括改善症状、内镜下表现、嗜酸性粒细胞炎症以及生活质量。因此,任何治疗方案调整后均需复查食管活检评估疾病活动度。EoE推荐治疗方案包括质子泵抑制剂(PPIs)、吞服性局部皮质类固醇(STCs)、食物排除饮食(FEDs)、单克隆抗体及食管扩张术(图2)。
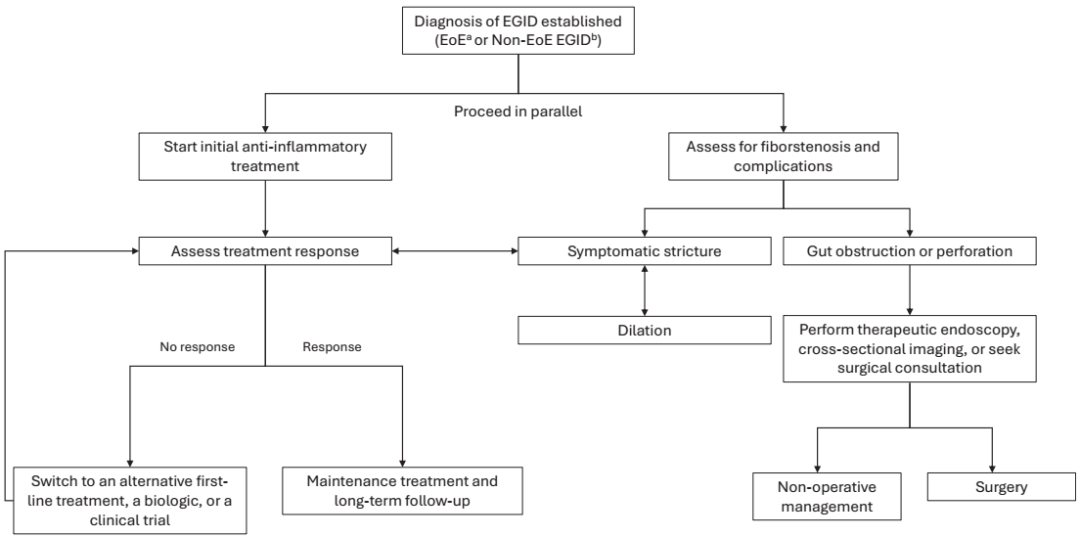
图2 EGIDs管理流程图
药物与FEDs可诱导并维持组织学缓解,而扩张术无法改善组织学疾病活动度,不建议作为单一治疗方案。由于缺乏头对头对照试验,所有药物治疗与FEDs均为EoE潜在一线及维持治疗方案,尽管各国指南存在差异,生物制剂通常作为升级治疗选择(表1)。
表1 最新EoE治疗指南及其主要建议
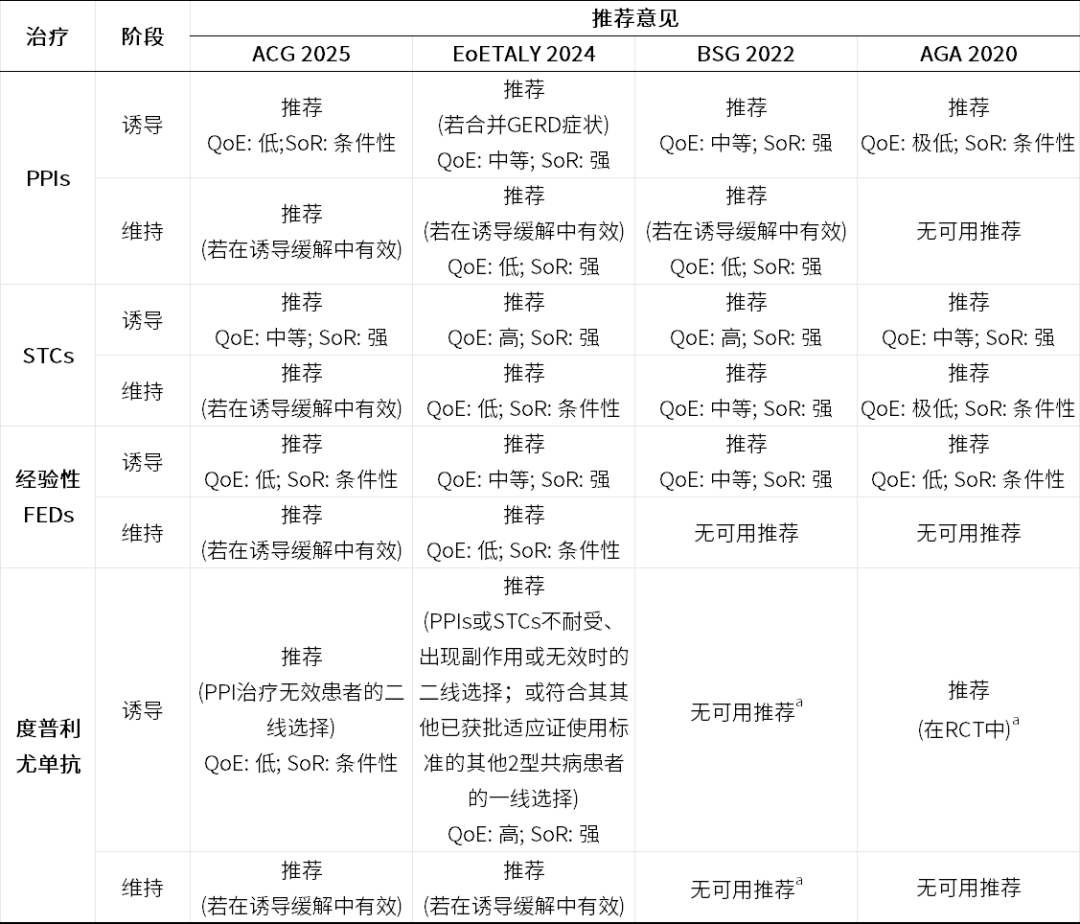
ACG:美国胃肠病学会;AGA:美国胃肠病学协会;BSG:英国胃肠病学会;EoETALY:意大利嗜酸性粒细胞食管炎诊断与管理指南;QoE:证据质量;SoR:推荐强度
•PPIs
PPIs为全球范围内EoE常用一线治疗药物,尽管其耐受性良好且可及性高,但目前用于EoE仍属超说明书用药。其可通过多种机制减轻食管炎症:减少胃酸反流以修复黏膜屏障、减少环境过敏原暴露;抑制嗜酸性粒细胞趋化因子3介导的食管嗜酸性粒细胞募集;降低信号转导与转录激活因子6(STAT6)表达;激活在2型辅助性T细胞介导反应中发挥作用的芳香烃受体;抑制钾转运腺苷三磷酸酶α链2(ATP12A),非胃型P2型H+、K+-腺苷三磷酸酶。
•STCs
STCs治疗理念为通过抗炎药物涂布食管发挥疗效,多项研究证实该方案有效。早期RCT证实,原本设计用于治疗哮喘,后调整用于EoE的超说明书STCs具有疗效。近年来,食管特异性STCs制剂相继获批,包括于2018年在欧洲获批的布地奈德口崩片(BOT)和2024年在美国获批的布地奈德口服混悬液(BOS)。
•单克隆抗体
随着对EoE发病机制认识的深入,多种靶向食管炎症介质的生物制剂已开展RCT研究,其中奥马珠单抗、美泊利珠单抗、瑞替珠单抗、本瑞利珠单抗和莱瑞利单抗未能达到组织学或症状学主要终点。然而,这些RCT表明EoE并非IgE介导,且嗜酸性粒细胞耗竭并不总能转化为临床或内镜改善,提示非嗜酸性粒细胞效应在EoE发病机制中发挥关键作用。
目前美国与欧洲唯一获批用于EoE的生物制剂为度普利尤单抗,系人源IgG4单克隆抗体,通过结合白细胞介素4(IL-4)受体α亚基同时靶向IL-13与IL-4信号通路。该药通过皮下注射给药,获批用于年龄≥1岁、体重≥15kg的EoE患者。
•FEDs
EoE为迟发型超敏反应、淋巴细胞驱动的2型疾病,规避食物诱因可诱导缓解。FEDs的核心理念是识别和避免患者特定的食物诱因。然而,由于EoE并非IgE介导,现有过敏检测(包括皮肤点刺试验、斑贴试验和血清免疫球蛋白检测)无法识别EoE的食物诱因,不推荐用于治疗决策。要素配方饮食通常仅用于婴儿或难治性患者,目前推荐的策略是经验性排除饮食,即去除EoE最常见的部分或全部诱因(如牛奶、小麦、鸡蛋、大豆、坚果和海鲜)。
non-EoE EGIDs的管理具有挑战性,原因在于缺乏确定的治疗终点、经过验证的结局指标以及导致批准治疗的成功RCT。因此,目前non-EoE EGIDs的管理主要基于小型病例系列和观察性研究的低质量证据。总体而言,皮质类固醇是non-EoE EGIDs的主要治疗方法,但也有非类固醇治疗的初步数据,包括FEDs、生物制剂、PPIs、肥大细胞稳定剂和免疫调节剂。肠道穿孔或梗阻患者可能需要手术干预。
•皮质类固醇
观察性研究中全身和局部皮质类固醇均已用于治疗non-EoE EGIDs。全身泼尼松(剂量高达60mg/天,随后在4-6周内逐渐减量)可诱导缓解,且不受肠道受累模式的影响,缓解率范围为50%-100%。由于non-EoE EGIDs可呈反复/复发或持续病程,常需长期治疗。在此背景下,局部皮质类固醇可能提供一种全身性不良事件较少的替代治疗方案。布地奈德肠溶剂型剂量范围为每天0.25-9mg,可通过调整给药方式以改善黏膜嗜酸性粒细胞增多、症状和内镜异常。
•FEDs
首项针对EoG和EoN的前瞻性饮食试验近期发布。该研究纳入15例组织学和临床活动期EoG或EoN或两者兼有的患者,评估为期6周的要素饮食疗效。所有患者均达到组织学缓解,多数患者观察到显著的内镜和症状改善。此外,重新引入食物常诱发疾病复发,支持食物抗原在EoG和EoN发病机制中的核心作用。
•单克隆抗体
近期一项度普利尤单抗治疗成人及青少年EoG的II期随机对照试验显示,与安慰剂相比,该药可改善组织学和内镜表现。尽管该研究在检测症状改善方面效力不足,但观察性研究报告了度普利尤单抗对non-EoE EGIDs的疗效,总体症状结局良好。
尽管目前没有维得珠单抗相关在研试验,但在小型病例系列中,该药对依赖或难治于其他甾体或生物制剂治疗的non-EoE EGIDs显示出诱导临床和组织学缓解的疗效。
•其他非甾体、非生物制剂治疗
已有关于使用PPIs、肥大细胞稳定剂、白三烯拮抗剂和免疫调节剂治疗non-EoE EGIDs的报告,病例报告/系列结果不同:
✓PPIs:一项累及食管的EoN病例报告显示PPIs减少了食管和十二指肠嗜酸性粒细胞增多,提示其可抑制十二指肠上皮细胞IL-4及IL-13信号通路。
✓肥大细胞稳定剂:早期报道显示,肥大细胞稳定剂(色甘酸钠、酮替芬)对EoG、EoN或EoC患者具有临床及组织学疗效。
✓白三烯拮抗剂:孟鲁司特据报道可改善与non-EoE EGIDs相关的症状。
✓免疫调节剂:硫唑嘌呤、6-巯基嘌呤在non-EoE EGIDs中已有探索,但研究结果存在矛盾。
总体而言,指南强调,目前数据不足以推荐或反对将上述任何药物用于non-EoE EGIDs的治疗。
目前多项针对EoE与non-EoE EGIDs的新型治疗策略正在研发中,包括:
✓新型局部皮质类固醇递送系统:如含糠酸莫米松黏膜黏附薄膜的胶囊ESO-101(NCT04849390)、长效氟替卡松食管注射制剂EP-104GI(NCT05608681)及氟替卡松口腔崩解片APT-1011;
✓单克隆抗体:如Cendakimab(抗IL-13,NCT04753697、NCT05214768)、Tezepelumab(抗胸腺基质淋巴细胞生成素,NCT05583227)、Solrikitug(抗胸腺基质淋巴细胞生成素,NCT06598462)、Barzolvolimab(抗KIT,NCT05774184)及CALY-002(抗IL-15,NCT04593251);
✓小分子药物:如免疫重置肽1104(NCT05084963)、艾曲莫德;
✓钾离子竞争性酸阻滞剂(P-CABs)。