研究设计
本研究为病例报告结合系统文献回顾。首先报告一例2012年于法国某医院诊治的13岁男性NSLAH患儿,其携带SHOC2基因c.4A>G(p.Ser2Gly)突变,并出现符合美国风湿病学会SLE分类标准的临床表现。随后,作者系统检索PubMed数据库中1966年至2012年间发表的英文和法文文献,关键词包括“lupus”与“Noonan syndrome”或“RASopathy”。纳入标准为:患者同时符合SLE的ACR分类标准和RAS病的临床或分子诊断标准。共纳入7篇文献,涉及7例患者,结合本病例共计8例进行分析。
研究结果
研究共纳入8例RAS病合并SLE患者,其中男性4例,女性4例,男女比例为1:1。SLE发病年龄范围为5至32岁,涵盖儿童期至成年早期(表1)。
表1:RASopathy与 SLE 患者的人口学、临床和生物学特征
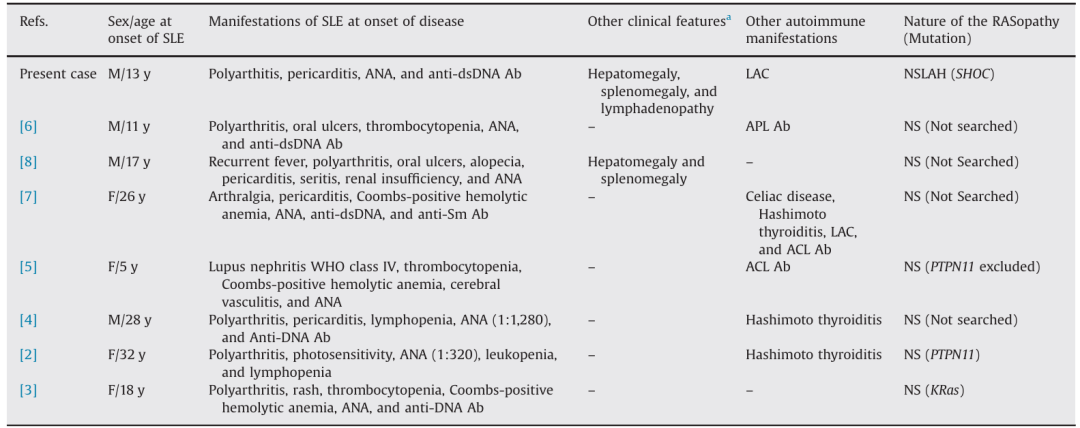
最常见的SLE表现为多
分子诊断方面,3例患者进行了基因检测,分别发现PTPN11、KRAS及SHOC2基因突变(本病例)。其余患者基于典型临床表现诊断为NS。
研究结论
本研究报道一例SHOC2基因突变相关NSLAH患儿并发SLE的病例,并结合文献回顾,共收集8例RAS病合并SLE的患者。结合两种罕见病的共现频率及RAS病患者中自身抗体阳性率较高的现象,提示RAS病可能为SLE的新的单基因易感条件。与经典SLE相比,该类患者具有更高的男性比例(1:1)、较低的皮肤受累率(1/8例)及较高的心包炎发生率(4/8例),部分患者还伴有良性淋巴增殖性疾病(如RALD)或其他自身免疫病(如桥本甲状腺炎)。
研究讨论
本研究通过对一例SHOC2突变相关NSLAH患儿的病例分析及文献回顾,系统探讨了RAS病与SLE之间的潜在关联。RAS病是一类由RAS/MAPK信号通路基因突变引起的神经发育综合征,既往研究多聚焦于其发育异常和肿瘤易感性,而其在自身免疫领域的作用尚未引起足够重视。近年来,相关研究显示,在42例RAS病患者中,52%存在至少一种自身抗体,其中5例ANA阳性,3例狼疮抗凝物阳性,提示RAS病患者可能存在潜在的免疫失调状态。这一发现为本研究提供了重要的背景支持。
值得注意的是,本研究中SLE的临床表现与传统SLE存在一定差异。首先,男女比例接近1:1,显著低于经典SLE的9:1女性优势,提示该类SLE可能具有不同的发病机制。其次,皮肤受累率仅为1/8,而心包炎和自身免疫性血细胞减少则更为突出。这些特征可能与RAS/MAPK通路在免疫细胞发育和功能调控中的多重作用有关。例如,RAS通路的异常激活可影响T细胞受体信号传导、调节性T细胞功能及B细胞耐受性,进而促进自身免疫反应的发生。
此外,本研究还发现部分RAS病患者合并良性淋巴增殖性疾病,表现为淋巴结肿大、肝脾肿大及自身抗体阳性,符合RAS相关自身免疫淋巴增殖综合征样疾病的表现。已有研究报道,体细胞NRAS或KRAS突变可导致RALD,其特征与本研究中的部分患者高度相似。这进一步支持RAS/MAPK通路异常在自身免疫病发病中的作用。
从临床角度看,RAS病患者若出现多关节炎、心包炎或血细胞减少等表现,应警惕合并SLE的可能。反之,对于早发SLE,尤其是男性患者或伴有发育异常者,也应考虑是否存在潜在的RAS病。早期识别有助于制定个体化治疗方案,如本病例中使用
研究存在受样本量较小、部分患者缺乏基因检测及长期随访数据等局限性,为全面评估该类SLE的疾病演变规律与治疗反应,仍需进一步开展多中心前瞻性研究,结合基因型-表型分析,进一步阐明RAS/MAPK通路异常在SLE发病中的具体机制。
本研究提示RAS病可能为SLE的新的单基因易感条件,其临床表现具有独特性。RAS病的深入研究不仅有助于揭示SLE的遗传异质性,也可能为开发新的靶向治疗策略提供线索。
参考文献:Bader-Meunier B, Cavé H, Jeremiah N, Magerus A, Lanzarotti N, Rieux-Laucat F, Cormier-Daire V. Are RASopathies new monogenic predisposing conditions to the development of systemic lupus erythematosus? Case report and systematic review of the literature. Semin Arthritis Rheum. 2013 Oct;43(2):217-9.
医脉通是专业的在线医生平台,“感知世界医学
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)