在HBV慢性感染过程中,部分HBV基因片段可整合至宿主基因组,其中部分整合的HBV基因能够表达病毒相关产物,如乙型肝炎小包膜蛋白[
慢性病毒感染的基础在于不断产生子代病毒,或病毒暂处于潜伏状态但在外界环境刺激后重新激活而产生子代病毒,以维系病毒在个体中的持续感染以及个体间的病毒传播。由于整合的HBV基因不能产生具有感染性的子代病毒,因而,维持持续性HBV感染的核心在于cccDNA。HBV cccDNA长度仅约3.2 kb,只存在于肝实质细胞的细胞核内,其生物学特性主要受到肝细胞内因子的调控,同时也受肝脏中肝巨噬细胞、免疫细胞等(即非肝实质细胞,non-parenchymal cell)的影响。已有研究表明,在cccDNA分子层面,其结构和功能并非均一而是高度异质的。基于cccDNA的基本生物学过程,其生命周期可简单划分为4个关键环节:合成、转录、消除及与非实质细胞的相互作用。其中,在肝实质细胞中,HBV cccDNA的形成、转录和消除是内因;而非实质细胞作为外因,可显著影响以上3个过程。本文重点阐述目前对cccDNA生命周期分子机制的框架认识,并指出未来需要解决的重点问题。
cccDNA的生命周期主要包括合成、转录、清除以及与非实质细胞的相互作用等关键环节(图1)。在合成阶段,cccDNA由松弛环状双链DNA(rcDNA)修复形成,其来源主要有2种途径:(1)病毒感染进入肝细胞;(2)已感染细胞内的再合成过程。在转录阶段,cccDNA的转录受到宿主和病毒两类因子的共同调控,既可被促进也可能被抑制;且在不同肝细胞之间,cccDNA的转录活性存在显著异质性。在清除阶段,cccDNA可因通过细胞增殖或免疫清除等多种生理或病理机制被消除。此外,肝组织中的非实质细胞也参与调控cccDNA的稳定性,其可通过直接接触或间接分泌细胞因子等方式施加影响。
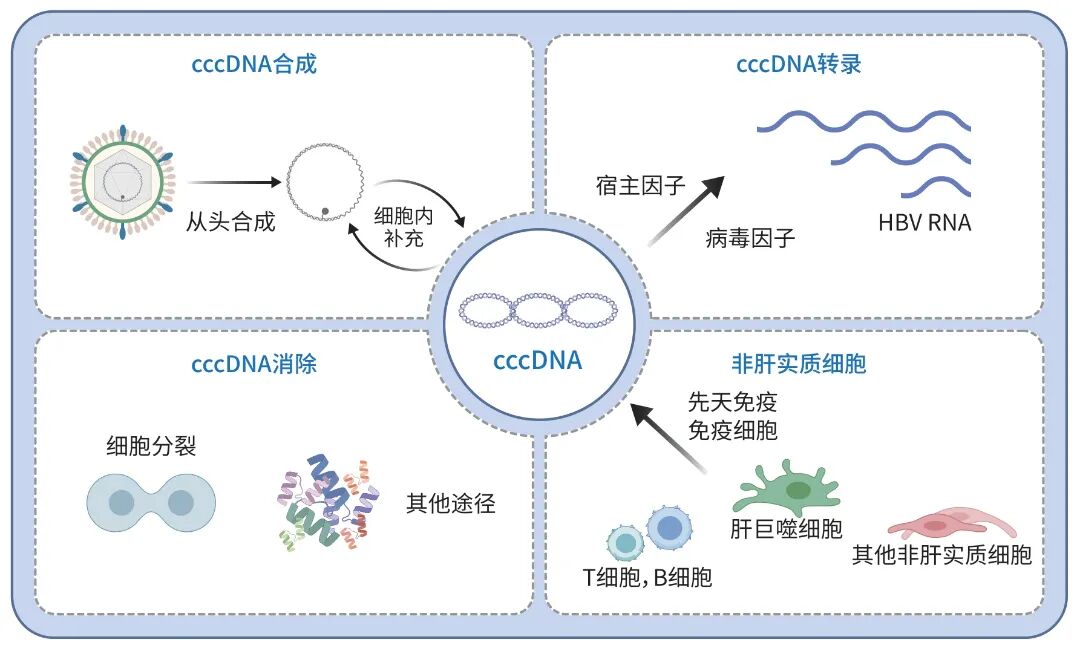
注: cccDNA,共价闭合环状DNA;HBV,乙型肝炎病毒。
图1 cccDNA生命周期的关键环节
1HBV cccDNA合成的关键分子机制
HBV cccDNA主要通过2种途径产生:(1)HBV病毒颗粒内包含rcDNA,以从头感染或再感染的方式通过受体钠离子-牛磺
尽管cccDNA合成研究已取得系列进展,但目前仍缺乏对cccDNA形成机制的深入理解。该领域尚存在一系列的科学问题有待解答,例如:病毒核衣壳在cccDNA形成过程中的作用及机制;参与cccDNA形成过程的宿主修复因子及调控因子,以及其具体的修复机制;哪些cccDNA形成环节中存在新靶点可作为潜在的药物设计位点等。为深入探究并更为有效地解答这些问题,需要建立能够高度模拟感染过程中cccDNA形成的体外研究模型,探索体外cccDNA微小
2HBV cccDNA转录调控的关键分子机制
HBV cccDNA以微小染色体的形式存在于细胞核中,其转录同样受到宿主和病毒因子两大类分子的共同调控。在转录活跃或非活跃时,cccDNA结合的组蛋白及宿主因子存在差异。cccDNA的转录活性受到组蛋白包装的调节、染色体结构维持蛋白5/6(SMC5/6)复合物和早幼粒细胞
尽管目前对cccDNA转录调控的分子机制研究已取得了长足的进展,但对于转录调控中的若干关键科学问题仍有待深入阐明,例如:cccDNA微小染色体的包装特征,SMC5/6复合体调控cccDNA转录沉默的分子机制,HBV X蛋白调节cccDNA转录的结构生物学基础,以及通过表观编辑抑制cccDNA转录的临床可行性。为实现对cccDNA转录的有效沉默,未来亟需综合运用病毒学、生物化学等多种生物学手段,结合高通量测序与生物信息学分析,从单分子、单细胞以及组织学层面,深入解析cccDNA基因转录和沉默的精细分子机制,从而为开发靶向cccDNA的沉默新策略提供依据。
3清除cccDNA的关键分子机制
目前临床上广泛使用的核苷(酸)类似物药物等治疗手段虽然可以有效抑制HBV复制,但其无法靶向肝细胞内已存在的cccDNA。虽然基于不同研究系统对cccDNA半衰期的估计存在差异,但cccDNA如同所有生物分子一样,均遵循从产生到消除的生命周期规律。已有研究表明,在生理状态下,细胞增殖可引起cccDNA稳定性降低;在病理状态下,cccDNA可通过2种途径被自然清除:非溶细胞性降解和溶细胞性清除。在细胞和动物体内,可通过CRISPR系统对cccDNA进行编辑,或基于杀伤性T细胞直接消除感染细胞,从而实现cccDNA的清除。
尽管该领域的相关研究已取得显著进展,但cccDNA清除的关键分子途径仍有待阐明。为实现精准、有效地清除cccDNA,还需要回答多个重要科学问题,例如:在不同的细胞周期及细胞分裂中,哪些宿主因子参与调控cccDNA数量维持;在免疫压力下,哪些宿主细胞和因子通过何种机制参与及调控cccDNA的消除;HBV X蛋白及HBV核心抗原是否及如何参与维持cccDNA的稳定性;如何实现cccDNA的精准靶向清除,减少对非感染细胞副作用等。因此,未来需要建立研究cccDNA清除机制新的体内外模型,并研发新型靶向清除cccDNA工具,研究和理解cccDNA的清除机制,特别是阐明病毒因子和宿主因子调控cccDNA稳定性和降解的具体作用机制,并研发相应的干预手段,为最终实现HBV的消除提供支撑。
4宿主免疫与cccDNA相互作用的动态特征和相关机制
HBV病毒感染和宿主免疫的相互作用一直是乙型肝炎领域的重要研究课题。肝组织中的非肝实质细胞(包括免疫细胞)可通过两种方式影响肝内cccDNA:依赖直接接触的作用方式和非直接接触/细胞因子的作用方式。在慢性乙型肝炎患者中,其免疫系统对感染细胞的识别和清除能力显著下降。近年来,动物模型的不断发展,以及干扰小RNA、反义寡核苷酸和细胞治疗等新型治疗方式推进至临床研究阶段,为解析宿主免疫与cccDNA相互作用的动态特征及机制提供了新的机遇。
目前处于临床研发阶段的抗乙型肝炎反义寡核苷酸药物虽不富集于肝实质细胞,但可显著降低外周血病毒标志物(如HBsAg)的水平,其具体机制和长期影响等仍有待阐明。此外,诸如HBV特异性T细胞过继疗法等新型治疗对cccDNA清除的效应及机制尚需深入探索;患者在接受治疗前后,肝脏局部免疫特征以及其与cccDNA水平及功能状态的关系也有待系统研究。这些相关科学问题的深入研究,将有助于理解cccDNA动态特征的底层生物学事件,从而开发消除病毒储存库的新策略,最终实现HBV消除并防止复发。
5小结
消除HBV对人类健康的威胁,是人类公共卫生领域的一项艰巨任务。近年来,随着对HBV生物学特性认识的深入、宿主免疫系统新靶点的发现以及新药研发的持续推进,针对慢性HBV感染的策略正从单纯的长期控制HBV病毒复制向实现有限治疗疗程迈进。然而,相关基础科学研究仍待加强,将基础科学进展转化为安全有效的新型疗法仍面临诸多挑战,包括在临床研究和实践中如何优化联合治疗策略以实现协同效应、如何平衡免疫激活与
本期专刊中还包括4篇从不同维度探讨消除乙型肝炎危害的专家论坛,提供对消除HBV危害的关键科学问题与突破路径的深入思考及真知灼见。相信随着科学技术的不断进步和多学科的交叉融合,人类最终将战胜乙型肝炎这一长期威胁健康的疾病,最终实现消除乙型肝炎危害的目标。