铁过载是长期
铁过载评估困境,临床标准亟待循证支撑
非恶性
临床实践中,血清铁蛋白因检测便捷常作为筛查工具,而通过MRI测定的LIC则被视为反映全身铁负荷的金标准,并被许多中心及临床研究用作移植准入的参考指标。然而,LIC测定在幼儿中操作困难,且既往研究并未在儿童NMHD群体中明确证实LIC与不良移植结局的关联。同时,铁蛋白作为急性期反应蛋白,其水平易受炎症干扰,特异性存疑。这种背景下,厘清铁蛋白与LIC孰能更有效预测移植风险,成为优化患儿围移植期管理、避免不必要治疗延误的关键科学问题。
核心发现:铁蛋白预后价值凸显,LIC金标准地位受挑战
本研究利用PEDSnet健康医疗网络数据,对2010年至2023年间接受首次HSCT的NMHD患儿进行了分析。最终,580名拥有移植前铁蛋白测量值的患者和260名拥有移植前LIC测量值的患者被纳入主要分析。研究定义高铁蛋白为>2500 ng/mL,高LIC为>5 mg Fe/g dw。核心发现围绕铁蛋白与LIC的预后预测能力展开。
如图1所示,在多中心队列中,移植前铁蛋白>2500 ng/mL(高铁蛋白组)的患儿,其3年总生存率为86.4%,显著低于铁蛋白≤2500 ng/mL组(92.9%),经年龄、性别、预处理方案、供体类型校正后,死亡风险比(HR)高达2.31,p=0.04。进一步亚组分析显示,这种生存差异仅在重度
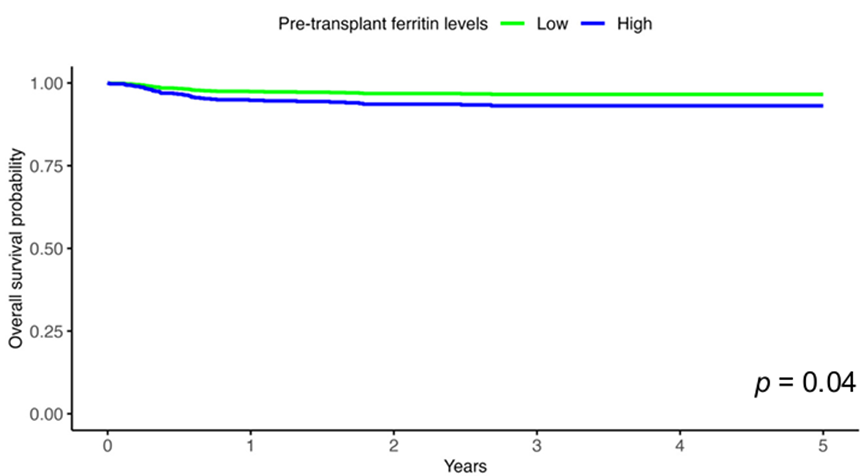
图1 高铁蛋白与较低的总生存率相关
研究评估了移植后一年内的菌血症发生情况。在整个队列中,高铁蛋白与菌血症风险增加相关(HR 2.18,p=0.005)。值得注意的是,在SAA亚组中,这种关联尤为突出,菌血症风险比高达3.33(95% CI 1.72-6.44,p<0.001,图2)。而高LIC与菌血症风险,无论是在整体队列还是在任何疾病亚组中,均未显示统计学关联。
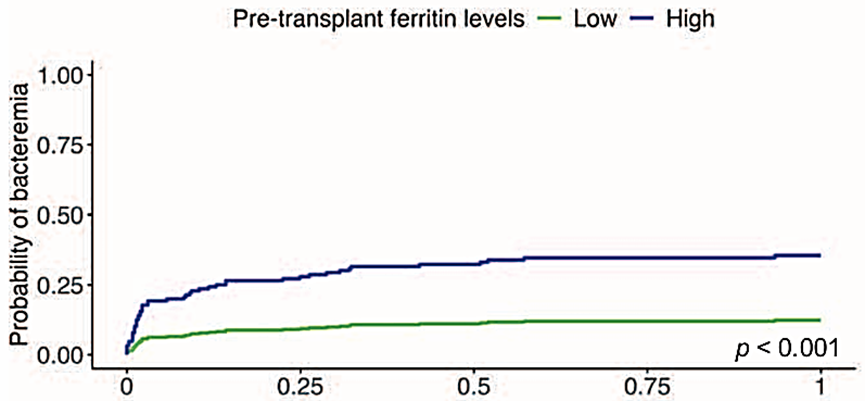
图2 高铁蛋白与SAA中菌血症的风险增加有关
其它结局:
移植物失败、植入时间、VOD风险与铁指标无显著关联
分析显示,高铁蛋白或高LIC与移植物失败发生率、中性粒细胞植入时间均无统计学关联。静脉闭塞性疾病(VOD)的风险分析仅限于接受
在移植前同时检测了两种指标的患儿中,铁蛋白与LIC的相关系数较低(r=0.22),提示在临床实践中两者一致性有限。此外,数据显示移植后铁过载现象常见:在多中心分析中,63%的患儿在移植后出现铁蛋白升高(>1000 ng/mL),68%的患儿LIC升高(>5 mg Fe/g dw),突出了移植后监测与干预的必要性。
在单中心接受移植后祛铁治疗的患儿中,使用
循证重塑铁管理策略,围移植期研究仍需推进
本研究通过对大规模儿科NMHD移植队列的实证分析,得出了可能影响临床实践的关键见解:
首先,研究结果对LIC作为铁相关移植风险分层的“金标准”角色提出了直接挑战。尽管LIC是量化肝脏铁储存的准确工具,但本研究未发现其与生存、严重感染等短期核心移植结局存在统计学关联。这促使我们重新审视,将特定LIC阈值作为移植绝对准入限制的合理性。
其次,研究确立了移植前高铁蛋白水平,特别是>2500 ng/mL,在NMHD患儿,尤其是SAA患儿中,是不良预后(生存率降低、菌血症风险增加)的重要风险标志。虽然铁蛋白水平受炎症状态影响,但其与硬性结局的强烈关联(p<0.05)使其成为一个不容忽视的预警信号。对于SAA伴高铁蛋白的患儿,强化移植后感染预防策略或具必要性。
最后,研究揭示了移植后铁过载的高发生率,并初步表明螯合与放血疗法均为有效的祛铁选择,为临床个体化决策提供了参考。
综上所述,本研究呼吁在HSCT日益成为NMHD常规治疗选择的时代,亟需开展前瞻性研究,以建立更精准的围移植期铁过载评估与管理体系。未来的工作应致力于区分铁负荷与炎症对铁蛋白的影响,并探索能更好预测临床结局的综合生物标志物,从而最终实现移植风险分层与治疗决策的精细化与最优化。
参考文献:
1. Gibson NM, et al. Impact of Iron Overload on Hematopoietic Stem Cell Transplant in Children with Non-Malignant Hematological Disorders. Blood Adv. 2026 Feb 4: blood advances.2025017942.

戳“阅读原文”,查看更多内容
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)