

1HBV基因组和生活周期(图1)
HBV是一种带包膜的DNA病毒,基因组全长约3.2 kb,为松弛环状双链DNA(rcDNA),包含4个开放阅读框(ORF):聚合酶、表面蛋白(S)、前核心(preC)/核心(C)和X。HBV感染肝细胞后,通过与肝细胞表面的硫酸乙酰
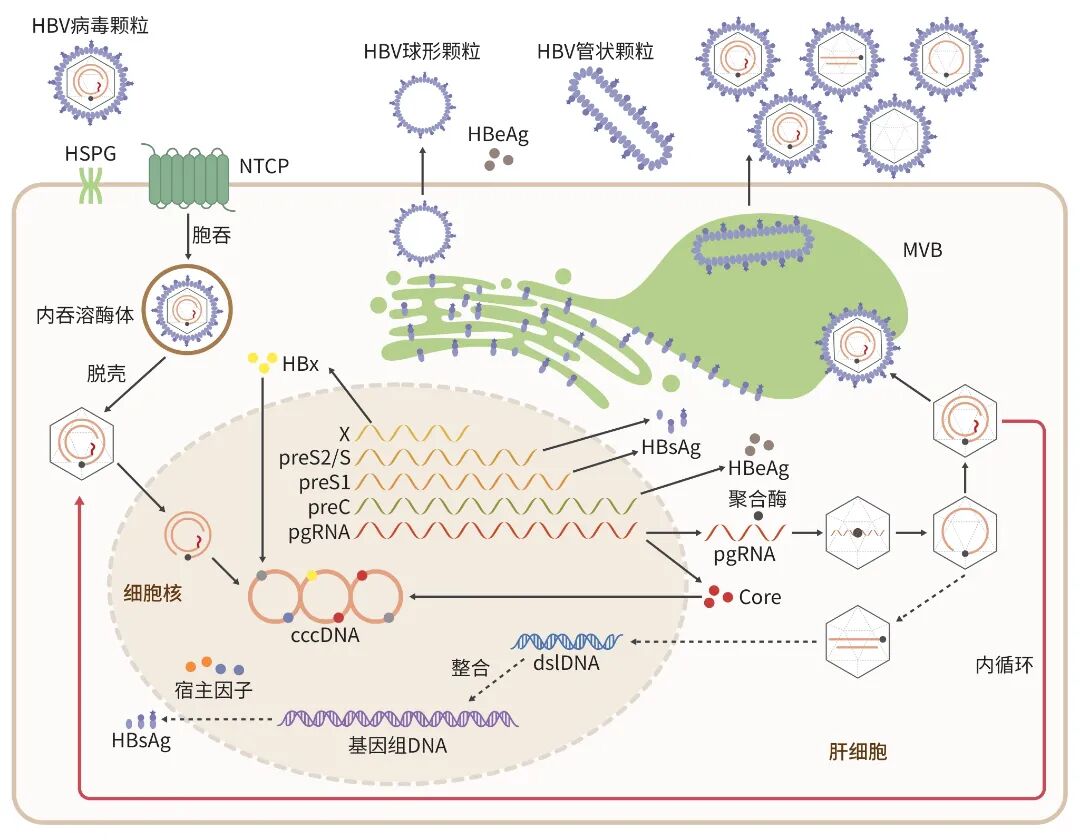
注: HBV生活周期包括病毒吸附、进入、脱衣壳、向细胞核的运输、cccDNA形成、转录、翻译、组装、分泌和整合。HBV,乙型肝炎病毒;HSPG,硫酸乙酰肝素蛋白聚糖;NTCP,钠离子-牛磺胆酸共转运多肽;HBeAg,
图1 HBV生活周期

2HBV动物模型
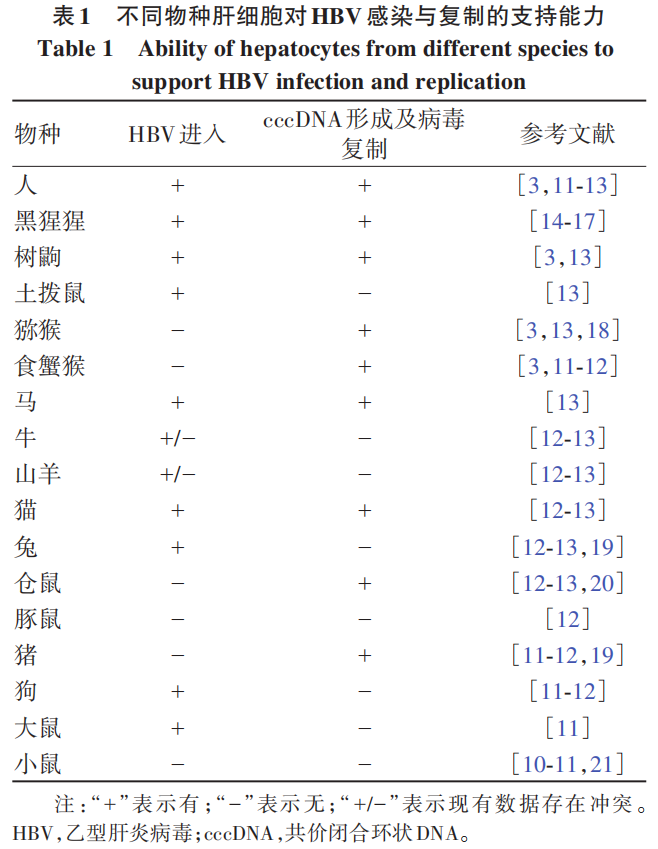
HBV感染具有严格的种属特异性,目前仅能在人类和黑猩猩中发生自然感染。研究表明,不同物种来源的肝细胞对HBV感染的易感性主要受到2个关键环节的限制:(1)受体介导的病毒内吞进入细胞;(2)病毒进入后至cccDNA形成的过程(表1)。以小鼠肝细胞为例,研究证实其中第2个限制环节主要涉及病毒核衣壳的分解与去组装。一旦cccDNA成功形成,后续的病毒复制过程通常不再受到明显限制。然而,目前尚缺乏能够完整支持HBV感染周期,并能真实模拟宿主免疫反应与疾病进展的动物模型。因此,建立易于操作、成本合理的实验动物模型对于HBV相关研究具有重要意义。
研究显示,即使一个病毒基因组当量的HBV便足以成功感染黑猩猩。感染HBV后,黑猩猩会出现与HBV感染者中非常相似的免疫反应和炎症特征,并且可以造成急性和慢性感染。急性感染期间的病毒清除主要通过非细胞毒性抗病毒机制,清除HBV复制中间体和cccDNA实现;进展为慢性感染的黑猩猩血清和肝组织中可以检测到病毒抗原和核酸,同时出现与HBV感染者中相似的门静脉周围炎症反应。然而,由于价格昂贵、体型较大以及动物伦理学等问题,使黑猩猩模型在HBV动物模型中的研究应用受到限制。
树鼩能在实验条件下感染HBV,并且会出现短暂性病毒血症、病毒清除以及乙型肝炎表面抗原血清学转换。尽管新生树鼩感染HBV后可出现低病毒血症的慢性感染,但是成年树鼩感染HBV后多为一过性感染,且病毒复制水平较低、维持时间较短。
猕猴能支持较长时间的HBV复制。然而,猕猴肝细胞并不支持HBV感染,过表达人源NTCP(hNTCP)后可支持HBV的感染并完成整个生活周期,表明NTCP是关键限制因子。Müller等将猴NTCP第158位
小鼠是研究中最常用的动物模型,但其本身并不能直接感染HBV。即使在小鼠肝细胞中过表达hNTCP或hNTCP转基因,小鼠仍不支持HBV感染。研究表明,小鼠肝细胞除了缺少病毒进入受体之外,在其细胞质中病毒核衣壳无法解离是限制HBV感染的重要原因。尽管如此,研究人员已建立一系列小鼠模型,用于模拟HBV感染或复制过程中的部分环节,广泛应用于各类研究,包括HBV转基因小鼠模型、高压水动力注射介导的HBV转染小鼠模型、重组腺病毒(AdV)介导的HBV转导小鼠模型、重组腺相关病毒(AAV)介导的HBV转导小鼠模型、cccDNA替代小鼠模型、人-鼠嵌合肝脏小鼠模型以及人免疫系统和肝双人源化小鼠模型(表2)。
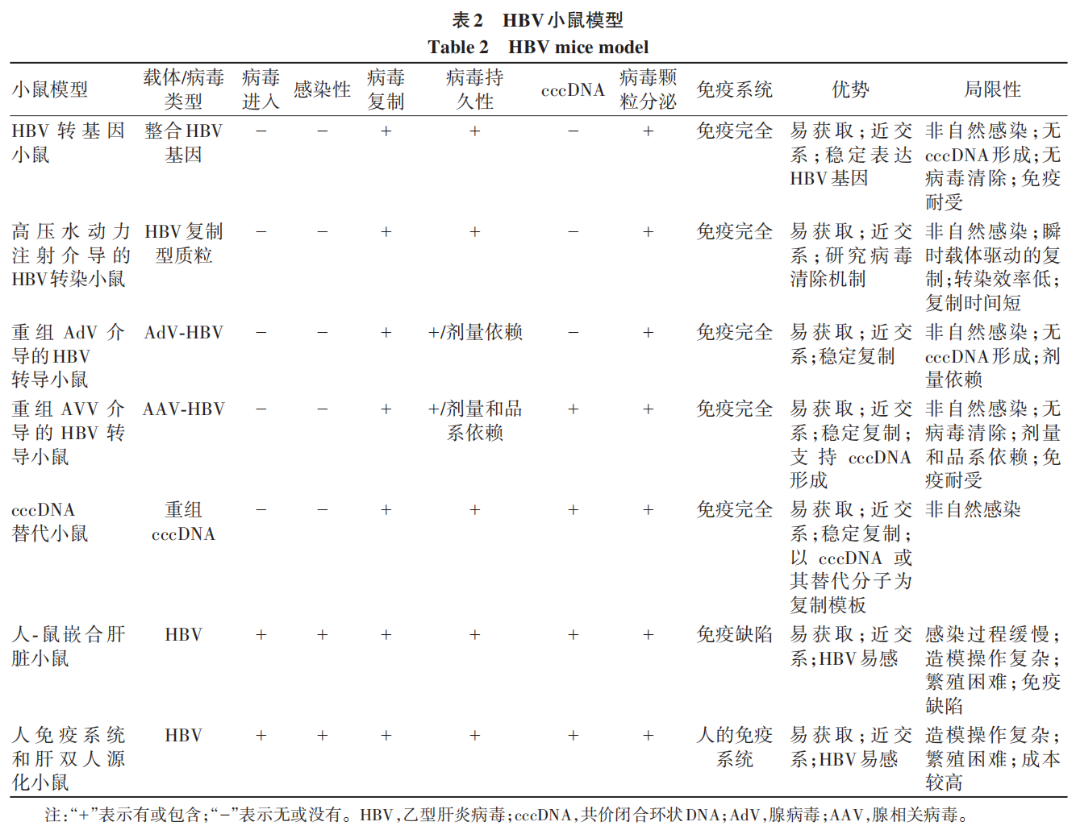
HBV转基因小鼠模型支持较高水平病毒复制并可产生完整病毒粒子。然而,该模型中的HBV感染并非自然获得、对HBV抗原天然免疫耐受且不能形成cccDNA,因此并不适于病毒感染和转录活性机制等方面的研究。高压水动力注射介导的HBV转染小鼠模型可在野生型小鼠中出现急性自限性反应,模拟HBV急性感染;而在免疫缺陷小鼠中,病毒复制状态可维持至少81 d。然而,该模型无法形成cccDNA,质粒骨架、小鼠品系等因素都会影响小鼠中HBV的复制持续时间。此外,高压水动力注射操作本身会引起较为严重的肝组织损伤,可能干扰对发病机制和免疫应答等实验结果的判断。重组AdV介导的HBV转导小鼠模型中急性和慢性感染的建立取决于病毒注射剂量。然而,该模型中无法形成cccDNA,载体编码的非HBV病毒蛋白产物可能刺激机体免疫应答,进而存在HBV被清除的风险,从而干扰对HBV诱发免疫反应的判断。重组AAV介导的HBV转导小鼠模型可模拟慢性HBV感染的部分病毒学和免疫学特征,同时可通过同源重组形成cccDNA。然而,该模型仍缺少HBV感染进入过程,且病毒复制的主要模板并非cccDNA。cccDNA替代小鼠模型是由研究人员开发出的用于替代cccDNA研究的小鼠模型,包括重组cccDNA、HBVcircle和时空控制的重组cccDNA。然而,这些模型形成的cccDNA分子与野生型cccDNA仍然存在区别。Xu等建立的AAV-HBV1.04小鼠模型,可通过宿主
基于对HBV动物模型的迫切需求,研究人员扩大了筛选宿主范围。Chen等研究发现,来源于土拨鼠、雪貂、土豚、马、兔、鲸鱼、大棕蝙蝠、猫和犀牛的NTCP同源物在人肝癌细胞(HepG2)中异源表达后,可使其支持HBV感染。进一步研究表明,猫、猪和仓鼠有望被开发为新型动物模型。Xu等进一步评估了包括猫在内的多个物种的肝原代细胞对HBV的易感性,首次发现猫肝原代细胞支持HBV自然感染,同时猫肝细胞可用于抗HBV药物筛选。值得注意的是,尽管雪貂和兔的NTCP在HepG2细胞中异源表达后支持HBV感染,但是其肝原代细胞并不支持HBV感染,表明病毒进入后依然存在限制因素。Zhang等研究发现,仓鼠的NTCP 并不支持HBV感染,但过表达hNTCP后可支持HBV感染。猪NTCP同样不支持HBV感染,但在猪的肝原代细胞中过表达hNTCP可支持HBV的感染以及完整生活周期。深入的研究揭示了猪NTCP中限制与HBV相互作用的158位和167位氨基酸。此外,有研究指出,大鼠和狗的NTCP支持

3基于HBV相关嗜肝病毒的替代模型
HBV所属的嗜肝DNA病毒科包含与其他物种密切相关的嗜肝病毒,包括毛里求斯食蟹猴HBV(mcHBV)、绒毛猴HBV(WMHBV)、卷尾猴HBV(CMHBV)、土拨鼠肝炎病毒(WHV)、鸭乙型肝炎病毒(DHBV)、家猫肝炎病毒(DCH)和松鼠乙型肝炎病毒等。这些病毒与其自然宿主有望成为HBV感染的替代模型。
Dupinay等在毛里求斯岛发现了少量自然状态下可感染mcHBV的食蟹猴群。mcHBV与人HBV D基因型ayw3血清型的临床分离株序列的同源性高达99%,且mcHBV与人HBV preS1区第68位氨基酸的差异也是限制其感染的关键因素。Lanford等从患有暴发性肝炎的圈养毛猴中分离得到WMHBV。松鼠猴可以感染WMHBV,并可表现出持续6~8个月的病毒血症。研究表明,狨猴肝原代细胞和诱导多能干细胞来源的肝样细胞支持HBV和更有效的WMHBV感染,且WMHBV preS1 1~48残基嵌合HBV病毒的感染效率高于野生型HBV。CMHBV最初是从金腹悬猴中分离鉴定出,其可通过hNTCP感染人肝癌细胞。这些嗜肝病毒的发现为建立猴模型提供了依据,但是其与HBV之间仍然存在差异。
WHV在病毒学特征上与HBV相似,包括基因组大小、结构、核苷酸序列(60%~70%相似性)和蛋白表达,且在病毒感染时宿主的先天和适应性免疫反应方面也十分相似。因此,该模型已被用于评价抗HBV药物和筛选针对HBV的免疫治疗策略。然而,土拨鼠与人类的遗传背景仍然存在差异,并不能完全真实地反映人感染HBV的状态。
DHBV由Mason等在北京鸭血清中发现。DHBV感染北京鸭模型价格经济、易饲养与操作,早期被广泛应用于研究HBV基因突变、病毒的免疫清除机制以及筛选HBV抗病毒药物。然而,DHBV与人HBV的同源性较低(约40%),且其不含X-ORF,使其在研究HBV分子机制方面受限。此外,不同种类的鸭感染DHBV后的表现形式也存在差异,因此该模型仍然无法完全模拟人HBV感染的全过程。
近年研究发现了一种新型猫嗜肝病毒——DCH,其感染与猫慢性肝炎相关。DCH具有部分双链、环状的DNA基因组,长度约为3 200个碱基,与其他嗜肝病毒类似,DCH的基因组包含P、S、C和X-ORF。值得注意的是,DCH的preS1序列在遗传上比WHV或北极地松鼠乙型肝炎病毒更接近人类HBV,提示DCH preS1可能具有与HBV preS1类似的功能。与HBV不同,DCH的X蛋白降解染色体结构维持蛋白6并不依赖于DNA结合蛋白1。此外,DCH感染的猫会出现持续性病毒血症和肝脏炎症,同时也可以通过整合导致猫肝癌的发生。

4小结
HBV研究长期受到缺乏理想动物模型的限制,现有的模型体系包括黑猩猩、树鼩、小鼠及其他潜在宿主(如猫、猪和仓鼠等),以及利用相关嗜肝病毒(如WHV、DHBV和DCH等)建立的替代模型。这些模型在HBV感染、复制、免疫反应及肝病进展等方面提供了宝贵的信息,但均存在一定局限:灵长类模型虽能较好地模拟人类感染过程,但受伦理与成本限制;树鼩模型可支持感染过程,却难以稳定维持慢性感染;小鼠模型虽具有高可操作性与遗传可塑性,却普遍缺乏对HBV的自然易感性。近年来,人源化肝脏和免疫系统的小鼠模型、NTCP转基因模型以及基于病毒载体的感染模型等新技术的出现,显著推动了HBV感染及cccDNA生物学研究的进展。同时,对HBV受体跨物种差异和宿主限制因子的深入解析,也为构建新型感染模型提供了理论基础。
未来,构建能够同时再现HBV完整生命周期、宿主免疫应答及慢性肝病进展的理想模型,仍是该领域的核心挑战之一。随着基因编辑、人源化重建、多器官类器官及体内-体外联合系统等的不断发展,多维度、互补性的HBV研究模型体系有望逐步建立。这将为深入阐明HBV感染与宿主相互作用机制、揭示cccDNA维持与清除规律,以及开发根治性抗HBV疗法,提供坚实的实验基础与技术支撑。

https://www.lcgdbzz.org/cn/article/doi/10.12449/JCH260105

徐在超, 夏宇尘. 乙型肝炎动物模型的研究现状与挑战[J]. 临床肝胆病杂志, 2026, 42(1): 26-32
来源:临床肝胆病杂志
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
